Аноксигенный фотосинтез
Фотосинтетический транспорт электронов у анаэробных фототрофных бактерий во многих отношениях отличается от только что описанного. В аноксигенном фотосинтезе участвует только одна световая реакция; она поддерживает циклический транспорт электронов. Электроны, покидающие цикл для восстановления NAD, не являются продуктом разложения воды. Фотосинтез зависит от наличия в среде восстановленных субстратов и не сопровождается выделением 02. Собственно фотореакция хотя и аналогична первой фотореакции у зеленых растений, однако у некоторых бактерий она приводит, вероятно, лишь к созданию протонного потенциала и тем самым к запасанию энергии (АТР), но не к восстановлению NAD. Таким образом, нециклический перенос электронов (от донора электронов к пиридиннуклеотиду) здесь отсутствует. По-видимому, NADH2 образуется в результате какой-то темновой реакции в ходе обратного транспорта электронов, протекающего с затратой энергии.
Следует, однако, заметить, что у фототрофных бактерий между отдельными группами существуют гораздо большие различия в составе пигментов и механизмах фотосинтеза, чем у зеленых растений. В последующем изложении мы вначале не будем касаться зеленых бактерий.
Фотореакция у пурпурных бактерий.Как уже говорилось, у пурпурных бактерий пигменты и компоненты электрон-транспортной системы тоже находятся в мембранах. Пигментный комплекс фотохимического реакционного центра удается отделить от пигментов антенны.
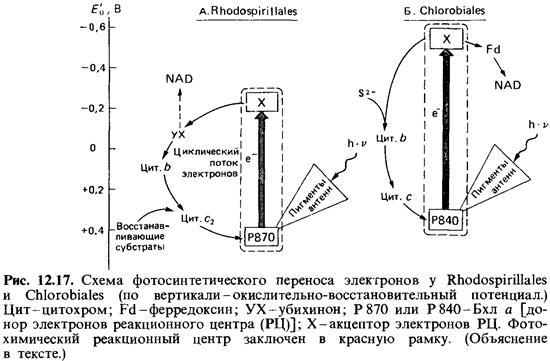
Энергия, поглощенная пигментами антенны (бактериохлорофиллом и каротиноидами) передается реакционным центрам. Изолированные реакционные центры состоят из белкового комплекса, содержащего Бхл а,бактериофеофитин, каротиноиды, убихинон и железосерный белок (FeS-белок). Пигмент реакционного центра обозначают Р870~по длине волны, при которой максимально снижается поглощение под действием света. На свету Р870 окисляется в Р870+. Окислительно-восстановительный потенциал этого донора электронов лежит между + 450 и + 490 мВ. Первичным акцептором электронов, вероятно, служит комплекс убихинона с FeS-белком. Окислительно-восстановительный потенциал этого комплекса должен быть близок к -100 мВ. Поэтому кажется маловероятным, что электроны, возбуждаемые при световой реакции у пурпурных бактерий, способны восстанавливать NAD. Скорее, они возвращаются через убихинон, цитохромы Ьи с2 и, возможно, FeS-белки назад к Р870 + (рис. 12.17). Необходимые же для восстановления NAD электроны, видимо, покидают путь циклического транспорта. Они переносятся на NAD в результате обратного транспорта, протекающего с затратой АТР.Это существенное отличие от в остальном аналогичной первой фотореакции при оксигенном фотосинтезе. Для пополнения цикла электронами пурпурные бактерии нуждаются во внешних донорах электронов. Пурпурные серобактерии могут использовать с этой целью сероводород, серу или тиосульфат; органические соединения (малат, сукцинат и др.) и молекулярный водород служат донорами электронов для обеих групп пурпурных бактерий.
Как показали многочисленные эксперименты, и у пурпурных бактерий фотосинтетический перенос электронов приводит к созданию протонного градиента. Интактные клетки реагируют на воздействие света выделением в среду протонов, приводящим к закислению среды. В суспензии пузырьков из фотосинтетических мембран (хроматофоров) свет вызывает перенос протонов, направленный внутрь. Таким образом, мембраны хроматофоров и тилакоидов имеют такую же полярность, как и субмитохондриальные пузырьки. Это будет понятно, если учесть, что все эти мембраны образуются путем впячивания внутрь и разрастания плазматической мембраны или же внутренней мембраны хлоропласта. Хотя точная локализация отдельных компонентов в мембране еще не установлена, можно думать, что переносчики водорода и электронов расположены и в мембране анаэробных фототрофных бактерий таким образом, что происходит разделение зарядов. В хроматофорах электроны транспортируются наружу, а протоны - внутрь. Создающийся протонный потенциал и служит движущей силой фотосинтетического фосфорилирования.
Фотореакция у зеленых бактерий.Механизмы фотореакции у зеленых бактерий еще не полностью выяснены. Есть указания на то, что первичный акцептор электронов, участвующий в световой реакции, у зеленых серобактерий обладает потенциалом около - 500 мВ (у пурпурных бактерий - всего лишь - 100 мВ!). При столь большом отрицательном потенциале становится возможным прямое использование электронов от первичного акцептора для восстановления ферредоксина и пиридиннуклеотида (рис. 12.17). Таким образом, восстановительную силу Chlorobiaceae, возможно, получают не путем обратного транспорта электронов, требующего затрат энергии. Такая независимость от обратного транспорта электронов была бы важной отличительной чертой фотосинтеза у зеленых бактерий по сравнению с пурпурными. Тогда фотореакция у Chlorobiaceae не уступала бы по своей эффективности первой фотореакции цианобактерий. С эволюционной точки зрения фотосинтез зеленых бактерий мог бы быть связующим звеном между фотосинтезом пурпурных бактерий и фотосинтезом цианобактерий и растений1.
Дата добавления: 2015-04-25; просмотров: 4206;
