Структура типу нікеліну
Структура арсеніду нікелю є поширеною для мінералів перехідних металів, особливо сульфідів та арсенідів. У структурах такого типу атоми перехідних металів займають всі октаедричні порожнини у щільноупакованих гексагональних ґратках аніонів, а аніони оточуються шістьма атомами перехідних металів з утворенням тригональних призм. На кожну октаедричну порожнину припадає дві незаселені тетраедричні порожнини. Октаедри мають спільні грані із сусідами уздовж осі с, а пари тетраедрів мають спільну грань, створюючи тригональні біпірамідальні порожнини. Структура NiAs виявляє дві важливі ознаки: 1) вона здатна вміщати в тригональні біпірамідальні порожнини додаткові атоми перехідних металів, максимальне число яких досягається при складі М2Х; 2) у ній можлива поява вакансій атомів металів, як впорядкованих так і хаотично розподілених у площинах, перпендикулярних осі с.
Проста структура NiAs є звичною для сполук перехідних металів, стійких при високих температурах і високому тиску. Ця структура відома в нікеліні NiAs і споріднених йому брейтгауптиті NiSb і лангиситі (Co,Ni)As, у високотемпературному «моносульфідному твердому розчині» Fei-xS –Nii-xS (скорочено mss), який можна вважати важливим попередником багатьох сульфідів Fe і Ni у магматичних родовищах міді і нікелю. Структура типу NiAs рідко зберігається при низьких температурах. У цих умовах виникають надструктури, і спотворені структури.
Важливим прикладом надструктур, що базуються на структурі NiAs, є структури сульфідів заліза з вакансіями металу, які складають групу піротину. Високотемпературні форми FeS, CoS і NiS володіють дійсною структурою NiAs, структура ж низькотемпературних мінералів характеризується різними спотвореннями, що проявляється у вигляді незначних переміщень атомів в FeS або ж повністю відмінної структури мілериту NiS.
Структури AX2.
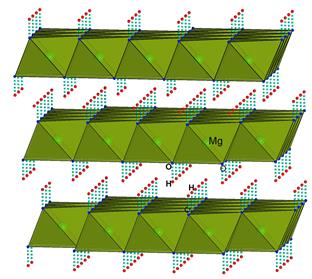
Cтруктура типу бруситу Mg(OH) 2
Рис. 5.5. Структура бруситу.
Тип молекулярної структури, у якій домінують безконечні плоскі молекули – шари із октаедричних поліедрів Mg(OH)6, зв’язані між собою водневими зв’язками
Структури типу рутилу TіO2
| 
|
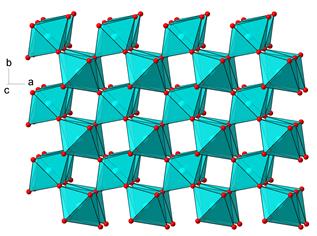
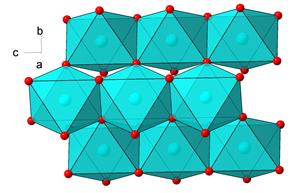
Рис. 5.6. Структура рутилу
Структура формується із ланцюжків октаедричних позицій Ti4+O6, зв’язаних між собою ребрами. Самі ж ланцюжки зв’язані між собою вершинами.
Структура такого типу належить каситериту SnO2.
Структури типу флюориту
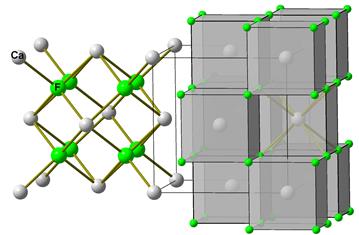
Рис. 5.7. Структура флюориту
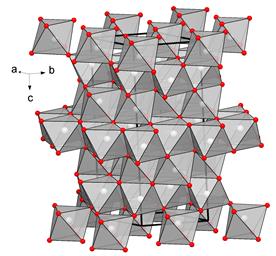
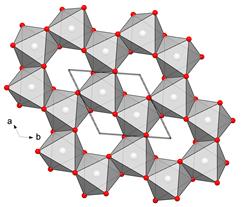
Структури A2X3 (структури корунду та гематиту). У ній всі катіони мають КЧ = 6, причому катіонні октаедри також попарно об'єднують свої грані. Структуру, похідну від Аl2О3 (Fe2O3), мають мінерали роду ільменіту, в яких в парі з Ti4+ виступають Fe2+, Mg2+ (r = 18,8) або Мn2+ (r = 17,5). Таким чином, всі ці мінерали є типовими подвійними оксидами. Вони мають не тільки однакові КЧ катіонів, але і типово катіонний мотив, для якого характерне усуспільнення ребер і навіть граней катіонних поліедрів.
| 
|
Рис. 5.8. Структура корунду.
Структура перовськіту ABO3
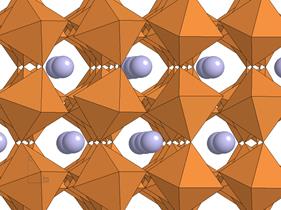 Структура перовськіту CaTiO3, містить дві катіонних кристалохімічних позиції – Ti4+ і Са2+ (r = 8,3), що істотно відрізняються як по КЧ (КЧ у Са = 12, у Ti = 6), так і по мотиву. Основу структури перовськіту утворює каркас з Ti-октаедрів, пов’язаних вершинами. В каркасі є крупні порожнини, в яких знаходяться катіони Са2+. Шарнірне з'єднання Ti-октаедрів дає можливість їм змінювати кут зв'язку Ti-О-Ti, що дозволяє каркасу пристосовуватися до різних катіонів, хоча при достатньо сильних його спотвореннях симетрія структури стає нижче ідеально кубічної.
Структура перовськіту CaTiO3, містить дві катіонних кристалохімічних позиції – Ti4+ і Са2+ (r = 8,3), що істотно відрізняються як по КЧ (КЧ у Са = 12, у Ti = 6), так і по мотиву. Основу структури перовськіту утворює каркас з Ti-октаедрів, пов’язаних вершинами. В каркасі є крупні порожнини, в яких знаходяться катіони Са2+. Шарнірне з'єднання Ti-октаедрів дає можливість їм змінювати кут зв'язку Ti-О-Ti, що дозволяє каркасу пристосовуватися до різних катіонів, хоча при достатньо сильних його спотвореннях симетрія структури стає нижче ідеально кубічної.
Рис. 5.9. Структура перовськіту.
Структура типу шпінелі AB2X4
Основою структури шпінелі є кубічна найщільніша упаковка аніонів, в якій половина октаедричних порожнин і одна восьма тетраедричних порожнин заповнені катіонами. Кубічна елементарна ґратка містить вісім формульних одиниць. Двовалентні і тривалентні катіони займають тетраедричі (А) і октаедричні (В) позиції в структурі. Аніонна позиція (Х) може заселятися киснем (в оксишпінелях) або сіркою (в тіошпінелях).
Паралельно {111} виділяються два типи шарів, що чергуються між собою (рис. ):
1) октаедричні, заповнені із співвідношенням заселених і незаселених порожнин 3:1, аналогічно корундовому шару;
2) октаедрично-тетраедричні із одинокими октаедрами, зв’язаними тетраедрами, таким чином, що кожний октаедр оточений 3+3 тетраедрами, зв’язаними із вершинами нижньої і верхньої грані октаедра.
 а.
а.
|  б.
б.
|
 в.
в.
|  г.
г.
|
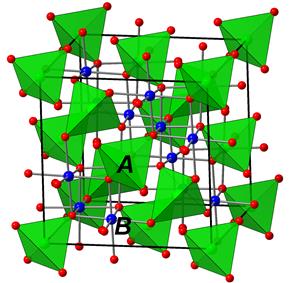
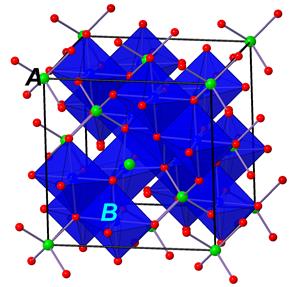
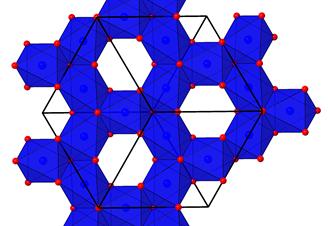
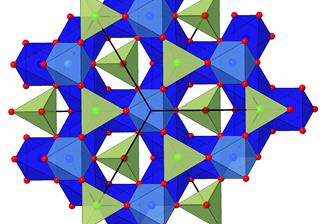
Рис. 5.10. Структура шпінелі.
У верхньому ряді показано розподіл тетраедричних (А) (а) і октаедричних позицій (В) (б) в елементарній комірці шпінелі. Зверніть увагу на чергування тетраедрів із різною орієнтацією в напрямку {111}.
У нижньому ряді зображені два типи шарів, що виділяються перпендикулярно {111} – октаедричний (в) і октаедрично-тетраедричний (г), зображений вище (тому світліший) октаедричного.
Якщо двовалентні катіони заповнюють позиції А, такий тип шпінелі називається нормальним; у інверсних шпінелях двовалентні катіони містяться в позиції В, а тривалентні катіони – як в октаедричних (В) і тетраедричних (А) позиціях. Існують змішані (невпорядковані) шпінелі, в яких октаедричні та тетраедричні шпінелі заселяються двох і трьохвалентними атомами в довільному порядку.
Кожен атом кисню чи сірки координується чотирма катіонами; три з них локалізуються в октаедричних позиціях В, наприклад, уздовж напрямів [100], [010] і [001], і один - в тетраедричній позиції А уздовж напряму [111].
Оксиди і сульфіди з групи шпінелей звичайно відносяться до кубічних просторових груп Fd3m та F43m.
До оксишпінелей відносять мінерали групи шпінелі MgAl2O3, серед них магнетит FeFe2O3 і хроміт FeCr2O3. До тіошпінелей відносять полідіміт Ni3S4, лінеїт Co3S4 і ґрейгіт Fe3S4. Похідну від шпінелевої структуру мають зігеніт (Co,Ni)3S4 і віоларит FeNi2S4. Крім того, існують природні селеношпінелі: борнхардтит Co3Se4, трюстедтит Ni3Se4.
Дата добавления: 2015-05-21; просмотров: 918;
