ВАПНУВАННЯ, МАГНЕЗІЙНЕ ВИДАЛЕННЯ СПОЛУК КРЕМНІЮ І СОДУВАННЯ ВОДИ
Вапнування води, тобто обробка води вапном, було відоме давно і раніше застосовувалося для зм'якшування води при підживленні котлів низького тиску. Проте у зв'язку з підвищенням параметрів пари і широким вживанням іонного обміну воно почало застосовуватися для поліпшення роботи іонообмінної частки ВПУ. В даний час основне призначення вапнування – зниження бікарбонатної лужності води. Одночасно з цим зменшуються жорсткість, солевміст, концентрації грубодисперсних домішок, з'єднань заліза і кремнієвої кислоти.
Підвищення рН води з метою зниження бікарбонатної лужності проводиться гашеним вапном Са(ОН)2, яке подається у воду у вигляді суспензії (вапняного молока).
Вапно, введене|запроваджувати| у воду, дисоціює|:
| Са(ОН)2 ⇄Са2+ + 2ОН–, | (2.40) |
внаслідок чого в розчині підвищується концентрація іонів Са2+ і ОН–. Це приЗводить до скріплення частки іонів Н+ в малодисоційовані молекули води
| H+ + OH– ⇄ H2O, | (2.41) |
оскільки іонний добуток Kw – постійна величина для даної температури.
Таким чином, рН зростає, що викликає зсув вуглекислотної рівноваги у бік утворення іонів СО32–, в які переходять всі форми вугільної кислоти. Збільшення концентрації СО32– викликає реакцію утворення важкорозчинного карбонату кальцію
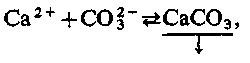
| (2.42) |
яка протікатиме за умови, що
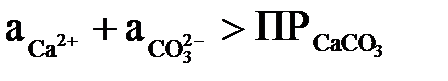 , ,
| (2.43) |
де 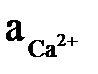 і
і 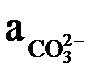 – активності іонів Са2+ і СО2 в розчині;
– активності іонів Са2+ і СО2 в розчині;
ПРСаСО3 – добуток розчинності СаСО3, рівний, зокрема, при температурі води 308 К 4,8·10–9.
Якщо доза вапна перевищує необхідну дозу для переводу всіх форм вугільної кислоти в карбонат-іони, утворюватиметься гідроокис магнію (ПРМg(ОН)2 = 5,5·10–12).
Необхідну для проведення процесу дозу вапна можна підрахувати|підсумовувати|, виходячи з таких рівнянь реагуючих речовин:
| Са(ОН)2 ⇄Са2+ + 2ОН–; | (2.44) |
| СО2 + 2ОН– ⇄СО32– +Н2О; | (2.45) |
| НСО3– + ОН– ⇄СО32– + Н2О; | (2.46) |
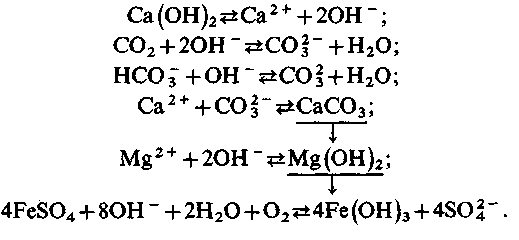
| (2.47) |
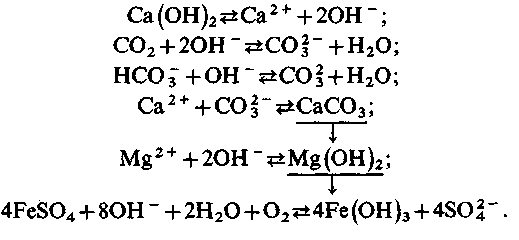
| (2.48) |
| 4Fe SO4 + 8ОН– +2Н2О + O2 ⇄4Fe(ОН)3 + 4SO42–. | (2.49) |
Реакція (2.49) вказує на те, що при проведенні спільно з вапнуванням процесу коагуляції частка іонів ОН– витрачається на гідроліз коагулянту і, отже, потрібна певна кількість вапна на цей процес.
Якщо основним призначенням вапнування є глибоке зниження бікарбонатної і карбонатної лужності води, то в розчині повинна виконуватися умова 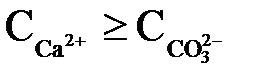 . Концентрація іона СО32–, що утворюється, мг-екв/кг, згідно (2.45) і (2.46) з урахуванням того, що в еквівалентних одиницях кількість іонів СО32–, що утворюються, буде в 2 рази більше кількості руйнованих іонів HCO3–, а також того, що практично ця реакція не йде до кінця при деяких значеннях рН, виражатиметься рівнянням
. Концентрація іона СО32–, що утворюється, мг-екв/кг, згідно (2.45) і (2.46) з урахуванням того, що в еквівалентних одиницях кількість іонів СО32–, що утворюються, буде в 2 рази більше кількості руйнованих іонів HCO3–, а також того, що практично ця реакція не йде до кінця при деяких значеннях рН, виражатиметься рівнянням
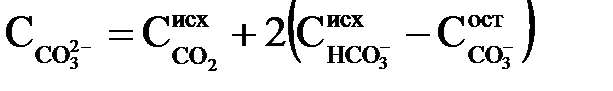
| (2.50) |
Концентрація іонів Са2+ визначається сумою іонів, що спочатку містяться у воді 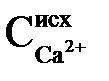 і введених з вапном еквівалентно іонам гідроксилу. Останні витрачаються згідно (2.45), (2.46), (2.49) на скріплення вільного СО2, розкладання бікарбонат-іонів в кількості, еквівалентній
і введених з вапном еквівалентно іонам гідроксилу. Останні витрачаються згідно (2.45), (2.46), (2.49) на скріплення вільного СО2, розкладання бікарбонат-іонів в кількості, еквівалентній 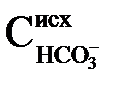 –
– 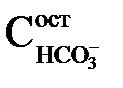 і на гідроліз коагулянту Dк. Таким чином, сумарна концентрація іонів Са2+, мг-екв/кг, буде рівна
і на гідроліз коагулянту Dк. Таким чином, сумарна концентрація іонів Са2+, мг-екв/кг, буде рівна
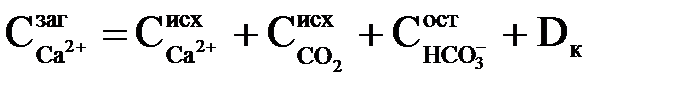 . .
| (2.51) |
Мінімальна доза вапна, мг-екв/кг, при цьому складе
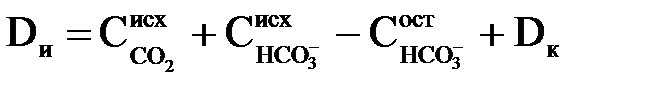 . .
| (2.52) |
З наведених рівнянь видно, що умова 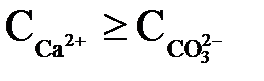 виконується, коли
виконується, коли
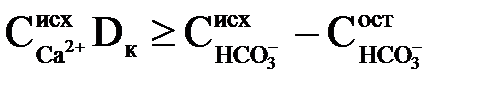 . .
| (2.53) |
Якщо початкова кальцієва жорсткість більше різниці між початковою і залишковою бікарбонатною лужністю, то доза вапна, що визначається з (2.52), достатня. Проте на практиці вельми вигідне переведення іонів Mg2+ в осад, для чого потрібне введення додаткової кількості вапна. При цьому концентрація іонів Са2+, мг-екв/кг, у вапнованій воді зростає еквівалентно зменшенню іонів Mg2+ і може бути визначена з рівняння
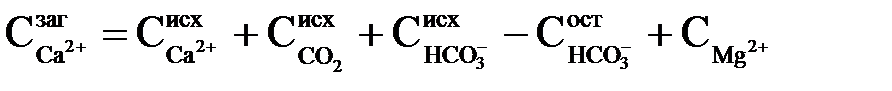 , ,
| (2.54) |
тоді умова 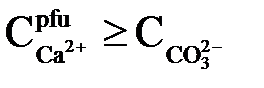 повинно виконуватися у формі
повинно виконуватися у формі
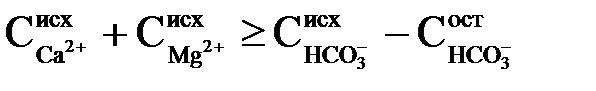
| (2.55) |
або
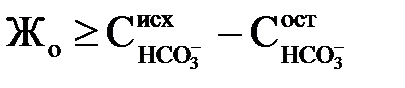 . .
| (2.56) |
Це співвідношення справедливе для переважної|гнітючого| більшості природних вод, і тому доза вапна, що визначається наведеним вище методом, дійсно приведе до зниження лужності| води.
Практично для зсуву в необхідному напрямі реакцій, що відбуваються при вапнуванні, вводиться деякий надлишок вапна для встановлення заданого значення рН. Величина цього надлишку вапна зазвичай невелика (0,1 – 0,2 мг-екв/кг). З врахуванням виділення в осад гідроокису магнію і введення надлишку вапна И його доза, мг-екв/кг, складе
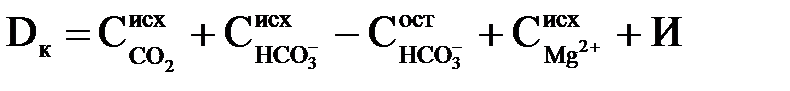
| (2.57) |
Солевміст води при її вапнуванні зменшується на величину карбонатної жорсткості (при 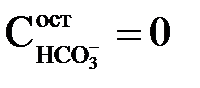 ) за вирахуванням введеного надлишку вапна і розчинності СаСО3 і Mg(ОН)2.За умови, що в початковій воді Жо=Що, і при рівноважному стані системи концентрацію іонів кальцію, г-іон/кг, що залишаються в розчині, згідно добутку розчинності СаСО3 можна визначити як
) за вирахуванням введеного надлишку вапна і розчинності СаСО3 і Mg(ОН)2.За умови, що в початковій воді Жо=Що, і при рівноважному стані системи концентрацію іонів кальцію, г-іон/кг, що залишаються в розчині, згідно добутку розчинності СаСО3 можна визначити як
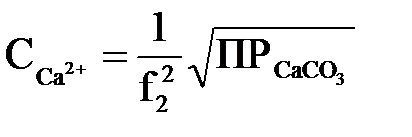
| (2.58) |
де f22 – коефіцієнт активності іонів Са2+ і СО32– в розчині.
Теоретично ця концентрація невелика (приблизно соті долі мг-екв/кг). При певному значенні добутку розчинності Mg(ОН)2 ще менше значення має концентрація іонів Mg2+. Проте практично жорсткість вапнованої води знижується не настільки значно. По-перше, при вапнуванні не зменшується некарбонатна жорсткість, хоча вона і змінюється якісно. Замість хлоридів, сульфатів кальцію і магнію у воді залишаються лише хлориди і сульфати кальцію. По-друге, на практиці процес зниження бікарбонатної лужності досить далекий від рівноваги, і тому у воді є концентрація кальцію, обумовлена наявністю залишкової концентрації бікарбонатів. Річ у тому, що іонні процеси у воді відбуваються швидко, а кристалізація твердої фази – дуже повільно, і саме вона визначає час, необхідний для завершення процесу вапнування. Співвідношення між концентраціями НСО3– і СО32– у воді при вапнуванні повністю визначається значенням рН. Якщо на практиці це значення підтримується на рівні 10,2 – 10,3, то цього достатньо для практично повного переведення НСО3– у СО32–.
Склад домішок води має визначальне значення при необхідності застосування процесу вапнування. Вапнування застосовується при великих значеннях лужності води (>2,0 мг-екв/кг) і малої різниці між її Жо і Що.
Приклад 2.1.Розрахувати за допомогою таблиці рівноважний склад іонних домішок в природній воді, обробленої методами коагуляції і вапнування:
| Концентрація | Іони | |||||
| SO42– | Cl– | HСО3– | Na+ | Mg2+ | Са2+ | |
| мг/л мг-екв/л г-іон/(л ×10–3) | 96,1 2,0 1,0 | 138,4 3,9 3,9 | 268,5 4,4 4,4 | 110,4 4,8 4,8 | 28,8 2,4 1,2 | 64,0 3,2 1,6 |
При перерахунку масових концентрацій окремих іонів в мілінормальні, треба|прямує| величини концентрацій, мг/л, розділити на еквівалентні маси відповідних іонів, наприклад для іона SO42– – 96,1/48,03, для іона НСО3– 268,5/61,02 і т.д.
Перевірка правильності аналізу:
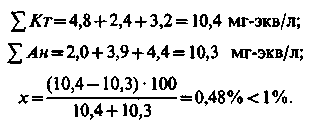
Технологічні показники якості води, мг-екв/л:
Жо = 3,2 + 2,4 = 5,6; Жк = 4,4; Жнк = 5,6 – 4,4 = 1,2; Ло = Лк = 4,4.
Солевміст початкової води
с/с = Σ(Кт + Ан) =706,2 мг/л.
Значення іонної сили початкової|вихідної| води
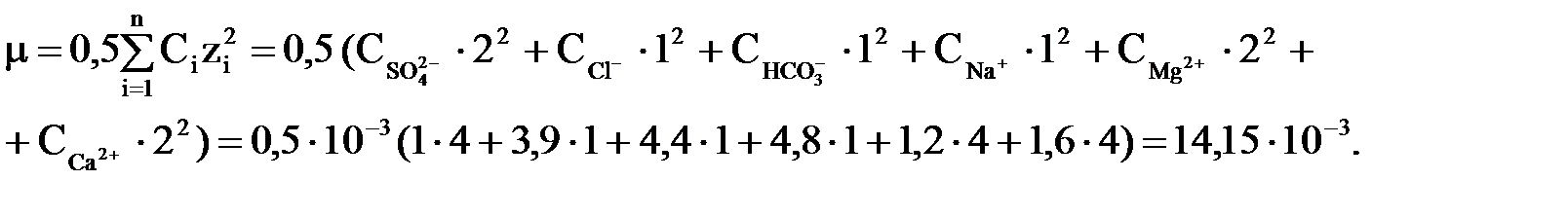
Активність іонів в початковій воді
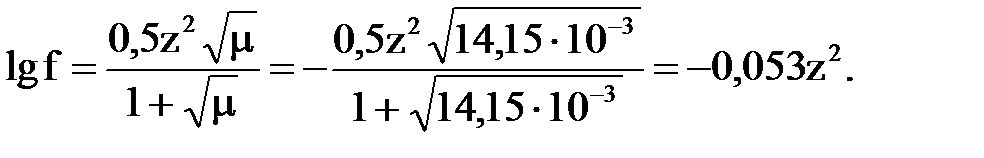
Тоді f1=0,885; f2=0,614; f3 = 0,334.
Додаємо у воду дозу коагулянту Dк = 0,75 мг-екв/л і вапно в такій кількості, щоб|аби| у воді встановилося оптимальне значення рН = 10,3| при температурі води, рівній 313 К.
За цим значенням рН знаходимо концентрації іонів Н+ і ОН–:
рН = 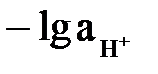 = 10,3;
= 10,3;
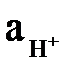 = 5,15 · 10–11;
= 5,15 · 10–11; 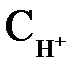 = 5,15 · 10–11/0,885 = 5,82 · 10 –11 г-іон/л.
= 5,15 · 10–11/0,885 = 5,82 · 10 –11 г-іон/л.
Відповідно активність і концентрація іонів ОН–
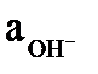 = 2,92 · 10–14/(5,15 · 10–11) = 0,567 · 10–3;
= 2,92 · 10–14/(5,15 · 10–11) = 0,567 · 10–3;
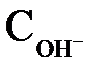 = 0,567 · 10–3/0,885 = 0,641 · 10 –3 г-іон/л.
= 0,567 · 10–3/0,885 = 0,641 · 10 –3 г-іон/л.
У попередньому розрахунку не враховано, що концентрації деяких іонів унаслідок введення у воду реагентів змінилися. Так,
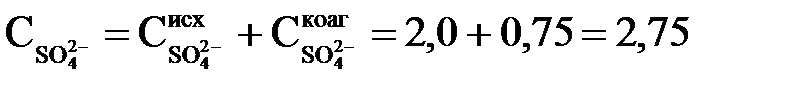 мг-екв/л = 1,375 · 10–3 г-іон/л.
мг-екв/л = 1,375 · 10–3 г-іон/л.
В процесі коагуляції утворюються з'єднання Fe(ОН)2 і Fe(ОН)3. Їх добутки розчинності відповідно дорівнюють 1 · 10–15 і 3,2·10–38.
Тоді залишкові концентрації іонів Fe2+ і Fe3+
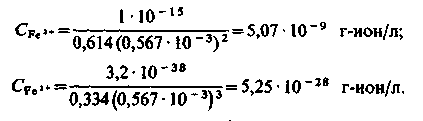
Залишкова концентрація іонів Mg2+
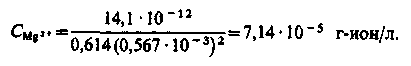
Залишкова концентрація іонів Са2+ невідома, невідома і концентрація іонів СО32– , тому, позначаючи першу як х, запишемо
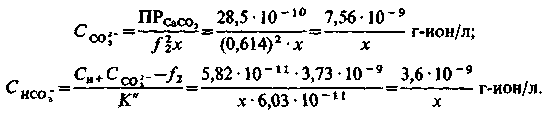
Залишкову концентрацію іонів Са2+ шукаємо через рівняння електронейтральності
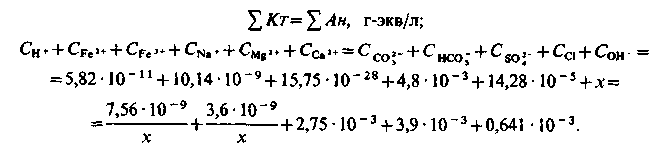
Нехтуючи малими значеннями, отримуємо|одержуємо| квадратне рівняння
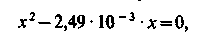
звідки х = 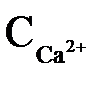 = 2,5 · 10–3 г-екв/л = 1,25 · 10–3 г-іон/л.
= 2,5 · 10–3 г-екв/л = 1,25 · 10–3 г-іон/л.
Тоді
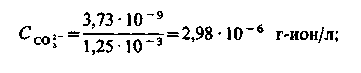
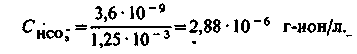
У цих розрахунках використовувалися значення μ і f, визначені через початковий склад природної води. Але ці значення змінилися, оскільки після введення реагентів змінилися концентрації іонів. Тому розрахунок вимагає уточнення, яке проводиться методом ітерації. Для цього, використовуючи набуті значення концентрацій іонів, визначаємо μ і f. Так, при першому наближенні отримуємо
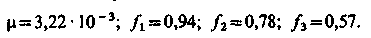
Отримані|одержувати| чинники|фактори| активності використовуються для перерахунку концентрацій іонів. Розрахунок проводиться до сходження значень іонної сили розчину в подальшому|наступному| і попередньому наближеннях. При цьому слід пам'ятати, що активність іонів ОН–, що визначає задане значення рН| води, не змінюється, змінюється лише їх масова (молярна) концентрація. Ця концентрація, мг-екв/л, складатиме надлишок вапна при дозуванні останньої у воду.
Якщо 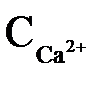 набагато більше
набагато більше 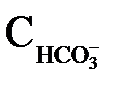 і необхідно провести глибше зм'якшування води, то операцію вапнування доповнюють содуванням, для чого окрім вапна дозують Na2CO3. При цьому відбуваються наступні реакції:
і необхідно провести глибше зм'якшування води, то операцію вапнування доповнюють содуванням, для чого окрім вапна дозують Na2CO3. При цьому відбуваються наступні реакції:
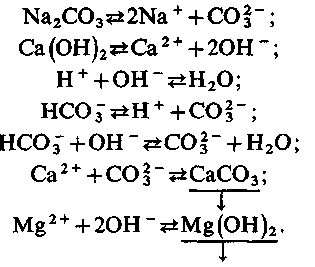
| (2.59) (2.60) (2.61) (2.62) (2.63) (2.64) (2.65) |
Якщо одночасно у воду подається коагулянт, то дози реагентів складають:
– доза вапна:
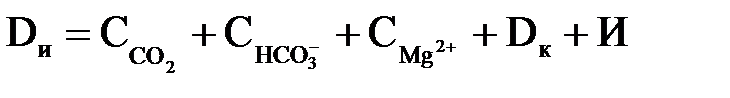
| (2.66) |
– доза соди:
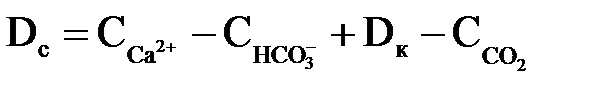
| (2.67) |
Рівноважна залишкова жорсткість води, мг-екв/л, обробленої таким чином, виражається|виказує| як
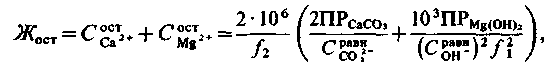
| (2.68) |
??????????
Тому у воду спеціально дозують з'єднання|сполуку| магнію – каустичний магнезит (70 – 80% MgO|). Механізм зниження концентрації кремнієвої кислоти полягає в тому, що колоїдна кремнієва кислота сорбується на поверхні, що містить|утримує| гідроокис магнію, яка утворюється в результаті| процесу вапнування, а також при гідролізі каустичного| магнезиту:
| MgO + H2O ⇄Mg(ОН)2. | (2.69) |
З іншого боку, гідроокис магнію частково дисоціює|:
| Mg(ОН)2 ⇄Mg(ОН) + + OH–, | (2.70) |
причому частка, що містить її, набуває електричного заряду. В умовах вапнування при рН = 10 ÷ 10,2 значна частина кремнієвої кислоти знаходиться в дисоційованому стані (ступінь дисоціації H2SiO3 по першому ступеню – близько 90%). Іони гідроксилу в цих умовах поступаються місцем іонам HSiO3–, які з'єднуються з гідроокисом магнію. Найбільш оптимальне значення рН для процесу видалення сполук кремнію з води повністю збігається з оптимальним значенням рН, прийнятим для вапнування, що істотно збільшує ефективність спільного процесу. Необхідна доза магнезиту (суспензія у воді) залежить від кремневмісту води і складає 10 – 20 мг/кг води. В результаті спільного застосування процесів коагуляції, вапнування і магнезійного видалення сполук кремнію залишковий вміст кремнієвої кислоти у воді знижується до 0,8 – 1,0мкг/кг незалежно від початкового кремневмісту. Якщо взяти до уваги, що при вапнуванні і коагуляції зниження кремневмісту відбувається приблизно на 40%, то можна у кожному конкретному випадку вирішувати питання про необхідність вживання процесу магнезійного видалення сполук кремнію.
Дуже велике значення при використанні методів осадження| мають процеси утворення часток|частинок| осаду. В наш час|нині| утворення твердої фази з|із| пересиченого розчину розглядають|розглядають| як результат протікання процесів агрегації| і орієнтації. Процес агрегації — це утворення кристалічних зародків, що проходять стадію колоїдного стану|достатку| з|із| придбанням|надбанням| електричного заряду, коагуляцію цих часток|частинок| і зростання|зріст| первинних кристалів. При орієнтації відбувається|походить| процес вдосконалення структури кристалів, що призводить|наводить| до зменшення їх питомої поверхні, а отже|, до збільшення розмірів кристалів. За співвідношенням швидкостей цих процесів визначають структуру осаду.
При переважанні процесу агрегації виходить аморфний осад, що складається з дрібних|мілких| часток|частинок|. Якщо ж переважає процес орієнтації, то виходить грубозернистий|крупнозернистий| кристалічний| осад. На швидкість процесів орієнтації впливає головним чином хімічна природа речовини. При осадженні простих полярних з'єднань|сполук| ця швидкість невелика, при утворенні гідроокисів – мала|. Структура осаду має велике значення для процесів його виділення з|із| розчину. Аморфний осад володіє добрими сорбціонними властивостями|, проте|однак| неміцний і має малу швидкість витання у воді (близько 1 мм/с), і навпаки, кристалічний осад володіє набагато більшою міцністю і швидкістю витання (продукти коагуляції зазвичай|звично| в нього не входять), але|та| має невелику сорбціонну| здатність|здібність|.
У експлуатаційних умовах необхідно забезпечувати стабільність вапнованої води, тобто нездатність до подальшої кристалізації твердої фази після|потім| виходу води з|із| освітлювача. В противном случае осад, що виділяється з|із| води, може істотно|суттєвий| утруднити роботу апаратів на наступних|таких| стадіях очищення води.
Одним з основних чинників|факторів|, сприяючих підвищенню ефективності процесів осадження, є|з'являється| підігрівання|підігрів| води. Основними причинами сприятливої дії підвищеної температури води є|з'являються| прискорення процесів кристалізації| твердої фази, поліпшення|покращання| відділення|відокремлення| осаду внаслідок|внаслідок| зменшення в'язкості води і зростання швидкості хімічних реакцій. Зазвичай|звично| при коагуляції температура води підтримується в діапазоні 303 – 308 К, а при вапнуванні – в| діапазоні 313 – 318 К з|із| відхиленням від прийнятої не більше ніж на 1 К, щоб уникнути виникнення конвективних токів|токів| в апаратах, що приводять|наводять| до порушення процесів освітлювання.
В наш час|нині| передочищення води проводиться|виробляє| в освітлювачах| із|із| завислим шаром осаду. Вся маса часток|частинок| твердої фази в цьому шарі знаходиться|перебуває| в стані динамічної рівноваги з|із| потоком води, що подається знизу. Завислі в потоці частки|частинки| твердої фази знаходяться|перебувають| в неперервному хаотичному русі, проте|однак| сам завислий шар в цілому|загалом| нерухомий. Найбільша швидкість осадження спостерігається біля|в| окремої частки|частинки| і за умови, що|при умові , що| Re < 2|, може бути записана як
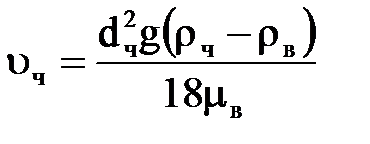 , ,
| (2.71) |
???????
По мірі накопичення часток|частинок| їх концентрація в шарі збільшується і виникає явище обмеженого осадження часток|частинок|, коли внаслідок|внаслідок| витрат|затрат| енергії на взаємотертя часток|частинок| швидкість осадження шару зменшується і, отже, для утримання шару часток|частинок| в завислому стані|достатку| необхідно| знижувати швидкість висхідного потоку води.
Кількісний зв'язок між необхідною швидкістю висхідного потоку води для підтримки шару в завислому стані|достатку| і концентрацією часток|частинок| в ньому виражається|виказує| рівнянням
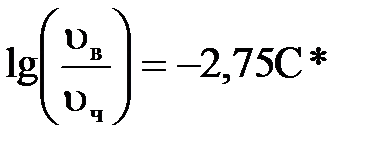 , ,
| (2.72) |
де υв – швидкістьвисхідного потоку води, м/с;
С* – масова концентрація часток в завислому шарі, кг/м3.
Ця обставина є|з'являється| основним чинником|фактором|, що дозволяє практично| здійснювати роботу освітлювачів із|із| завислим шаром. При зростанні швидкості потоку відбувається|походить| розширення шару і концентрація часток|частинок| в ньому зменшується. При цьому швидкість осадження шару зростає і він як би пристосовується до зміни гідродинамічної обстановки. Якщо швидкість потоку падає, то шар стискається|стискає| і швидкість його осадження також падає.
Основним достоїнством завислого шару осаду є|з'являється| те, що він працює за типом фільтруючого завантаження|загрузки|, витягуючи з|із| води, що протікає крізь нього, дрібнодисперсні частки|частинки| в результаті адгезйних| і сорбційних| процесів. При цьому ефективність процесу видалення|віддалення| таких часток|частинок| буде тим вище, чим більше концентрація часток|частинок|, складових завислого шару. Але|та| підвищення концентрації крупних часток|частинок| приводить|наводить| до зниження швидкості висхідного потоку води, а отже|, і продуктивності апарату. Тому у кожному конкретному випадку слід знаходити|находити| оптимальний варіант.
Швидкість зміни концентрації дрібних|мілких| часток|частинок|, що сорбуються великими, може бути пропорційна|пропорціональна| їх концентраціям:
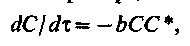
| (2.73) |
де С – поточнаконцентрація дрібних часток, кг/м3;
b – параметр процесу, що характеризує інтенсивність сорбції дрібних часток великими.
При заданій продуктивності апарату в технологічному процесі швидкість висхідного потоку постійна, і, отже, в будь-якому перетині шару х концентрація С* не змінюється. Тоді
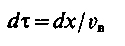
| (2.74) |
і (2.73) можна записати у формі
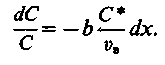
| (2.75) |
Інтегруючи в межах від Со до С і від 0 до Н, отримаємо
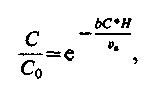
| (2.76) |
де Н – висота| завислого шару, м.
Природно, що сорбція дрібних|мілких| часток|частинок| з|із| об'єму|обсягу| води під час роботи освітлювача приведе до збільшення концентрації| С*, і тому необхідне постійне відведення надлишку з|із| об'єму|обсягу| завислого шару. Інакше з|із| підвищенням концентрації С*, щоб|аби| утримати цей шар в завислому стані|достатку|, доведеться|припаде| зменшити швидкість потоку води, а значить, і продуктивність освітлювача. Тому частина об'єму|обсягу| завислого шару безперервно відводиться в шламоуплотнитель|.
В наш час на ТЕС використовуються освітлювачі для коагуляції типа ЦНИИ МПС і для вапнування типа ВТИ. Освітлювачі ВТИ мають діапазон продуктивності від 63 до 1000 м3/ч (рис. 2.7). Освітлювачі виконані у вигляді ???????
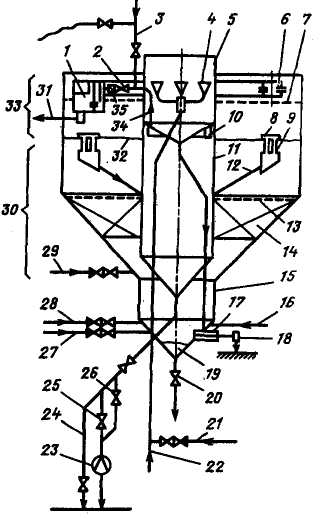
Рис. 2.7. Схема освітлювача марок ВТИ-400И, ВТИ-630И, ВТИ-1000И для вапнування води:
1– розподільний пристрій; 2 – задвижка «отсечки»; 3 – вода для промивання колектора шламоуплотнителя; 4 – розподільна система у воздухоотделителе; 5 – воздухоотделитель; 6 – кільцевий жолоб; 7 – верхня горизонтальна решітка; 8 – шламоприемные труби; 9 – шламоприемные вікна; 10 – перфорований колектор; 11 – шламоуплотнітель; 12 – шламоотводящие труби; 13 – горизонтальна решітка; 14 – вертикальні перегородки; 15 – камера змішування води і реагентів; 16 – сброс промивальної води з механічних фільтрів; 17 – введення води в освітлювач; 18 – регулюючий пристрій; 19 – грязевик; 20 – линия періодичного продування грязевика; 21, 28 – подача коагулянта; 22 – початкова вода; 23 – измерительная шайба; 24 – лінії спорожнення шламоуплотнителя; 25, 26 – продувочні лінії; 27 – подача вапняного молока; 29 – подача поліакриламіду; 30 – зона контактного середовища; 31 – вихід освітленої води; 32 – верхня границя завислого шару; 33 – зона освітленої води; 34 – отвод води з шламоуплотнителя в розподільний пристрій; 35 – дросельна заслонка
?????????
Декілька вище смесителя вводиться|запроваджує| флокулянт|. Передбачена також подача в смеситель води після|потім| промивання|промивки| механічних фільтрів для кращого формування твердої фази. В процесі перемішування в смесителе реагенти взаємодіють з|із| домішками|нечистотами| води і утворюється тверда фаза. Потім потік води, піднімаючись|підіймати| вгору|угору|, проходить через заспокійливу систему для зменшення обертального руху і поступає|надходить| в циліндрову частину|частину| освітлювача. На певній висоті цієї зони формується завислий шар. Для відведення частини|частини| шламу з|із| шару передбачені виносні шламоприемные| вікна, через які шлам потрапляє в шламоуплотнитель|. Ущільнений шлам виводиться з|із| освітлювача| з|із| продувочною| водою, а освітлена вода («отсечка») (≤ 20% продуктивності освітлювача) прямує в розподільний пристрій|устрій|. Основний потік освітленої води проходить через завислий шар, збирається кільцевим жолобом і також прямує в розподільний пристрій|устрій|, а потім в проміжний бак. Частина|частина| грубодисперсних речовин, що потрапили разом з початковою|вихідною| водою, а також крупні кристали осаду, що утворився, осідають в нижній| частині|частині| смесителя, що виконує функцію грязевика, і відводяться| з|із| нього.
Швидкість руху води через завислий шар в освітлювачах| типа|типу| ВТИ приймають в діапазоні 1,34 – 3,57 мм/с залежно від його продуктивності. Зміна продуктивності освітлювачів типа|типу| ВТИ допускається не вище 125% розрахункової. При хорошій|добрій| роботі освітлювача освітлена вода не повинна містити|утримувати| більше 10 мг/кг твердої фази.
Згідно нормам технологічного проектування ТЕС рекомендується встановлювати на передочищенні не менше двох освітлювачів з сумарною продуктивністю, що перевищує на 10% розрахункову потребу в освітленій воді Dосв.
Повна розрахункова продуктивність всіх встановлюваних освітлювачів Dр.п повинна враховувати витрату води на продування шламоуплотнителей qпр, а також годинну витрату води на промивання механічних фільтрів qф:
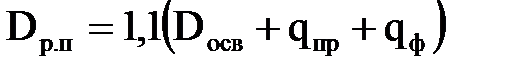 . .
| (2.77) |
Витрата води на безперервне продування з експлуатаційного досвіду можна прийняти рівним 0,03 Dpп.
Кількість освітлювачів дорівнює
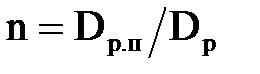 , ,
|
де Dp – розрахункова продуктивність одного освітлювача.
Воно має бути, виходячи з умов експлуатації, не менше двох і не більше чотирьох. З цих умов необхідно, враховуючи стандартний ряд освітлювачів, вибрати розрахункову продуктивність одного освітлювача.
Діаметр циліндричної частини|частини| освітлювача, м, з|із| коаксіально розташованими|схильними| шламоуплотнителем| і воздухоотделителем| визначається як
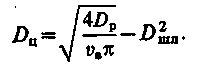
| (2.78) |
Діаметр шламоуплотнителя, м, можна визначити, виходячи з того, що швидкість підйому води в шламоуплотнителе складає близько 80% швидкості води в зоні завислого шару, а максимальне значення «отсечки» складає 10% Dp:
| (2.79) |
Висота ущільнювача розраховується з|із| умови необхідного часу перебування води в ньому для осадження шламу і виведення його з|із| освітлювача. Конічна частина|частина| освітлювача розраховується з|із| умови перебування води в цій частині|частині| протягом 10 – 15 хв., а висота воздухоотделителя – з умови|, що швидкість опускання води в ньому не повинна перевищувати 20 – 25 м/год., і за час опускання повітряні бульбашки повинні встигнути|устигати| досягти дзеркала води.
Розрахункові швидкості води, м/с, в інших вузлах освітлювача приймаються рівними: у трубопроводах, що підводяться і відводяться | 1,5 – 2,0; на виході з|із| сопла 0,8 – 1,75; підйомні в реакційній зоні 5,0 – 5,5; підйомні в зоні, що висвітлюється 4,0 – 4,5; у отворах верхніх грат 0,3.
Висота зони, що займається завислим шаром, складає залежно від продуктивності освітлювача від 2,8 до 4,9 м, а висота зони освітлювання (до збірного жолоба) – відповідно від 1,9 до 2,5 м..
Для нормальної роботи освітлювача необхідна безперервна дозована подача реагентів у воду. Для цього готують робочі розчини реагентів строго|суворий| постійних концентрацій, виходячи з вибраних доз цих реагентів. На рис. 2.8 показана схема розвантаження вапна і приготування концентрованого| розчину вапняного молока. Вивантаження вапна із|із| залізничного вагону проводиться|виробляє| в приймальний|усиновлений| бункер, звідки вона потім потрапляє в дробарку, в якій проводиться|виробляє| дроблення її крупних шматків. Роздроблене вапно потім подається шнековим| транспортером на елеватор і далі за допомогою шнеків – в залізобетонні бункери, що є|з'являються| акумуляторами вапна. По мірі потреби вапно з|із| цих бункерів поступає|надходить| у витратний бункер і потім|і тоді| за допомогою тарільчатого| питателя – в| апарат МИКА, в якому відбувається гасіння вапна освітленою водою. Концентроване вапняне молоко очищується від домішок|нечистот| (недопала|) у циклоні| і поступає|надходить| в залізобетонне ячейку|комірку|, а потім в міру необхідності за допомогою насосу через циклон, що представляє другий ступінь|рівень| очищення, подається у витратні баки-мішалки на ВПУ. Недопал дробиться на щічній дробарці і потім|і тоді| видаляється в систему гідрозоловидалення| або на шламовідвал|. У витратних баках (рис. 2.9) вапняне молоко розбавляється водою до робочої концентрації і насосами-дозаторами подається в освітлювач. У схему приготування і подачі робочого розчину вапняного молока включені насоси рециркуляції| і песколовушка|. На рис. 2.10 показана схема мокрого зберігання, приготування і подачі робочого розчину коагулянта. Коагулянт, що надходить на ТЕС, вивантажується з|із| вагону за допомогою транспортера в залізобетонне ячейку|комірку|, де розбавляється водою. Для грубого очищення розчину коагулянта в цьому ячейке встановлені|установлені| ящики, заповнені гранулами антрациту. Цей міцний розчин перепускається у вічко|комірку| чистого коагулянта і потім|і тоді| у витратні мірники, звідки після|потім| розведення водою насосами-дозаторами через фільтр тонкого очищення подається в освітлювач.
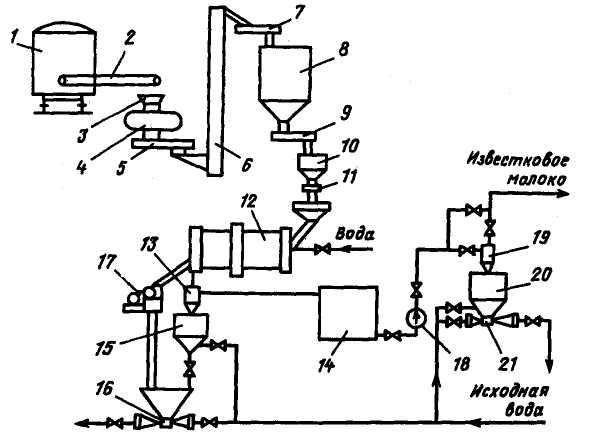
Рис. 2.8. Схема розвантаження вапна і приготування концентрованого розчину вапняного молока:
1 – залізничний вагон; 2 – стрічковий конвеєр; 3 – приймальний бункер; 4 – дробилка; 5 – шнековый конвеєр; 6 – елеватор; 7, 9 – транспортери; 8 – залізобетонний бункер; 7 – витратний бункер; 11 – тарільчатий питатель; 12 – аппарат МИКА; 13 – циклон; 14 – ячейка для концентрованого розчину; 15 – бункер недопала; 16 – апарат гідрошламовидалення; 17 – щічна дробарка; 18 – насос; 19 – циклон; 20 – бункер; 21 – шламоудалитель
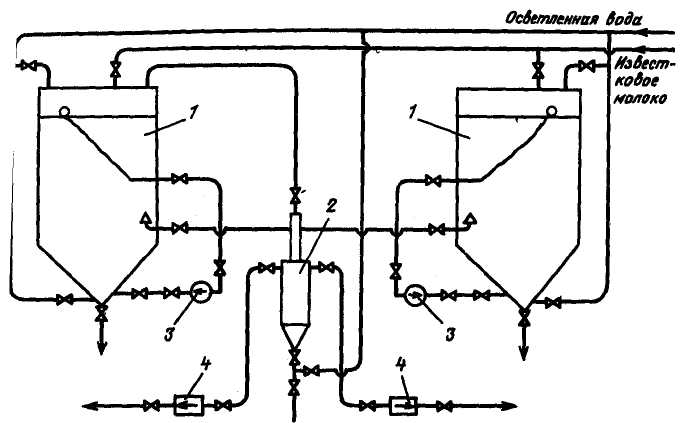
Рис. 2.9. Схема приготування і дозування вапняного молока:
1 – витратні баки-мішалки; 2 – песколовушка; 3 – насоси рециркуляції; 4 – насоси-дозатори.
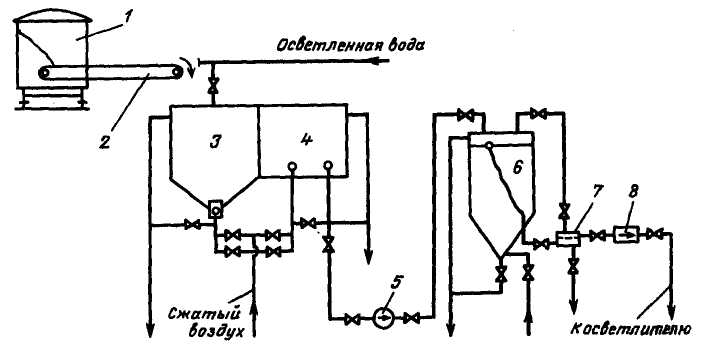
Рис. 2.10. Схема приготування і дозування коагулянта:
1 – залізничний вагон; 2 – конвеєр; 3 – вічка брудного розчину; 4 – ячейка чистого розчину; 5 – насос;6 – витратний бак-мірник; 7 – фільтр-сітка; 8 – насос-дозатор
Концентрація робочого розчину реагенту визначається за формулою
| Ср = Dр Dр.п · 103 / Dн.д, | (2.80) |
де Dp – доза коагулянта або вапна, мг-екв/л;
Dн.д– продуктивність насоса-дозатора, л/год.
Робочий об'єм|обсяг| бака-мішалки при подачі вапна або мірника при подачі коагулянта визначається за формулою
| Vм = Вм Сисх /Ср, | (2.81) |
де Вм – кількість концентрованого розчину реагенту, що подається в бак, л;
Сисх – концентрація міцного розчину, що подається в бак, мг-екв/л.
Робочі об'єми|обсяги| витратних баків повинні вибиратися з|із| розрахунку роботи не менше ніж однієї зміни. Концентрація робочого розчину вапняного молока складає 1500 – 2000 мг-екв/л, а робочого розчину коагулянта – 4 – 6% з розрахунку на|розраховуючи на| чисту речовину.
Дата добавления: 2015-05-19; просмотров: 1853;
