Глава 5. Влияние химического состава на структуру и свойства Ме
§1. Представление о диаграммах фазового равновесия (диаграммах состояния – ДС)
Пример: процесс кристаллизации расплав-кристалл (ж-тв)
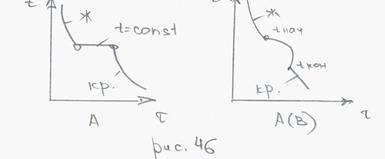
С = 1+1-2 = 0, такое превращение безвариантное и идет при постоянной температуре.
С = 2+1-2 = 1, кристаллизация твердого раствора обязана идти в интервале tн – tк, есть 1 степень свободы.
Общий закон выглядит так:
«Любое превращение подчиняется физическому правилу фазового равновесия, которое устанавливает четкое соответствие между числом компонентов К, числом фаз Ф и числом степеней свободы С, которые можно менять не влияя на фазовый состав»
К – А, В, С, …
Ф – ж, А, В, А(В), АmBn, …
С – t, P, концентрационный компонент.
При Р = const, С = К+1-Ф.
Выводы:
1. Условия протекания и превращения не случайны, температура начала и конца любого превращения названа критической точкой, например:
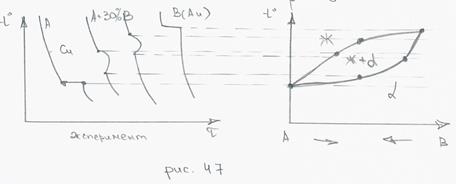
На любой диаграмме состояния между одинарными фазами есть двойные.
2. Совокупность критических точек начала и конца превращения образуют границу фазовых областей.
3. Диаграмма состояния показывает расположение всех границ фазовых областей в зависимости от составов сплавов и температуры.
§2. Основные (типичные) типы диаграммы состояния, их фазовый и структурный анализ
1. ДС сплавов, компоненты которых не ограниченно растворимы друг в друге.
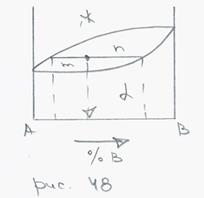
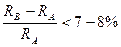 - одинаковые решетки.
- одинаковые решетки.
Фазовый анализ:
1) описать все фазы;
2) указать их на диаграмме;
3) для любых фаз диаграммы указать их состав и количество каждой фазы.
Итак, проведем анализ этой диаграммы:
1) ж – расплав, α – твердая фаза.
Точка 1 – фаза 1 , α – твердый раствор (100%), химический состав αх1.
Точка 2 – фаза 2, α+ж, температура t2.
2) химический состав: если фаз две, то химический состав определяется по правилу концентраций – проводят горизонталь до пересечения с ближайшими линиями, точка пересечения с границей показывает химический состав.
жхж + αхα, количество определяется по правилу обратных отрезков:
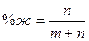 ,
, 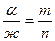 ,
, 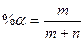 .
.
Структурный анализ.
Для любого сплава описать конечную структуру, она зависит от тех превращений, которые были в сплаве при охлаждении, любой сплав прошел одинаковое превращение. В данном случае все сплавы прошли одинаковое превращение, все они будут иметь одинаковую конечную структуру.
- ДС сплавов, компоненты которых не растворимы друг в друге.
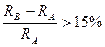
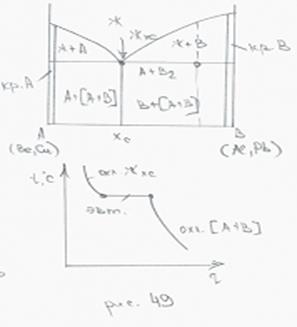
Фазы: ж, крист. А и В.
Структурный анализ.
ХХс —> А+В
С = К+1-Ф = 2+1-3 = 0, эвтектическая (безвариантная), [А+В] – эвтектика.
Все сплавы будут содержать эвтектику, фазовых структур будет видно 3, а фаз – 2.
- ДС сплавов, компоненты которых обладают ограниченной переменной растворимостью.
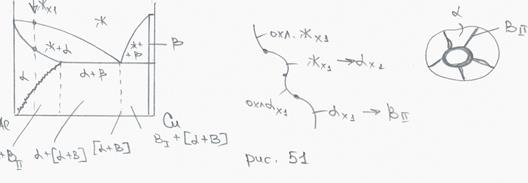
Фазы: ж, В, α-твердый р-р, А(В).
- ДС сплавов, компоненты которых имеют полиморфное превращение (меняется кристаллическая решетка).
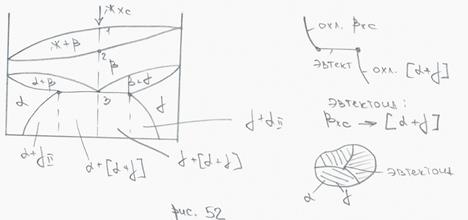
Фазы: ж, α, β, γ – твердые растворы.
§3. Значение диаграммы состояний
1) по диаграмме состояний для любого сплава можно установить все превращения. Конечную структуру, получить представление о его механических свойствах;
2) по ДС можно предсказать характер изменения физических свойств;
3) по ДС можно определить технологические свойства сплавов, легче деформируется диаграмма (1), чем (2) – см. предыдущий параграф ;
4) лучшие литейные качества имеет эвтектический сплав;
5) по ДС для любого сплава можно указать какую термическую обработку, с какой целью для него можно применить. Любой сплав при нагреве может оказаться всего в 3-х ситуациях:
- нет никаких превращений вплоть до начала плавления – (1) и (2);
- сплав при нагреве проходит через линию переменной растворимости (3);
- изменяется тип кристаллической решетки при нагреве сплава (4).
Дата добавления: 2015-04-25; просмотров: 1513;
