Горение газов
Горение газовых смесей протекает весьма различно в зависимости от условий опыта. Когда горение идет при постоянном давлении, наблюдается равномерное распространение пламени с постоянной скоростью.
Рассмотрим влияние некоторых факторов на скорость распространения пламени (W).
Скорость W существенно зависит от концентрации компонентов газовой смеси. Характер зависимости представлен на рисунке.
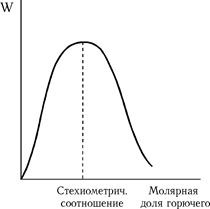
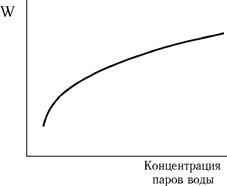
На горение некоторых газовых смесей существенно влияет присутствие паров воды даже в небольших количествах (каталитическое действие при горении СО; на горении метановых смесей практически не сказывается). Характер зависимости скорости распространения пламени представлен на рисунке.
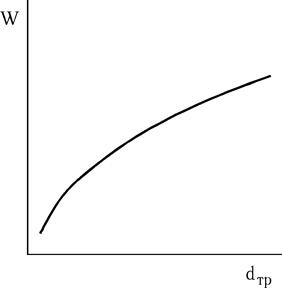
Скорость распространения пламени существенно зависит от диаметра трубки (уменьшаются теплопотери и происходит искривление фронта пламени).
Пусть в трубке площадью поперечного сечения s распространяется пламя со скоростью v. Объем смеси, сгорающей за единицу времени
V = vs.
С другой стороны, в каждой точке поверхности фронта пламя распространяется по нормали к этой поверхности со скоростью W. Если поверхность искривленного фронта пламени обозначить через S, то тот же самый объем смеси
V = WS.
Следовательно:
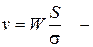 закон площадей.
закон площадей.
Если химическая реакция горения не является автокаталитической (цепной), то причиной распространения пламени может быть только передача тепла от продуктов горения несгоревшей смеси. Такой вид распространения пламени называется тепловым.
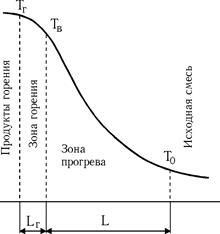
Распределение температур в горящей газовой смеси имеет вид, представленный на рисунке. Зоны прогрева и горения весьма узкие, причем всегда Lг < L. Эти зоны для газовых смесей составляют доли миллиметра. Причем, чем с большей скоростью распространяется пламя, тем уже зоны.
Скорость распространения пламени может быть определена по формуле:
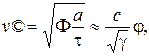
где F < 1 – коэффициент, зависящий от кинетики реакции и температур T0 и Tг;
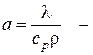 коэффициент температуропроводности смеси;
коэффициент температуропроводности смеси;
l – коэффициент теплопроводности;
t – время химической реакции;
с – скорость звука в зоне горения;
g – среднее число столкновений, необходимое для элементарного акта химической реакции;
j < 1 – безразмерный множитель.
Как видите, практически пользоваться этой формулой весьма затруднительно, но приведена она здесь с другой целью: из нее видно, что скорость распространения пламени при горении всегда меньше, причем во много раз, скорости звука. Это объясняется тем, что скорость передачи энергии в газе путем теплопроводности во много раз меньше скорости распространения упругих колебаний.
Согласно теории горения Зельдовича – Франк-Каменецкого скорость распространения пламени:
– в случае реакции первого порядка (мономолекулярной реакции)
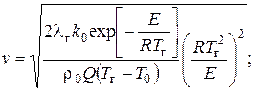
– в случае реакции второго порядка (бимолекулярной реакции)
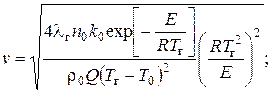
Здесь n0 – концентрация реагирующего вещества в г/см3;
lг – коэффициент теплопроводности газа при Tг;
k0 – предэкспоненциальный множитель;
r0 – плотность газа;
Q – объемная теплотворная способность смеси.
При этом влияние давления на скорость распространения пламени следующее:
– для мономолекулярных реакций v пропорциональна 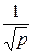 ;
;
– для бимолекулярных реакций v не зависит от p.
Дата добавления: 2015-03-03; просмотров: 1477;
