ЛАБОРАТОРНА РОБОТА № 3
5.2. Визначення ацетофенону або бензофенону методом постійно-струмової полярографії
Об’єктами полярографічного аналізу можуть бути не лише неорганічні речовини, але й багато з органічних речовин, які здатні до електрохімічних перетворень. В електродній реакції відновлення органічної речовини переважно беруть участь йони водню.
R + nH+ + ne– ® RHn (13)
Саме тому аналіз проводять в буферних розчинах з достатньо великою буферною ємкістю.
До полярографічно активних фраґментів органічних речовин належать, наприклад, альдегідна, кетонна, азо-, нітро-, пероксигрупи та багато інших, які в умовах полярографічного аналізу легко відновлюються в межах зміни потенціалу РКЕ від 0 до –2,7 В і можуть бути визначені.
Органічні речовини, які електрохімічно окиснюються важче від ртуті, тобто при потенціалах, більших +0,4 В, можуть бути визначені з застосуванням платинового електрода. Так аналізують органічні кислоти (малеїнову, фумарову) та деякі ефіри.
Оскільки багато з органічних речовин нерозчинні або погано розчинні у воді, то для підвищення їх розчинності до води додають органічні розчинники, наприклад, метанол, етанол, діоксан, оцтову кислоту, диметилформамід, гліколь, моногліколеві ефіри і т.п.
Механізм відновлення кетонів, у тому числі ацетофенону та бензофенону, значною мірою залежить від рН середовища. При рН = 5 відновлення проходить в дві стадії.
1-ша стадія відповідає відновленню протоґенованої карбонільної групи
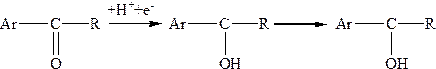
2-га стадія — відновленню кетильного радикала до карбінолу
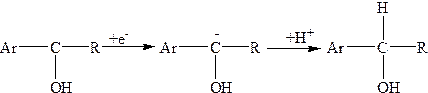
Обом стадіям на вольтамперній кривій відповідають хвилі при різних значеннях потенціалу. При рН > 5 відновлення йде також через дві стадії, одначе процеси протікають значно швидше, і на полярограмах фіксується одно-, двоелектронна хвиля відновлення кетону до карбінолу.
Метою роботи є кількісне визначення ацетофенону або бензофенону в розчині методом калібрувального графіка.
Реактиви, посуд та прилади
1. Вихідний стандартний 4∙10–3 М розчин ацетофенону (або бензофенону).
2. Фоновий електроліт — розчин, що містить 1 М NH4OH i 1 M NH4Cl в 50%-му етанолі.
3. Сульфіт натрію кристалічний (для зв’язування розчиненого кисню).
4. Бюретки на 25 мл — 2 шт.
5. Стаканчик місткістю 50–70 мл, що служить електролізером.
6. Електроди НКЕ та РКЕ.
7. Електролітичний місток, заповнений насиченим розчином KCl і загущений аґар-аґаром.
8. Полярограф.
Дата добавления: 2015-02-28; просмотров: 736;
