Вопрос 37: Принцип Паули.
Принцип Паули в простейшей формулировке: в одном и том же атоме не может быть более одного электрона с одинаковым набором четырех квантовых чисел п, l, ml и тs, т. е. Z(п, l, ml, тs) = 0 или 1, где Z(п, l, ml, тs) – число электронов, находящихся в квантовом состоянии, описываемом набором четырех квантовых чисел: п, l, ml, ms. Таким образом, принцип Паули утверждает, что два электрона, связанные в одном и том же атоме, различаются значениями по крайней мере одного квантового числа.
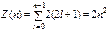 .
.
Совокупность электронов в многоэлектронном атоме, имеющих одно и то же главное квантовое число п, называют электронной оболочкой. В каждой из оболочек электроны подразделяются по подоболочкам, соответствующим данному значению l. Поскольку орбитальное квантовое число принимает значения от 0 до n - 1, число подоболочек равно порядковому номеру п оболочки. Количество электронов в подоболочке определяется магнитным и магнитным спиновым квантовыми числами: максимальное число электронов в подоболочке с данным l равно 2(2l+1). Системы фермионов встречаются в природе только в состояниях, описываемых антисимметричными волновыми функциями (квантово-механическая формулировка принципа Паули). Так как принцип Паули лежит в основе систематики заполнения электронных состояний в атомах, то он позволяет объяснить Периодическую систему элементов Д. И. Менделеева (1869) – фундаментальный закон природы – основу современной химии, атомной и ядерной физики. Учитывая, как это делается в современной теории, что порядковый номер Z химического элемента равен общему числу электронов в атоме данного элемента, каждый последующий элемент можно «образовать» из предыдущего прибавлением к ядру одного протона (соответственно прибавлением одного электрона в электронной оболочке атома) с возрастанием числа электронов каждый следующий электрон занимает возможное энергетическое состояние с наименьшей энергией, заполнение электронами энергетических состояний происходит в соответствии с принципом Паули. Совершим «небольшую экскурсию» по Периодической системе, рассмотрев элемент за элементом. Единственный электрон атома водорода находится в состоянии 1s, характеризуемом квантовыми числами 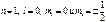 (ориентация его спина произвольна). Оба электрона атома Не находятся в состоянии 1s, но с антипараллельной ориентацией спина. Электронная конфигурация для атома Не записывается как 1s2 (два 1s-электрона). На атоме Не заканчивается заполнение К-оболочки, что соответствует завершению I периода Периодической системы элементов Менделеева. Третий электрон атома Li (Z=3), согласно принципу Паули, уже не может разместиться в целиком заполненной K-оболочке и занимает наинизшее энергетическое состояние с n = 2 (L-оболочка), т. е. 2s-состояние. Электронная конфигурация для атома Li 1s2 2s. Атомом Li начинается II период Периодической системы элементов. Четвертым электроном Be (Z=4) заканчивается заполнение подоболочки 2s. У следующих шести элементов от В (Z=5) до Ne (Z= 10) идет заполнение подоболочки 2р (табл. 2). II период Периодической системы заканчивается неоном – инертным газом, для которого подоболочка 2р целиком заполнена.
(ориентация его спина произвольна). Оба электрона атома Не находятся в состоянии 1s, но с антипараллельной ориентацией спина. Электронная конфигурация для атома Не записывается как 1s2 (два 1s-электрона). На атоме Не заканчивается заполнение К-оболочки, что соответствует завершению I периода Периодической системы элементов Менделеева. Третий электрон атома Li (Z=3), согласно принципу Паули, уже не может разместиться в целиком заполненной K-оболочке и занимает наинизшее энергетическое состояние с n = 2 (L-оболочка), т. е. 2s-состояние. Электронная конфигурация для атома Li 1s2 2s. Атомом Li начинается II период Периодической системы элементов. Четвертым электроном Be (Z=4) заканчивается заполнение подоболочки 2s. У следующих шести элементов от В (Z=5) до Ne (Z= 10) идет заполнение подоболочки 2р (табл. 2). II период Периодической системы заканчивается неоном – инертным газом, для которого подоболочка 2р целиком заполнена.
Дата добавления: 2015-02-25; просмотров: 1234;
