Билет 10
1. Осмоти́чний ти́ск (або дифу́зний ти́ск) — термодинамічний параметр, що характеризує прагнення розчину понизити свою концентрацію при зіткненні з чистим розчинником внаслідок зустрічної дифузії молекулрозчинника та розчиненої речовини.
Для дуже розбавлених розчинів недисоціюючих речовин знайдена закономірність, що досить точно описується рівнянням:
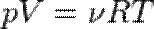
де 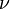 — число молей речовини в розчині об'єму V; R — універсальна газова стала; Т — абсолютна температура (в Кельвінах), p — величина осмотичного тиску.
— число молей речовини в розчині об'єму V; R — універсальна газова стала; Т — абсолютна температура (в Кельвінах), p — величина осмотичного тиску.
P = CRT,
де P — осмотичний тиск, Па; С — концентрація розчиненої речовини моль/л (молярна концентрація може бути замінена на моляльну — моль/кг); R — газова стала; T — температура, °К.
Для розчинів електролітів осмотичний тиск більше розрахованого в і разів. У зв’язку з цим для розчинів електролітів закон Вант-Гоффа має таке значення:
P = і CRT,
де і — ізотонічний коефіцієнт (і>1), який показує, у скільки разів збільшується кількість часток при дисоціації порівняно з недисоційованою речовиною.
Осмотичний тиск має велике значення для життєдіяльності рослин і тварин, оскільки тканини їхніх клітин – це ті самі напівпроникні перегородки рослинного або тваринного походження, а клітини наповнені водними розчинами різних речовин. Осмотичний тиск клітинного соку дорівнює 0,4–2,0 МПа. Якщо клітини рослини занурити у воду (або поливати рослину водою), то вода проникає в клітини, створюючи в них гідростатичний тиск, внаслідок чого рослина стає міцною і пружною (явище тургору). Навпаки, якщо занурити клітину в розчин, концентрація розчинених речовин в якому більша, ніж у клітині, то вода з останньої переходить у зовнішній розчин, а клітина зморщується (явище плазмолізу).
Дата добавления: 2015-01-13; просмотров: 1808;
