Термодинамическая система.
Техническая термодинамика (т/д) рассматривает закономерности взаимного превращения теплоты в работу. Она устанавливает взаимосвязь между тепловыми, механическими и химическими процессами, которые совершаются в тепловых и холодильных машинах, изучает процессы, происходящие в газах и парах, а также свойства этих тел при различных физических условиях.
Термодинамика базируется на двух основных законах (началах) термодинамики:
I закон термодинамики - закон превращения и сохранения энергии;
II закон термодинамики – устанавливает условия протекания и направленность макроскопических процессов в системах, состоящих из большого количества частиц.
Техническая т/д, применяя основные законы к процессам превращения теплоты в механическую работу и обратно, дает возможность разрабатывать теории тепловых двигателей, исследовать процессы, протекающие в них и т.п.
Объектом исследования является термодинамическая система, которой могут быть группа тел, тело или часть тела. То что находится вне системы называется окружающей средой. Т/д система это совокупность макроскопических тел, обменивающиеся энергией друг с другом и окружающей средой. Например: т/д система – газ, находящейся в цилиндре с поршнем, а окружающая среда – цилиндр, поршень, воздух, стены помещения.
Изолированная система - т/д система не взаимодействующая с окружающей средой.
Адиабатная (теплоизолированная) система – система имеет адиабатную оболочку, которая исключает обмен теплотой (теплообмен) с окружающей средой.
Однородная система – система, имеющая во всех своих частях одинаковый состав и физические свойства.
Гомогенная система – однородная система по составу и физическому строению, внутри которой нет поверхностей раздела (лед, вода, газы).
Гетерогенная система – система, состоящая из нескольких гомогенных частей (фаз) с различными физическими свойствами, отделенных одна от другой видимыми поверхностями раздела (лед и вода, вода и пар).
В тепловых машинах (двигателях) механическая работа совершается с помощью рабочих тел – газ, пар.
Свойства каждой системы характеризуются рядом величин, которые принято называть термодинамическими параметрами. Рассмотрим некоторые из них, используя при этом известные из курса физики молекулярно-кинетические представления об идеальном газе как о совокупности молекул, которые имеют исчезающе малые размеры, находятся в беспорядочном тепловом движении и взаимодействуют друг с другом лишь при соударениях.
Давление обусловлено взаимодействием молекул рабочего тела с поверхностью и численно равно силе, действующей на единицу площади поверхности тела по нормали к последней. В соответствии с молекулярно-кинетической теорией давление газа определяется соотношением
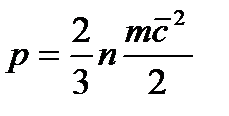 , (1.1)
, (1.1)
Где n — число молекул в единице объема;
т — масса молекулы; с2— средняя квадратическая скорость поступательного движения молекул.
В Международной системе единиц (СИ) давление выражается в паскалях (1 Па=1 Н/м2). Поскольку эта единица мала, удобнее использовать 1 кПа = 1000 Па и 1 МПа=106 Па.
Давление измеряется при помощи манометров, барометров и вакуумметров.
Жидкостные и пружинные манометры измеряют избыточное давление, представляющее собой разность между полным или абсолютным давлением р измеряемой среды и атмосферным давлением
pатм, т.е. 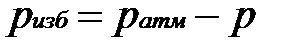
Приборы для измерения давлений ниже атмосферного называются вакуумметрами; их показания дают значение разрежения (или вакуума):
 ,
,
т. е. избыток атмосферного давления над абсолютным.
Следует отметить, что параметром состояния является абсолютное давление. Именно оно входит в термодинамические уравнения.
Температурой называется физическая величина, характеризующая степень нагретости тела. Понятие о температуре вытекает из следующего утверждения: если две системы находятся в тепловом контакте, то в случае неравенства их температур они будут обмениваться теплотой друг с другом, если же их температуры равны, то теплообмена не будет.
С точки зрения молекулярно-кинетических представлений температура есть мера интенсивности теплового движения молекул. Ее численное значение связано с величиной средней кинетической энергии молекул вещества:
 , (1.2)
, (1.2)
где k — постоянная Больцмана, равная 1,380662•10ˉ23 Дж/К. Температура T, определенная таким образом, называется абсолютной.
В системе СИ единицей температуры является кельвин (К); на практике широко применяется градус Цельсия (°С). Соотношение между абсолютной Т и стоградусной I температурами имеет вид
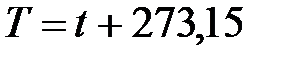 .
.
В промышленных и лабораторных условиях температуру измеряют с помощью жидкостных термометров, пирометров, термопар и других приборов.
Удельный объем v — это объем единицы массы вещества. Если однородное тело массой М занимает объем v, то по определению
v= V/М.
В системе СИ единица удельного объема 1 м3/кг. Между удельным объемом вещества и его плотность существует очевидное соотношение:
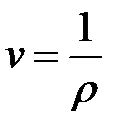
Для сравнения величин, характеризующих системы в одинаковых состояниях вводится понятие «нормальные физические условия»:
p=760 мм рт.ст.= 101,325 кПа; T=273,15 K.
В разных отраслях техники и разных странах вводят свои, несколько отличные от приведенных «нормальные условия», например, «технические» (p= 735,6 мм рт.ст.= 98 кПа, t=15˚C) или нормальные условия для оценки производительности компрессоров (p=101,325 кПа, t=20˚С ) и т. д.
Если все термодинамические параметры постоянны во времени и одинаковы во всех точках системы, то такое состояние системы называется равновесным.
Если между различными точками в системе существуют разности температур, давлений и других параметров, то она является неравновесной. В такой системе под действием градиентов параметров возникают потоки теплоты, вещества и другие, стремящиеся вернуть ее в состояние равновесия. Опыт показывает, что изолированная система с течением времени всегда приходит в состояние равновесия и никогда самопроизвольно выйти из него не может. В классической термодинамике рассматриваются только равновесные системы.
Уравнение состояния.Для равновесной термодинамической системы существует функциональная связь между параметрами состояния, которая называется уравнением состояния. Опыт показывает, что удельный объем, температура и давление простейших систем, которыми являются газы, пары или жидкости, связаны термическим уравнением состояние вида:
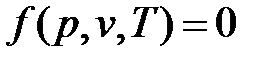 .
.
Уравнению состояния можно придать другую форму:
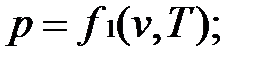
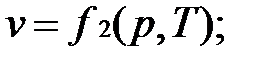
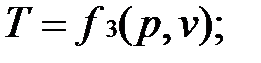
Эти уравнения показывают, что из трех основных параметров, определяющих состояние системы, независимыми являются два любых.
Для решения задач методами термодинамики совершенно необходимо знать уравнение состояния. Однако оно не может быть получено в рамках термодинамики и должно быть найдено либо экспериментально, либо методами статистической физики. Конкретный вид уравнения состояния зависит от индивидуальных свойств вещества.
Дата добавления: 2015-02-16; просмотров: 1233;
