Лейкоцитарна формула, її вікові та патологічні зміни
Процентне співідношення різних форм лейкоцитів у периферичнійкрові називають лейкоцитарною формулою. її прийнято зображати в певній стандартній формі.
| Вид лейкоцита | Нейтрофіли | Еозино філи | Базофіли | Лімфоцити | Моноцити | ||
| юні | п-ядер. | сегм.яд. | |||||
| Процент | 0-1 | 1-5 | 45-70 | 1-5 | 0,5-1 | 20-40 | 2-10 |
Збільшення кількості юних та паличкоядерних форм нейтрофілів .називають зсувом вліво.
Лейкоцитарна формула має виражені вікові особливості. Так, дитина народжується із співвідношенням нейтрофілів та лімфоцитів, характерним для дорослої людини. Але уже в перші дні у неї починає наростати процент лімфоцитів і зменшуватися процент нейтрофілів. їх кількість зрівнюється на 5-6 добу життя. Це вирівнювання називають першим перехрестом лейкоцитарної формули. Кількість лімфоцитів наростає до 5 року життя і перевищує відносний вміст нейтрофілів. Але потім поступово починається зворотний процес і у 5-6 років процент нейтрофілів та лімфоцитів знову вирівнюється. Цей стан називають другим перехрестом лейкоцитарної формули.
Суттєво змінюється лейкоцитарна формула і при деяких патологічних станах. Так, гострі бактеріальні інфекції, як правило, супроводжуються нейтрофільним лейкоцитозом і зниженням числа еозинофілів та лімфоцитів. Поява моноцитозу свідчить про перемогу організму над патогенними мікроорганізмами. Хронічні інфекції характеризуються лімфоцитозом. Зсув лейкоцитарної формули вліво (тобто в сторону збільшення проценту юних форм нейтрофілів) часто зустрічається при лейкозах - пухлинних захворюваннях кровотворних органів. При аутоімунних захворюваннях станах та глистяних інвазіях спостерігається еозінофілія. Алергія, як правило, супроводжується збільшенням проценту базофілів.
Механізми захисту клітинного гомеостазу організму
В процесі життєдіяльності організму у внутрішнє середовище можуть попасти чужерідні мікроорганізми та макромолекули, які порушують цілісність його клітин. Ці мікроорганізми та молекули є носіями чужої генетичної інформації і загрожують індивідуальності організму. Внаслідок мутацій під впливом різних факторів (вірусів, мікроорганізмів, радіації) генетично чужерідними стають і власні клітини організму. В організмі функціонує спеціальна система, яка ідентифікує такі генетично чужерідні клітини та макромолекули і знищує їх. Ця система називається імунною, її складовими компонентами є кістковий мозок, тімус, лімфовузли та лім-фоїдні утворення шлунка і кишечника, а також лімфоїдна тканина внутрішніх органів та лейкоцити в крові і тканинах. Імунна система забезпечує два типи захисних механізмів: неспецифічні - спрямовані проти всіх чужерідних факторів незалежно від їх природи; та специфічні - спрямовані конкретно проти певного чужерідного фактора. Кожен із цих типів реалізується двома шляхами: шляхом клітинного та гуморального імунітету.
Клітинний імунітет пов'язаний із впливом на чужерідний фактор лейкоцитів, а гуморальний- розчинених в крові та міжклітинній рідині захисних речовин білкової природи та антитіл (імуноглобулінів). Поділ захисних механізмів на специфічні та неспецифічні умовний, тому що включення неспецифічних механізмів вимагає попереднього розпізнавання чужерідного фактора специфічними механізмами. Тобто обидва типи механізмів взаємодіють при реалізації імунної відповіді.
До неспецифічних механізмів клітинного імунітету відносяться запальна реакція і фагоцитоз, що реалізуються мікро- та макрофагами.
Гуморальні неспецифічні механізми представлені:
• білком лізоцимом, що міститься в слині, слізній рідині, крові, слизі дихальних шляхів та інших рідинах організму.
• системою комплементу - складається із 11 білків плазми, що позначаються буквами С 1-...11. В фізіологічних умовах ці білки знаходяться в неактивному стані, але можуть активуватися як безпосередньо чужерідним агентом, так і специфічними клітинними механізмами. Послідовна каскадна активація цих білків приводить до лізису мембран чужерідних клітин і їх загибелі.
• системою пропердіну - складається із трьох компонентів: білка пропердіну Р, фактора В -глікопротеїду та протеолітичного фермента. Ця система також реагує на чужерідні тіла і пошкоджує їх.
• лейкінами та бета-лізинами , що виділяються лейкоцитами;
• плакінами - секретуються тромбоцитами.
Специфічні клітинні механізми імунітету реалізуються Т-лімфоцитами та макрофагами. На протязі всього життя кістковий мозок поставляє в кров, а звідти в тимус невеликі кількості попередників Т-лімфо-цитів. В тимусі Т-лімфоцити набувають поверхневих рецепторів до різних антигенів і виходять в кров, мігруючи у вторинні лімфоїдні органи. Якщо в ці органи попадає антиген, то ті лімфоцити, які мають рецептори до цього антигена, інтенсивно проліферують і диференціюються в ефекторні Т-лімфоцити. Т-лімфоцити складають 60-80% всіх лімфоцитів. Приблизно 10% цієї кількості циркулює в крові дуже тривалий час (до 10 років), не ділячись. Це клітини імунної пам'яті. Якщо антиген поступає в кров, то він активує ці клітини, а вони вже стимулюють проліферацію ефекторних Т-лімфоцитів, що знищують антиген.
Серед ефекторних Т-лімфоцитів розрізняють слідуючі класи:
• Т-хелпери - стимулюють диференціювання В-лімфоцитів;
• Т- кіллери - здійснюють цитотоксичну дію на чужерідні агенти;
• Т-ампліфаєри - підсилюють проліферацію Т-кіллерів;
• Т- супресори - пригнічують імунну відповідь на певний антиген.
Специфічний гуморальний імунітет забезпечують В-лімфоцити, які також утворюються в кістковому мозку, але диференціювання проходять у лімфатичних вузлах, селезінці, пеєрових бляшках кишечника. На їх поверхні утворюються рецептори антигенів у вигляді імуноглобулінів М. Частина В-лімфоцитів тривало циркулює в крові, забезпечуючи імунну пам'ять, а більша частина перетворюється в плазматичні клітини, які секретують антитіла.
Кооперація імунокомпетентних клітин в імунній відповіді
Перше попадання антигену в організм через деякий латентний період викликає проліферацію лімфоцитів імунної пам'яті і утворення невеликої кількості ефекторних Т-лімфоцитів та антитіл. Цю реакцію імунної системи називають первинною імунною відповіддю. Вона розвивається, як правило, на протязі 3-4 тижнів. При повторному поступанні цього антигена швидко без будь-якого латентного періоду в крові створюється висока концентрація антитіл до нього та суттєво збільшується кількість ефекторних Т-лімфоцитів, специфічно чутливих до цього антигена. Така реакція називається вторинною імунною відповіддю і підтримується на протязі тривалого часу: місяці і навіть роки.
Реалізація імунної відповіді вимагає кооперації різних імунокомпетентних клітин. Так, поява антигена у внутрішньому середовищі приводить до його фагоцитування макрофагами. Антигенні детермінанти після лізису антигена транспортуються на поверхню макрофага. Першими на ці детермінанти реагують Т-лімфоцити імунної пам'яті, які активуються і секретують біологічно активну речовину інтерлейкін-2. Ця речовина стимулює проліферацію ефекторних Т-лімфоцитів. Т-хелпери, які при цьому утворюються, взаємодіючи із макрофагами, впливають на проліферацію В-лімфоцитів. Ці в свою чергу диференціюються у плазматичні клітини і починають інтенсивно продукувати антитіла.
Згортальна та протизгортальна система крові
Тромбоцити крові та їх функції
Кількість тромбоцитів у периферичній крові складає 200-400х109/л. Тромбоцити мають форму пластинок. їх розміри: діаметр - близько 1,5-4 мкм; товщина 0,5-0,75 мкм. Ці формені елементи подібно до еритроцитів не є справжніми клітинами, вони не мають ядра і більшості субклітинних структур. Утворюються в кістковому мозку із мегакаріоцитів шляхом відщеплення від них фрагментів цитоплазми. В крові циркулюють 5-11 днів, після чого руйнуються в печінці, легенях та селезінці.
Функції тромбоцитів досить різноманітні. Основна з них - участь в системі гемостазу. На мембрані тромбоцита, у його внутрішніх гранулах міститься значна кількість біологічно активних сполук, які вважаються тромбоцитарними факторами згортання крові. Велике значення для гемостазу має здатність тромбоцитів безперервно змінювати розмір та форму, утворюючи багаточисленні відростки псевдоподії), якими тромбоцит фіксується до пошкодженої поверхні судин. Ця здатність зумовлена наявністю в тромбоциті скоротливих білків типу актоміозинового комплексу.
Тромбоцити виконують також захисну функцію завдяки їх здатності о фагоцитозу бактеріальних тіл, вірусів та імунних комплексів.
На поверхні тромбоцитів транспортуються різноманітні БАР.
Загальна характеристика механізмів зупинки кровотечі
Механізми зупинки кровотечі (гемостаз) ділять на первинний (судинно-тромбоцитарний) гемостаз та вторинний (коагуляційний). Первинний гемостаз реалізується на протязі декількох перших хвилин після початку кровотечі. Проте він здатний зупинити кровотечу тільки із невеликих судин. У більшості випадків він лише дає поштовх до розгортання каскадного механізму коагуляційного гемостазу.
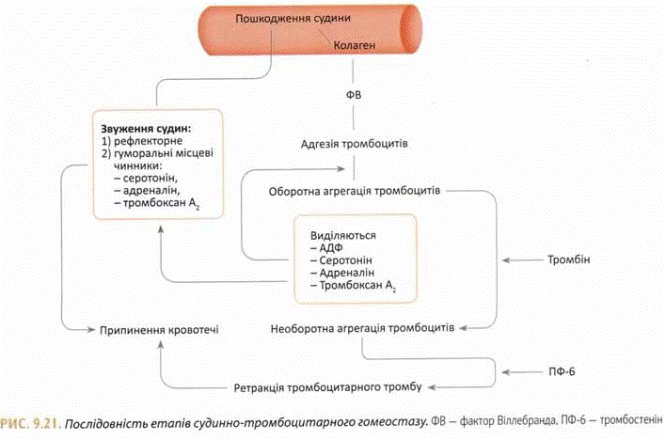
Первинний гемостаз включає:
• рефлекторний спазм, судин одразу після їх пошкодження. Цей спазм підтримується вазоактивними речовинами, які виділяються із тромбоцитів при їх пошкодженні. Це - серотонін, адреналін, тромбоксан;
• адгезію тромбоцитів - приклеювання до місця ушкодження судини, яке досягається завдяки реакції колагенових ниток із негативно зарядженими тромбоцитами. При цьому тромбоцити утворюють псевдоподії, якими і фіксуються до стінок судини:
• зворотну агрегацію тромбоцитів - склеювання тромбоцитів одного із одним і формування так званого «білого тромба», що прикриває ушкоджену ділянку судинної стінки.
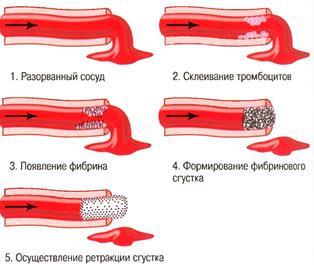
Коагуляційний гемостаз полягає у переході розчиненого в плазмі білка фібриногену у нерозчинний білок фібрин, що утворює густу сітку, у якій накопичуються формені елементи крові. Таким способом формується «червоний тром», який надійно прикриває ушкоджене місце судини і запобігає виходу крові у тканини.
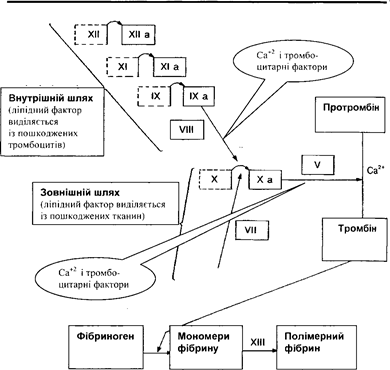
Процес коагуляції починається із утворення протромбіназного комплексу (тромбопластину) внаслідок послідовно діючих ферментативних процесів. Він утворюється при взаємодії ліпідного фактору із плазмен-ними факторами згортання. В залежності від походження ліпідного фактору розрізняють зовнішній та внутрішній шляхи згортання крові.
При зовнішньому шляху утворення протромбінази активуючий ліпідний фактор виділяється із пошкоджених клітин судин та тканин, а при внутрішньому — із тромбоцитів.
Подальші реакції є спільні для обох шляхів коагуляції крові. Під дією тромбопластину в присутності іонів кальцію, плазменний білок протромбін перетворюється в тромбін, а останній ініціює перетворення фібриногену в фібрин.
Фактори згортання крові
В плазмі крові у вільному стані знаходиться ряд БАР, які забезпечують процес згортання крові, їх називають плазменними факторами згортання і згідно міжнародної номенкатури позначають цифрами римського алфавіту. Ці цифри відображають хронологію відкриття факторів. Більшість факторів знаходяться в неактивному стані. Для позначення їх активного стану добавляють маленьку букву "а". Крім цифр назва фактора відображає його хімічну структуру, участь у механізмі гемостазу або ж прізвище хворого, в крові якого був виявлений даний фактор.
Так, на сьогоднішній день відомо 12 плазменних факторів (VI фактор - відсутній)
 І - фібриноген;
І - фібриноген;
 II - протромбін;
II - протромбін;
 III - тканинний тромбопластин
III - тканинний тромбопластин
 IV - іони кальцію;
IV - іони кальцію;
 V - проакцелерин;
V - проакцелерин;
 VII - проконвернтін;
VII - проконвернтін;
 VIII - антигемофільний глобулін;
VIII - антигемофільний глобулін;
 IX - Фактор Крістмаса, антигемофільний фактор В;
IX - Фактор Крістмаса, антигемофільний фактор В;
 X - фактор Стюарта-Прауера, протромбіназа;
X - фактор Стюарта-Прауера, протромбіназа;
 XI - плазменний попередник тромбопластину:
XI - плазменний попередник тромбопластину:
 XII - фактор Хагемана, контактний фактор;
XII - фактор Хагемана, контактний фактор;
 XIII - фібринстабілізуючий фактор, фібриназа.
XIII - фібринстабілізуючий фактор, фібриназа.
Усі ці фактори можна розділити на дві групи: попередники ферментів (II, VII, IX, X, XI, XII) та неферменти (І, IV, V, VIII).
На мембрані і всередині тромбоцитів містяться клітинні фактори згортання, які позначаються арабськими цифрами. Найбільше значення мають фактор 3 - фософоліпіди мембран тромбоцитів; 4-й фактор - зв'язує гепарин; 5-й фактор - фібриноген; 6-й - тромбостенін; 10-й - серотонін; 11-й - фактор агрегації.
Коагуляційний гемостаз
Зовнішній шлях починається із активації VII ф, ліпідним фактором, який виділяється із мембран ушкоджених тканин та стінок судин. Цей фактор активує XII ф. Хагемана і разом із іонами кальцію, та ф. V утворює комплекс, який і є тканинною протромбіназою.
Внутрішній щлях починається із контакту коллагену із тромбоцитами. При цьому активується ф. XII Хагемана і утворює комплекс із XI фактором. Ця реакція триває декілька хвилин. Після чого протікають швидкі каскадні процеси формування комплексу, що складається із ф. ІХа, VIII, тромбоцитарного фактору 3 та іонів Са+2. Цей комплекс активує ф.Х, який разом із фосфоліпідами, що виділяються тромбоцитом, утворює кров'яну протромбіназу.
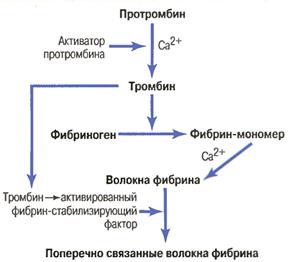
Наступний етап - утворення тромбіну є спільним для внутрішнього та зовнішнього шляху коагуляційного гемостазу. Протромбіназа має протеолітичну дію по відношенню до білка протромбіну із фракції альфа-2-гло-булінів. В присутності іонів кальцію під впливом протромбінази він перетворюється в тромбін. Для утворення протромбіну в печінці потрібен вітамін К. Тому його недостатність (наприклад при порушенні всмоктування в кишечнику) приводить до порушень гемостазу.
Тромбін є пептидазою, яка ефективно розщеплює пептидні зв'язки в молекулі фібриногену. Мономери фібрину після цього утворюють гель, який в присутності іонів кальцію та ф.ХШ перетворюється в сітчасту структуру, в якій заплутуються формені елементи крові, переважно еритроцити.
Останнім етапом коагуляційного гемостазу є ретракція згустка, що утворився, в ході якої він стискується, втрачає сироватку і стає більш компактним. Цей процес відбувається під впливом тромбоцитарного фактору тромбостеніну, що виділяється при руйнуванні еритроцитів.
Розчинення кров'яного згустку такий же ланцюговий ферментативний процес, як і його утворення. В даний час вважається, що в крові постійно протікають, як процеси утворення невеликих кількостей фібрину так і процеси фібринолізу. В нормі вони зрівноважені. І лише в тому ви падку, коли коагуляційна система додатково стимулюється продуктами пошкодження судин і тромбоцитів, коагуляція починає переважати над фібринолізом.
Суть фібринолізу полягає в тому, що один із білків плазми із фракціі глобулінів - плазміноген - під впливом його активаторів - фібринокінш (кров'яних і тканинних) перетворюється в активну форму плазмін. Плазмін є протеолітичним ферментом, який гідролізує фібрин і розчиняє згусток. Крім того, він пригнічує плазменні фактори згортання (V, VIII, ХІІ, протромбін). Плазмін залишається активним тільки декілька секунд і швидко інактивується білком плазми антиплазміном.
Найважливішими тканинними активаторами плазміногену є тканинні фібринокінази, особливо багато їх в м'язовому шарі матки. Кров'яні фібринокінази звільняються із тромбоцитів пошкоджених клітин крові в присутності лізокіназ, що виділяються із клітин крові при запальних процесах. Так, при лікуванні тромбозів застосовують екзогенну лізокіназу -стрептокіназу, яку продукує мікроб - гемолітичний стрептокок.
До фізіологічних антикоагулянтів, які підтримують кров в рідкому стані відноситься антитромбін ІІІ(білок із фракції альфа-2-глобулінів, гепарин, нитки фібрину, які адсорбують на собі плазменні фактори згортання крові.
Мал.75. Основні етапи коагуляційного гемостазу
Фібриноліз та його механізми. Порушення згортання крові
Оскільки тромбоцити приймають участь у багатьох етапах згортання крові, то зменшення кількості тромбоцитів в крові або тромбоцитопенія, супроводжується порушеннями гемостазу. Так, при зменшенні кількості тромбоцитів крові до 50x109/л у всіх органах виникають крапкові капілярні кровотечі, збільшується час кровотечі, сповільнюється ретракція згустку.
Згортання крові порушується і при запальних та дегенеративних захворюваннях печінки (гепатит, цироз) в результаті пригнічення синтезу протромбіну та ф.УІІ, IX, X.
Порушення згортання відбувається також при дефіциті в організмі вітаміну К, який в нормі поступає з їжею та утворюється мікрофлорою кишечника. Оскільки цей вітамін є жиророзчинним, то він всмоктується з кишечника тільки в присутності жовчі. Патологія жовчоутворення та жовчовиділення також приводить до його дефіциту.
До спадкових порушень гемостазу належить хвороба гемофілія, яка передається рецесивно у зв'язку із статтю. Хворіють мужчини, а носіями є жінки. Є декілька форм цієї хвороби, кожна із яких зв'язана із відсутністю деякого плазменного фактора. Так, найбільш вираженою є гемофілія, причиною якої є відсутність ф.УІІІ. Клінічно легше протікають гемофілії, викликані недостатністю IX та XI фактора.
Порушення згортання у вигляді гіперкоагуляції спостерігається при стресі. Так, час зсідання крові при вираженому стресі зменшується із 5-10 хв. до 3-4 хв. В основі цього лежить вплив на систему гемостазу катехоламі-нів. Так, адреналін стимулює виділення із стінок судин факторів, що сприяють утворенню тканинної протромбінази. У високій концентрації адреналін безпосередньо активує ф. Хагемана. Протромбіназну активність мають також жирні кислоти, які з'являються в крові внаслідок катаболічної дії адреналіну. Гіперкоагуляція спостерігається також при тривалому збудженні симпатичної та парасимпатичної нервової системи.
Плазміни, або фібринолізини — це чинники, які руйнують фібрин, що утворився при коагуляційному гемостазі.
Фібринолітична система складається із неактивної форми ферментів — плазміногенів, що синтезуються у печінці, частково у нирках та еозинофілах, які під впливом активаторів переходять в активний стан — плазміни (фібринолізини): протеолітичні ферменти, що гідролізують фібрин.

Антикоагулянти — це чинники, які протидіють або блокують розвиток коагуляційного гемостазу, а саме утворення червоного тромбу.
За механізмами дії більшість антикоагулянтів є інгібіторами коагулянтів: вони зв'язуються з активним центром ферменту, блокують його і виключають з подальшого процесу коагуляції.
До головних інгібіторів факторів зсідання крові належать такі:
 Антитромбін III (АТ III)- основний інгібітор тромбіну, факторів X, IX. Він також інактивує фактори XI. XII. Синтезується у печінці. Його називають гєпариновим кофактором І, бо в присутності гепарину антитромбін III збільшує свою активність у тисячі разів.
Антитромбін III (АТ III)- основний інгібітор тромбіну, факторів X, IX. Він також інактивує фактори XI. XII. Синтезується у печінці. Його називають гєпариновим кофактором І, бо в присутності гепарину антитромбін III збільшує свою активність у тисячі разів.
 Гепарин - синтезується у печінці. Зв'язується з АТ III, завдяки чому прискорюється утворення комплексу "тромбін-АТ III - гепарин', який викликає інактивацію тромбіну. Після утворення комплексу гепарин дисоціює із нього і зв'язується з іншою молекулою АТ III, що призводить до багатьох циклів інактивації тромбіну. Гепариновий кофактор II (ГКII) - синтезується у печінці, циркулює у крові близько 2.5 діб є інгібітором лише тромбіну у присутності гепарину, але активність цього комплексу менша, ніж "АТ III -гепарин".
Гепарин - синтезується у печінці. Зв'язується з АТ III, завдяки чому прискорюється утворення комплексу "тромбін-АТ III - гепарин', який викликає інактивацію тромбіну. Після утворення комплексу гепарин дисоціює із нього і зв'язується з іншою молекулою АТ III, що призводить до багатьох циклів інактивації тромбіну. Гепариновий кофактор II (ГКII) - синтезується у печінці, циркулює у крові близько 2.5 діб є інгібітором лише тромбіну у присутності гепарину, але активність цього комплексу менша, ніж "АТ III -гепарин".
 Білок С (БС) - синтезується у печінці під впливом вітаміну К. Циркулює у крові в неактивній формі, зв'язується з поверхнею ендотелію за допомогою кальцієвих містків; активується тромбіном.
Білок С (БС) - синтезується у печінці під впливом вітаміну К. Циркулює у крові в неактивній формі, зв'язується з поверхнею ендотелію за допомогою кальцієвих містків; активується тромбіном.
 Білок 5 - синтезується у печінці та ендотеліальних клітинах під впливом вітаміну К. прискорює інактивацію як вільних, так і зв'язаних факторів VIII.
Білок 5 - синтезується у печінці та ендотеліальних клітинах під впливом вітаміну К. прискорює інактивацію як вільних, так і зв'язаних факторів VIII.
Нитки фібрину — відбирають на себе 90% тромбіну і виключають його з процесу зсідання крові.
Дата добавления: 2015-02-13; просмотров: 6662;
