МЕТОДИЧЕСКИЕ УКАЗАНИЯ. В соответствии с вариантом имеем следующие линейные модели:
В соответствии с вариантом имеем следующие линейные модели:
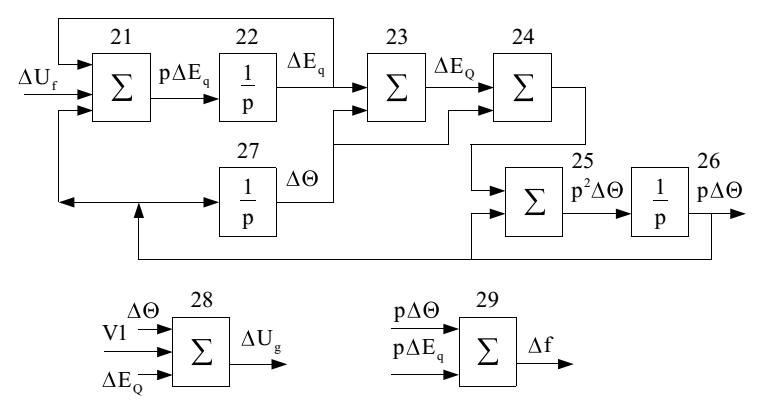
Рис. 5.4. Линейная модель синхронного генератора, оснащѐнного системой возбуждения
Графически отобразим нормальный режим на диаграмме рабочих режимов:
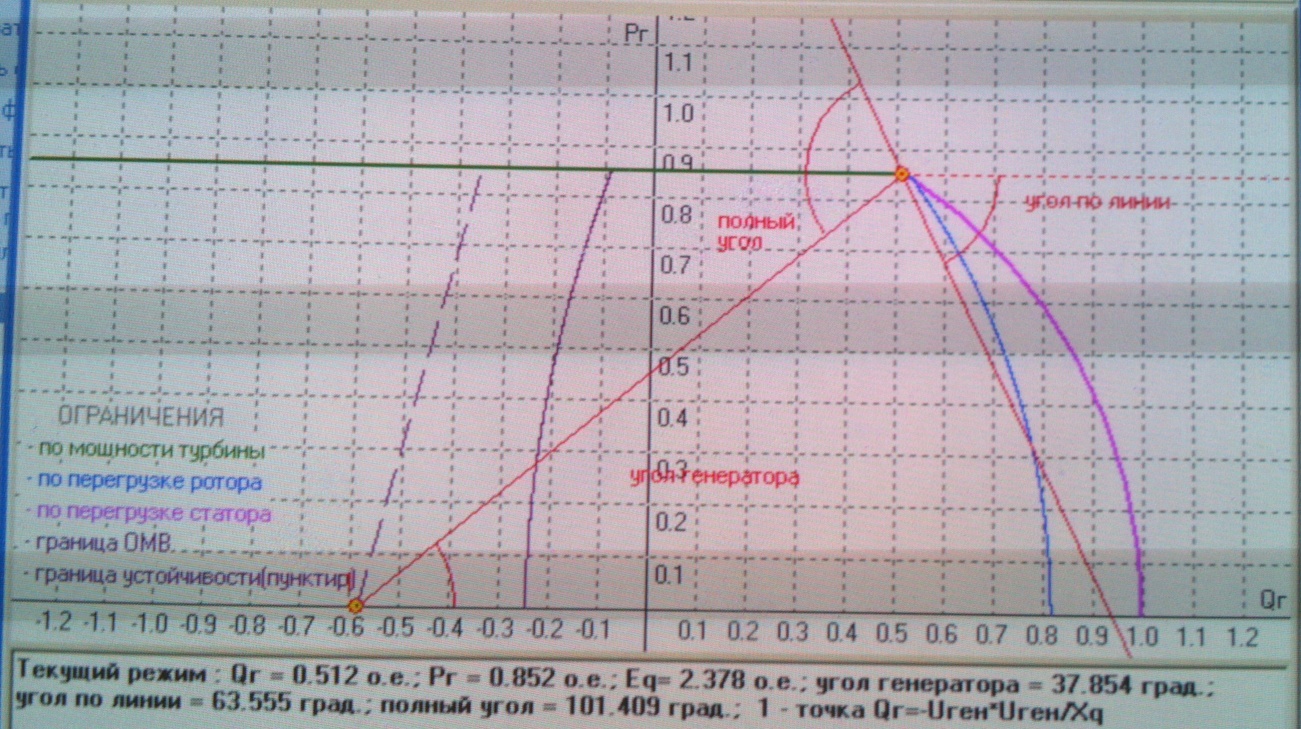
Рис.5.5 Диаграмма мощности рабочих режимов
Рассчитанные в среде «NETSIM» переходные процессы системы регулирования с учетом динамических свойств элементов регулятора:
1) Результаты расчета, переменные которого относятся к синхронному генератору (рис. 5.4) в относительных единицах холостого хода:
– отклонение частоты напряжения генератора ΔfU [рад/c] (выход блока Y29 на рис. 5.4):
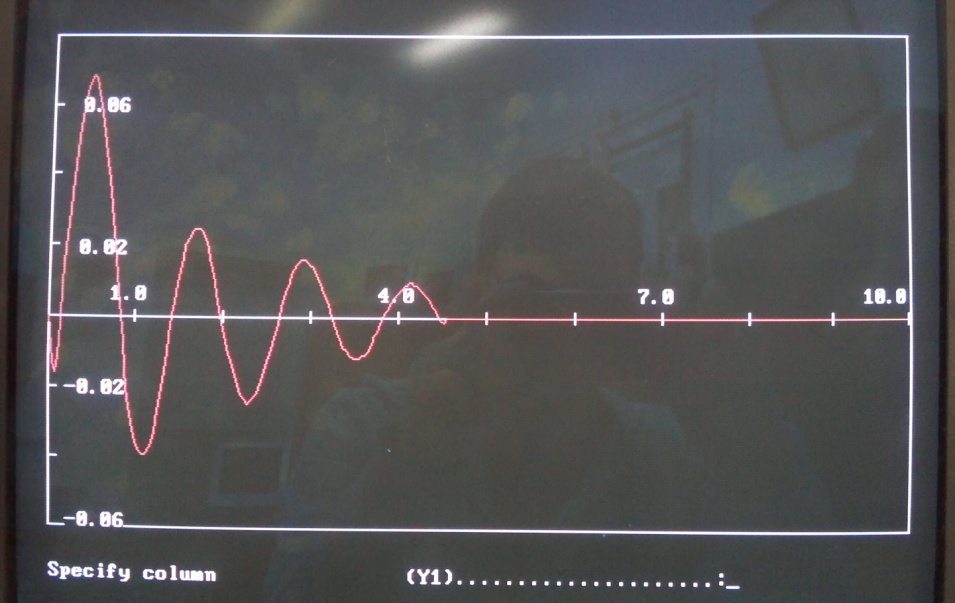
2) переменные, относящиеся к аппаратным блокам регулятора возбуждения – в вольтах:
– сигнал на выходе АРВ [В] (выход блока Y16 на рис. 5.3):
Вывод:в ходе лабораторной работы исследовали на компьютерной модели различные типы систем возбуждения и автоматических регуляторов возбуждения по программе, разработанной в «НИИ Электромаш». В ней были построены диаграммы мощности установившегося режима и смоделированы переходные процессы в блоках СГ и регулятора возбуждения.
| Выполнил ст-т ЭнФ 4-6 Егоренко В.Н. | ДАТА: |
| Принял асс. ЭСЭЭС Гончарова Н.В. |
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
по курсу «Общая химия»
Ростов - на – Дону
Содержание
1. Основные классы неорганических соединений . . . . . . . . . . . . . . . . . . . . 3
2. Строение атома . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .. . . . . . . . . . . . . 11
3. Химическая кинетика и равновесие . . . . . . . . . . . . . . . . . . . . . . . . . . . . 19
4. Растворы . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .. . . . . . . . . . . . 23
5. Электролитическая диссоциация . . . . . . . . . . . . . . . . . . ... . . . . . . . . . . . 26
6. Гидролиз солей . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .29
7. Окислительно-восстановительные реакции. . . . . . . . . . . . . . . . . . . . . .34
8. Электродные потенциалы. Гальванические элементы . . . . . . . . . . . . . .40
9. Коррозия металлов. Методы защиты от коррозии . . . . .. . . . . . . . . . . . 46
10. Вяжущие вещества. Коррозия бетонов . . . . . . . . . . . . .. . . . . . . . . . . . .52
Основные классы неорганических соединений
Роль химии в научно-техническом прогрессе велика. Множество простых и сложных веществ применяют в разных областях строительной, производственной и сельскохозяйственной сфер. Среди них достаточное количество неорганических соединений. К важнейшим классам неорганических соединений относят оксиды, основания, кислоты, соли.
Оксиды
Оксид – сложное вещество, включающее в себя два элемента, один из которых кислород в степени окисления -2. Общая формула оксидов ЭхОу , где х – число атомов элемента; у – число атомов кислорода.
Дата добавления: 2015-01-10; просмотров: 699;
