Строение и свойства атомов. Элемент азот N — первый представитель главной подгруппы V группы Периодической системы
Элемент азот N — первый представитель главной подгруппы V группы Периодической системы. Его атомы содержат на внешнем энергетическом уровне пять электронов, из которых три электрона неспаренные (вспомните правило «8-N»). Отсюда следует, что атомы этих элементов могут присоединять три электрона, завершая внешний энергетический уровень, и вследствие этого приобретают степень окисления -3, например в соединениях с водородом — аммиаке NН3 и с металлами — нитридах Li3N, Mg3N2 и др.
Атомы азота могут также отдавать свои внешние электроны более электроотрицательным элементам (фтору, кислороду) и приобретать при этом степени окисления +3 и +5. Атомы азота проявляют восстановительные свойства и в степенях окисления +1, +2, +4.
Азот — простое вещество. В свободном состоянии азот существует в виде двухатомной молекулы М2. В этой молекуле два атома N связаны очень прочной тройной ковалентной связью:

Эту связь можно обозначить и так:
N=N
Азот — бесцветный газ без запаха и вкуса. В воде растворяется хуже кислорода. Прочностью молекулы азота обусловлена его химическая инертность.
При обычных условиях азот взаимодействует только с литием, образуя нитрид Li3N:
6Li + N2 = 2Li3N
С другими металлами он взаимодействует только при высоких температурах.
Также при высоких температурах и давлении в присутствии катализатора азот реагирует с водородом, образуя аммиак:
2N+ ЗН2 <-> 2NH3
(дайте характеристику этой реакции и рассмотрите условия смещения химического равновесия вправо).
При температуре электрической дуги он соединяется с кислородом, образуя оксид азота(II) (дайте характеристику этой реакции и также рассмотрите условия смещения химического равновесия вправо).
В природе азот содержится в основном в атмосфере — 78,09% по объему или 65,6% по массе. Над каждым гектаром земной поверхности постоянно «висят» 8 тыс. т азота. Из природных неорганических соединений азота наиболее известна чилийская селитра NaNO3.
Большая часть связанного азота содержится в органических веществах.
Азот, полученный перегонкой жидкого воздуха, в промышленности применяют для синтеза аммиака и производства азотной кислоты. Раньше этот газ в качестве инертной среды использовали для наполнения электрических ламп. В медицине чистый азот применяется в качестве инертной среды при лечении туберкулеза легких, а жидкий азот — при лечении заболеваний позвоночника, суставов и др.
Круговорот азота в природе. Азот — жизненно важный элемент. Все основные части клеток тканей организма построены из белковых молекул, в состав которых входит азот. Без белка нет жизни, а без азота нет белка. Человек получает белки из растительной и животной пищи, животные, в свою очередь, получают их также из растений. Следовательно, растения — один из источников пополнения азота, который поддерживает жизнь.
Содержание связанного азота в почве очень незначительно (до 1 кг в 1 т), к тому же большая часть его входит в состав органических соединений и непосредственно недоступна для растений. Однако постепенно, в результате деятельности бактерий, органические соединения превращаются в минеральные — соли аммония или нитраты, которые и усваиваются растениями.
Азот входит в состав растительных белков. Животные получают готовые белковые вещества из растений; в животном организме содержится от 1 до 10% азота (по массе), в шерсти и в рогах — около 15%. Все важнейшие части клеток (цитоплазма, ядро, оболочка) построены из белковых молекул.
Еще большее значение имеют особые бактерии, которые живут в клубеньках на корнях бобовых растений (клевера, гороха, вики, люпина и др.), их так и называют «клубеньковыми». Вот эти бактерии и связывают свободный атмосферный азот, т. е. превращают его в соединения, которые усваивают растения, образуя белки своего организма.
Соединения азота в почве пополняются также во время грозовых ливней. Как вы уже знаете, при этом из азота и кислорода образуется оксид азота(П), который под действием кислорода воздуха превращается в оксид азота(IV):
2NO + 02 = 2NO2
Последний взаимодействует с водой (также в присутствии кислорода воздуха), и получается азотная кислота:
4NO2 + 02 + 2Н20 = 4НNO3
Эта кислота, попадая в почву, реагирует с находящимися в ней соединениями натрия, кальция, калия и образует соли — селитры, необходимые для растений (рис. 27).
Открытие азота. В 1772 г. английский ученый Д. Резерфорд и шведский исследователь К. Шееле обнаружили в своих экспериментах по сжиганию веществ газ, который не поддерживает дыхания и горения. Позднее, в 1787 г., А. Лавуазье установил наличие в воздухе газа, не поддерживающего дыхания и горения, и по его предложению этому газу было дано название «азот», означающее «безжизненный» (от лат. а — нет и зоэ — жизнь). Другое латинское название нитрогениум, введенное в 1790 г. Ж. Шапталем, означает «рождающий селитру».
Аммиак
Прежде всего рассмотрим строение молекулы аммиака NН3. Как вы уже знаете, на внешнем энергетическом уровне атомы азота содержат пять электронов, из которых три электрона неспаренные. Именно они и участвуют в формировании трех ковалентных связей с тремя атомами водорода при образовании молекулы аммиака NH3:
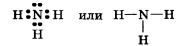
Три общие электронные пары смещены в сторону более электроотрицательного атома азота, а так как молекула аммиака имеет форму треугольной пирамиды (рис. 28), то в результате смещения электронных пар возникает диполь, т. е. система с двумя полюсами.
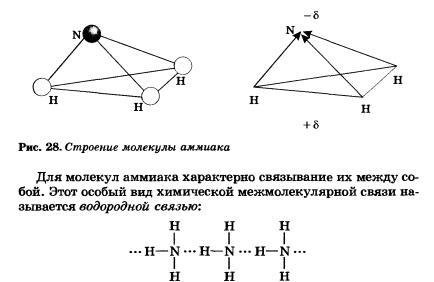
Водородная связь — это химическая связь между атомами водорода одной молекулы и атомами очень электроотрицательных элементов (фтора, кислорода, азота), имеющих иеподеленные электронные пары другой молекулы.
Это очень слабая связь — примерно в 15—20 раз слабее ковалентной. Благодаря ей некоторые низкомолекулярные вещества (т. е. имеющие небольшую молекулярную массу) образуют ассоциаты, что приводит к повышению температур плавления и кипения веществ. Водородная связь образуется между молекулами воды, спиртов, фтороводорода.
Очень важную роль играет водородная связь в молекулах важнейших для живых существ соединений — белков и нуклеиновых кислот.
Аммиак — бесцветный газ с резким запахом, почти в два раза легче воздуха. Аммиак нельзя вдыхать продолжительное время, так как он ядовит. Этот газ легко сжижается при обычном давлении и температуре -33,4 °С, а при испарении жидкого аммиака из окружающей среды поглощается много тепла, поэтому аммиак применяется в холодильных установках.
Аммиак очень хорошо растворим в воде: при 20 °С в 1 объеме ее растворяется около 710 объемов аммиака (рис. 29). Концентрированный водный раствор аммиака (25%-ный по массе) называется водным аммиаком, или аммиачной водой, а используемый в медицине раствор аммиака известен под названием нашатырный спирт. Тот нашатырный спирт, который имеется в вашей домашней аптечке, содержит 10% аммиака.
Если к раствору аммиака прилить несколько капель фенолфталеина, то он окрасится в малиновый цвет, т. е. покажет щелочную среду:
NH3 + Н20 <-> NH3 • Н20 -> NН4 + ОН-
Наличием гидроксид-ионов ОН- и объясняется щелочная реакция водных растворов аммиака. Если окрашенный фенолфталеином раствор аммиака подогреть, то окраска исчезнет (почему?).
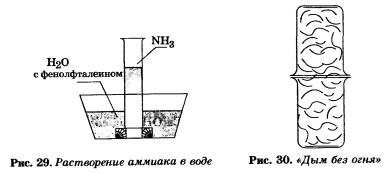
Аммиак взаимодействует с кислотами, образуя соли аммония. Это взаимодействие наглядно наблюдается в следующем опыте: если стеклянную палочку или стакан, смоченные раствором аммиака, поднести к другой палочке или стакану, смоченным раствором соляной кислоты, то появится густой белый дым (рис. 30). Вот и верь после этого поговорке, что дыма без огня не бывает:
NH3 + НСl = NH4Сl
Хлорид аммония
И водный раствор аммиака, и соли аммония содержат особый ион — катион аммония NH4, играющий роль катиона металла. Он получается в результате того, что атом азота имеет свободную (неподеленную) электронную пару, за счет которой и формируется еще одна ковалентная связь с катионом водорода, переходящего к аммиаку от молекул кислот или воды:
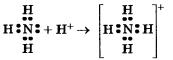
Такой механизм образования ковалентной связи, которая возникает не в результате обобществления непарных электронов, а благодаря свободной электронной паре, имеющейся у одного из атомов, называется донорно-акцепторным.
В данном случае донором этой свободной электронной пары служит атом азота в аммиаке, а акцептором — катион водорода кислоты или воды.
Еще одно химическое свойство аммиака вы сможете сами прогнозировать, если обратите внимание на степень окисления в нем атомов азота, а именно -3. Конечно же аммиак — сильнейший восстановитель, т. е. его атомы азота могут только отдавать электроны, но не принимать их. Так, аммиак способен окисляться или до свободного азота (без участия катализатора):
4NН3 + 302 = 2N2 + 6Н20
или до оксида азота(II) (в присутствии катализатора):
4NН3 + 502 = 4N + 6Н20
Как производят аммиак в промышленности, вы уже знаете — синтезом из азота и водорода. В лаборатории аммиак получают действием гашеной извести Са(ОН)2 на соли аммония, чаще всего на хлорид аммония:
Са(ОН)2 + 2NН4С1 = СаСl2 + 2NН3 + 2Н20
Газ собирают в перевернутый кверху дном сосуд, а распознают или по запаху, или по посинению влажной красной лакмусовой бумажки, или по появлению белого дыма при внесенной палочке, смоченной соляной кислотой. Аммиак и его соли широко используются в промышленности и технике, в сельском хозяйстве, быту. Основные области их применения показаны на рисунке 31.
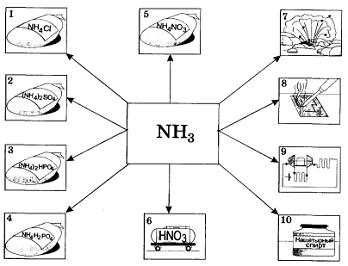
Рис. 31. Применение аммиака и солей аммония:
1—5 — производство минеральных удобрений; 6 — производство азотной кислоты; 7 — получение взрывчатых веществ; 8 — для паяния; 9 — в холодильных установках; 10 — в медицине и быту (нашатырный спирт)
6. Кислоты, ионное уравнение
С одним из представителей веществ этого класса вы уже познакомились, когда рассматривали летучие водородные соединения на примере хлороводорода HCl. Раствор его в воде и представляет собой соляную кислоту. Они имеет ту же формулу HCl. Аналогично при растворении в воде другого летучего водородного соединения — сероводорода H2S образуется раствор слабой сероводородной кислоты с формулой H2S.
Молекулы этих кислот состоят из двух элементов, то есть онн являются бинарными соединениями. Одннко к классу кислот относят также и соединения, состоящие из большего числи химических элементов. Кик привило, третьим элементом, входящим в состив кислоты, является кислород. Поэтому такие кислоты называют кислородсодержащими в отличие от HCl и H2S, которые называются бескислородными. Перечислим некоторые кислородсодержащие кислоты.

Обратите внимание, что все кислоты (н кислородсодержащие, и бескислородные) обязательно содержат водород, который в формуле записывается ня первом месте. Вся остальная часть формулы называется кислотным остатком. Например, у HCl кислотным остатком является Сl-.
Кислотами называются сложные вещества, молекулы которых состоят из атомов водорода и кислотных остатков.
Как правило, кислотные остатки образуют элементы-неметаллы.
По формулам кислот можно определить степени окисления атомов химических элементов, образующих кислоты.
Для бинарных кислот это сделать просто. Так как у водорода степень окисления +1. то в соединении H+1Cl-1 у хлора степень окисления -1, а в соединении H2+1S-2 у серы степень окисления -2.
Несложно будет рассчитать и степени окисления атомов элементов неметаллов, образующих кислотные остатки кислородсодержащих кислот. Нужно только помнить, что суммарная степень окисления атомов всех элементов в соединении равна нулю, а степени окисления водорода +1 и кислорода -2.
Зная степень окисления элемента-неметалла, образующего кислотный остаток кислородсодержащей кислоты, можно определить, какой оксид ей соответствует. Например, серной кислоте HgSO, в которой у серы степень окисления равна +6, соответствует оксид серы (VI) S03; азотной кислоте HN03, в которой у азота степень окисления равна +5, соответствует оксиl азота (V) NzOu.
По формулам кислот можно также определить и общий заряд, который имеют кислотные остатки. Заряд кислотного остатка всегда отрицателен и равен числу атомов водорода в кислоте. Число атомов водорода в кислоте называется основно стью. Для одноосновных кислот, содержащих один атом водорода, например HCl и HN08, заряды кислотных остатков равны 1-. Для двухосновных кислот, например H2SO4 и H2S, заряды кислотных остатков равны 2-, то есть
SO4 2- и S 2-.
В природе встречается много кислот: лимонная кислота в лимонах, яблочная кислота в яблоках, щавелевая кислота в листьях щавеля. Муравьи защищаются от врагов, разбрызгивая едкие капельки муравьиной кислоты. Она же содержится в пчелином яде и в жгучих волосках крапивы.
При скисании виноградного сока получается уксусная кислота, а при скисании молока — молочная кислота. Та же самая молочная кислота образуется при квашении капусты и при силосовании кормов для скота. Нам хорошо известны часто применяемые в быту лимонная и уксусная кислоты. Употребляемый в пищу уксус и представляет собой раствор уксусной кислоты.Многие кислоты нужны в народном хозяйстве в огромных количествах, производство этих веществ называется многотоннажным. К их числу относятся серная и соляная кислоты.
Серная кислота S2SO4 — бесцветная жидкость, вязкая, как масло, не имеющая запаха, почти вдвое тяжелее воды. Серная кислота поглощает влагу из воздуха и других газов. Это свойство серной кислоты используют для осушения некоторых газов.
При смешивании серной кислоты с водой выделяется большое количество теплоты. Если воду вливать в серную кислоту, то вода, не успев смешаться с кислотой, может закипеть и выбросить брызги серной кислоты на лицо и руки работающего. Чтобы этого не случилось, при растворении серной кислоты нужно вливать ее тонкой струей в воду и перемешивать.
Серная кислота обугливает древесину, кожу, ткани. Если в пробирку с серной кислотой опустить лучинку, то происходит химическая реакция — лучинка обугливается. Теперь понятно, как опасно попадание брызг серной кислоты на кожу человека и одежду.
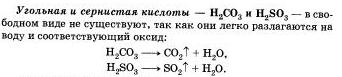
Растворы всех кислот кислые, но распознавать концентрированные кислоты на вкус не решится ни один химик — это опасно. Есть более эффективные и безопасные способы обнаружения кислот. Их так же, как и щелочи, распознают с помощью индикаторов.
Прильем к растворам кислот по нескольку капелек раствора лакмуса фиолетового цвета. Лакмус окрасится в красный цвет. Метиловый оранжевый при действии кислот меняет оранжевый цвет на красно-розовый.
А вот кремниевую кислоту, поскольку она нерастворима в воде, так распознавать нельзя.
При обычных условиях кислоты могут быть твердыми (фосфорная Н3Р04, кремниевая Н2SiO2) и жидкими (в чистом виде жидкостью будет серная кислота H2SO4).
Такие газы, как хлороводород HCl, бромоводород НВг, сероводород H2S, в водных растворах образуют соответствующие кислоты.
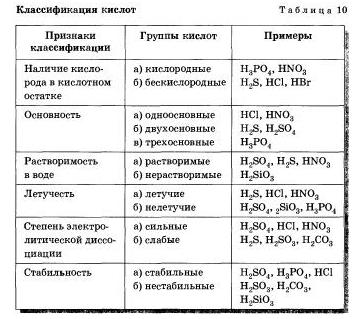
Вы уже знаете, что угольная Н2СО3 и сернистая H2SO3, кислоты существуют только в водных растворах, так как являются слабыми и нестойкими. Они легко разлагаются на оксиды углерода (IV) и серы (IV) — С02 и SO2, соответственно, и воду. Поэтому выделить эти кислоты в чистом виде невозможно.Часто путают понятия летучесть и устойчивость (стабильность). Летучими называют кислоты, молекулы которых легко переходят в газообразное состояние, то есть испаряются. Например, соляная кислота является летучей, во устойчивой, стабильной кислотой. О летучести нестабильных кислот судить нельзя. Например, нелетучая нерастворимая кремниевая кислота при стоянии разлагается на воду u SiO2.Водные растворы соляной, азотной, серной, фосфорной и ряда других кислот не имеют окраски. Водные растворы хромовой кислоты Н2СгJ2 имеют желтую окраску, марганцевой кислоты НМnО4 — малиновую. Однако, какими бы разными ни были кислоты, все они образуют при диссоциации катионы водорода, которые и обусловливают ряд общих свойств: кислый вкус, изменение окраски индикаторов (лакмуса и метилового оранжевого), взаимодействие с другими веществами. Разделение кислот на группы по различным признакам представлено в таблице 10.
Дата добавления: 2015-01-10; просмотров: 3342;
