СЕКРЕЦИЯ И РЕГУЛЯЦИЯ
Секреция белковых и полипептидных гормонов контролируется высокоспецифическими внеклеточными стимулами. В большинстве случаев такие стимулы представляют собой изменения уровня циркулирующих в крови веществ, что должно было бы привести к нарушению гомеостатического равновесия, а гормональные продукты, высвобождаемые вследствие этих изменений, действуют на соответственные органы-мишени, в результате чего восстанавливается гомеостаз (рис. 3—6). Например, повышение после приема пищи количества глюкозы в крови стимулирует секрецию инсулина, который в свою очередь стимулирует поглощение глюкозы мышцами, в связи с чем содержание глюкозы в крови нормализуется. Другим примером служит стимуляция высвобождения паратиреоидного гормона уже небольшим снижением уровня кальция в крови. Выделившийся при этом паратиреоидный гормон действует на свои органы-мишени — костную ткань и почки, способствуя обратному поступлению кальция во внеклеточную жидкость. Эти регуляторные процессы включают и ингибиторную петлю обратной связи, в силу которой продукты, вырабатываемые органами-мишенями и выделяемые в кровоток в ответ на действие гормонов, тормозят его дальнейшую секрецию. Например, снижение уровня глюкозы в крови тормозит дальнейшую секрецию инсулина, а увеличение содержания кальция в крови тормозит высвобождение паратиреоидного гормона. Большое число регуляторных петель обратной связи может действовать согласованно, что, например, наблюдается в отношении физиологической регуляции секреции различных гормонов передней долей гипофиза (рис. 3—7). В некоторых случаях точная природа стимула, участвующего в регуляции секреции гормона, выяснена недостаточно полно; эта неопределенность касается, например, «факторов», ответственных за «вспышки» секреторной активности, проявляемой передней долей гипофиза, и контролирующих элементов, управляющих циркадными или суточными ритмами.
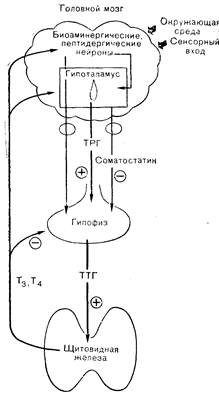
Рис. 3—7. Регуляторные петли обратной связи в гипоталамо-гипофизарной системе. Такая регуляция может быть показана на примере любого из гипофизарных гормонов, в частности ТТГ, ЛГ, ФСГ, пролактина, СТГ.
Окончательные детали молекулярных процессов сопряжения внеклеточных стимулов с секрецией гормона и в конце концов с биосинтезом нового гормона, необходимого для восполнения его количества в железе, неизвестны. В известных же случаях эти процессы в разных клетках, секретирующих белковые гормоны, могут быть различными. Имеются, однако, данные о том, что в секреции многих гормонов может принимать участие общий механизм сопряжения. Этот механизм в качестве 2-го медиатора использует цАМФ (рис. 3—8). Согласно данной модели, стимулирующий фактор не проникает в клетку, а взаимодействует с рецептором, расположенным в структурах плазматической мембраны. Каким-то образом при связывании с рецептором плазматической мембраны стимулирующий фактор активирует аденилатциклазу, что приводит к образованию 3,5-цАМФ, который в свою очередь превращает неактивную форму фосфорилирующего фермента — протеинкиназы в активную форму путем отсоединения регуляторной субъединицы (PC) от активной каталитической субъединицы (КС).

Рис. 3—8. Предполагаемый механизм действия полипептидных гормонов на клетку-мишень. KС — каталитическая субъединица; PC — регуляторная субъединица. Объяснения »
Протеинкиназа (активная субъединица) катализирует фосфорилирование определенных внутриклеточных белков, причем считается, что образующиеся таким образом фосфорилированные белки играют роль в процессах транспорта и секреции гормона, вероятно, путем активации микротрубочек и/или слияния мембран секреторных гранул с плазматической мембраной. В настоящее время из-за отсутствия экспериментальных доказательств перечисленных процессов они остаются в высшей степени гипотетическими. Действительно, о характере процессов и сил, участвующих во внутриклеточном продвижении белков, известно крайне мало.
Следует отметить важную роль кальция в секреторном процессе. Потоки кальция из внеклеточной жидкости в клетку, равно как и его потоки из внутриклеточных органелл (например, митохондрий) в цитозоль, тесно сопряжены с секреторными процессами. При дефиците кальция во внеклеточной жидкости секреция значительно тормозится. Возможно, что вход кальция в клетку каким-то еще не изученным образом связан с активацией аденилатциклазы.
На секрецию белковых гормонов многими эндокринными органами влияют и катехоламины, действующие через адренергические рецепторы, связанные с рецепторами, реагирующими на главные стимулы. Считают, что эти адренергические эффекты служат модуляторами секреторной активности, находящейся в основном под контролем главных стимулирующих факторов.
С секреторными процессами должны быть каким-то образом связаны процессы биосинтеза. Синтез новых молекул гормона необходим для пополнения потраченных и, наоборот, при уменьшении потребности в секреции должен был бы тормозиться и синтез новых молекул гормона, чтобы предотвратить перегрузку им клетки. Мало известно о клеточных механизмах, сопрягающих секреторные процессы с процессами биосинтеза, т. е. не ясно, непосредственно влияют внеклеточные факторы, регулирующие скорость секреции, на скорость биосинтеза гормона, или сам по себе процесс секреции обеспечивает появление регуляторных сигналов, передающихся на отдельные этапы биосинтеза. Степень сопряжения секреторной и биосинтетической активности в конкретной эндокринной железе в большой мере может определяться относительной величиной накопления гормонов в железе. Железы, обладающие сравнительно большим количеством гормона, могут удовлетворять потребность в секреции более длительное время, чем железы с меньшими запасами его. Судя по главному морфологическому признаку секреторных клеток — присутствию секреторных гранул, все эндокринные клетки в той или иной степени обладают запасом гормонов. Вероятно, такие запасающие системы возникли с целью придания эндокринным секреторным клеткам свойства буфера или резервуара гормона, который может быть мобилизован на удовлетворение секреторных потребностей в течение очень короткого времени, без включения механизмов острого изменения скорости биосинтеза гормона.
Конкретный этап (или этапы) процесса биосинтеза гормона, на котором осуществляется регуляция этого процесса, в настоящее время не известен. Согласно существующим представлениям (см. рис. 3—1), регуляция могла бы происходить на одном или нескольких уровнях; помимо синтеза ДНК (рост и деление клеток), эти уровни включают: 1—транскрипцию; 2—посттранскрипционные процессы; 3 — трансляцию; 4 — посттрансляционные процессы. Клеточный и молекулярный уровни регуляции биосинтеза большинства белковых гормонов идентифицированы далеко не в той степени, которая позволила бы сделать определенные заключения. Однако имеющиеся ограниченные сведения, касающиеся, например, биосинтеза паратиреоидного гормона, свидетельствуют о том, что главные объекты регуляторных влияний в ответ на изменение содержания кальция в крови локализуются на уровне деления клеток и/или транскрипционном этапе. Стимуляция железы в условиях снижения содержания кальция приводит, очевидно, к увеличению синтеза РНК и в конце концов к гиперплазии железы. В околощитовидной железе функционирует и 3-й регуляторный механизм на посттрансляционном уровне: изменение внутриклеточного кругоооборота гормона. Таким образом, до сих пор нет достаточно четких и убедительных данных, которые свидетельствовали бы о том, что внеклеточные стимулы могут быть ответственными за изменение скорости расщепления биосинтетических предшественников или скорости инициации и трансляции мРНК, кодирующих гормоны.
Дата добавления: 2015-01-19; просмотров: 1164;
