ОБЩИЕ АСПЕКТЫ БИОСИНТЕЗА БЕЛКА
Процессы синтеза белка включают много сложных реакций, с помощью которых информация, исходно закодированная на полинуклеотидном «языке» гена (ДНК) в конце концов будет выражена полиаминокислотным «языком» конечного биологически активного белка. В целях обсуждения эти процессы можно разделить на четыре этапа (рис. 3—1).
1. Транскрипция. Синтез РНК в форме предшественников, обладающих большой молекулярной массой, на матрице ДНК.
2. Посттранскрипционная модификация. Контролируемая модификация РНК, включающая этапы образования мРНК из РНК-предшественника путем вырезания и нового объединения сегментов РНК, равно как и модификации 3-конца РНК за счет полиаденилирования и 5 -конца за счет добавления 7-метилгуанозиновых «колпачков».
3. Трансляция. Сборка аминокислот с помощью специфического взаимодействия антикодонов аминоацилированных тРНК,— «носителей» с соответствующими кодонами мРНК, связанной с полирибосомами, и, наконец, полимеризации аминокислот с образованием полипептидной цепи.
4. Посттрансляционная модификация. Одна реакция или их сочетание, включающее расщепление пептидных связей (превращение биосинтетических предшественников в промежуточные или окончательные формы белка путем протеолитического расщепления), образование аминокислотных производных. (гликозилирование, фосфорилирование) и складывание полученной полипептидной цепи с приданием ей нативной конфигурации.
Последний этап синтеза белка представляет особый интерес в силу того, что такие посттрансляционные модификации могут являться способом, которым клетка различает отдельные классы белков и направляет их в соответствующие области, где они оказывают свое действие [1].
Эта проблема (разделение белков по клеточным пространствам после синтеза) уже много лет привлекает внимание специалистов в области клеточной биологии. Установлено, что типичная эукариотическая клетка за определенное время в процессе цикла синтезирует около 50 000 различных белков [2]. Современные данные свидетельствуют о том, что это множество производимых клеткой различных белков синтезируется общим пулом полирибосом [3]. Каждый вид синтезированных белков направляется в специальное место, где проявляется его специфическая биологическая функция. Например, особые группы белков транспортируются в ядро и другие субклеточные органеллы, где они выполняют функции либо регуляторных белков, либо ферментов, либо структурных белков, участвующих в биогенезе различных органелл, тогда как другие группы белков синтезируются специально на экспорт из клетки (иммуноглобулины, факторы свертывания крови, сывороточный альбумин и белковые или пептидные гормоны). Понятно, что силы, принимающие участие в этом процессе направленного транспорта белков, должны определяться очень сложным сочетанием информационных сигналов. Другими словами, поскольку информация для этого процесса транслокации может заключаться только во всей, либо в части первичной структуры или в конформационных свойствах самого белка, то посттрансляционная модификация (см. рис. 3—1) может играть решающую роль в определении белковой функции. Как только вновь синтезированный белок высвобождается из комплекса мРНК — рибосома — образующаяся цепь, дальнейшая регуляторная роль РНК представляется совершенно невероятной.
Другая проблема, стоящая перед исследователями, работающими в области биосинтеза полипептидных гормонов, заключается в том, каким образом регулируются биосинтетические и секреторные процессы. Исследования регуляторных механизмов ведутся в двух направлениях: 1 — изучение природы клеточных механизмов, — участвующих в сопряжении внеклеточных регуляторных стимулов с внутриклеточными процессами, определяющими изменения образования и высвобождения гормонов; 2 — определение стадии синтеза белка, на которую направлена регуляция, т. е. выяснение происходит она на транскрипционном (и претрансляционном), трансляционном или посттрансляционном уровне.
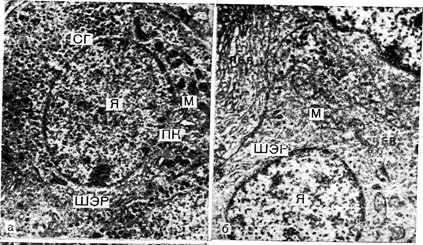
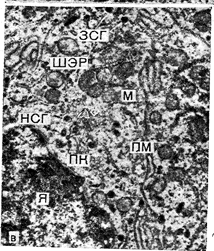
Рис. 3—2. Типичные продуцирующие белковые гормоны эндокринные клетки, в которых видны субклеточные органеллы. а — Гипофизарный тиротроф (мышь); б — опухоль у мыши. состоящая из тиротропных клеток, сохраняемая путем серийных подкожных трансплантаций мышам с гипотиреозом: в — околощитовидная железа быка: Можно видеть (резко выраженный ШЭР и редкие секреторные гранулы в опухоли из тиротропных клеток (см. рис. 3—26) по сравнению с нормальным гипофизарным тиротрофом (см. рис. 3—2а).
Я — ядро: ШЭР — шероховатый эндоплазматический ретикулум; ПК — пластинчатый комплекс: М — митохондрия; ПМ — плазматическая мембрана; СГ — секреторная гранула; ИСТ незрелая секреторная гранула зсг — зрелая секреторная гранула. Электронная микрофотография Х10000.
Дата добавления: 2015-01-19; просмотров: 1446;
