ВИРУСНЫЙ КАНЦЕРОГЕНЕЗ
Опухолеродные ДНК-содержащие вирусы
· Вирус EBV поражает эпителиальные клетки полости носа, гортани и уха, а также В-лимфоциты. Его тропность в значительной степени определяется молекулой адгезии CD-21, экспрессированной на этих клетках.
· Поражение В-клеток, приводящее к развитию лимфомы Беркитта носит скрытый характер, при котором линейный геном EBV присутствует в В-лимфоцитах в виде эписомы (плазмиды), т.е. самостоятельной кольцевой внехромосомной молекулы ДНК. Репликации вируса не происходит. Клетка приобретает бессмертие.
· В молекулярные механизмы опухолевого роста вовлечены: мембранный белок EBV – LMP - 1, предотвращающий апоптоз путем взаимодействия с геном bcl-2 и усиливающий продукцию ИЛ-10, повышающего В-клеточную активность; ядерные белки EBV: EBNA -LP, вовлеченный в регуляцию аутокринных факторов, необходимых для роста В-клеток; EBNA-1,поддерживающий вирус в скрытом состоянии; EBNA-2, индуцирующий экспрессию поверхностных клеточных маркеров (CD 21; CD 23) и клеточных протоонкогенов (с - fgr и с - myc); EBNA-3, усиливающих экспрессию LMP – 1.
· Активно размножающаяся популяция В-лимфоцитов имеет повышенный риск мутации при транслокации t (8; 14), в результате которой ген с-myc, контролирующий пролиферацию, контактирует с одним из локусов гена Ig. Активация с-myc дает пораженным клеткам преимущества в росте, но недостаточна для малигнизации и рассматривается лишь как один из этапов в многоступенчатом процессе развития лимфомы Беркитта.
· Вирус HBV вызывает гепатоцеллюлярный рак, эндемичный в странах Дальнего Востока и Африки.
· Геном HBV не кодирует онкобелки и не обнаруживает закономерной интеграции вблизи какого-либо известного протоонкогена. Предполагается, что он оказывает непрямое и, возможно, многофакторное действие.
· HBV, вызывая хроническое повреждение гепатоцитов и их регенеративную гиперплазию, расширяет пул клеток, подвергающихся риску генетических изменений. В митотически активных гепатоцитах мутации могут иметь случайный характер или вызываться агентами из микроокружения, например, афлотоксинами.
· HBV кодирует регуляторный белок HBx, активирующих транскрипцию клеточных протоонкогенов (инициация) и протеинкиназу С (промоция).
 |
 |
 |
 |
Раздел VII.
СТАДИИ КАНЦЕРОГЕНЕЗА. ИНИЦИАЦИЯ
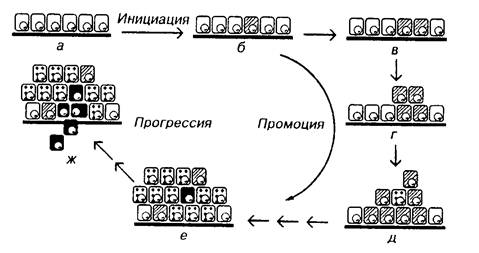
а - нормальные эпителиальные клетки ; б - появление (инициация) одной клетки; в, г, д - развитие (промоция) атипической пролиферации; е - приобретение злокачественных свойств (Ca in situ); ж - прорыв (инвазия) базальной мембраны, способность к прогрессии и метастазированию. (По В.Г. Черенкову, 1999)
Канцерогенез – стадийный многоступенчатый процесс, основу которого составляют нелетальные повреждения генома клеток (мутации), накопление этих мутаций и их проявления на уровне приобретения какого-либо фенотипа. У злокачественных опухолей этот фенотип включает в себя: избыточный рост, инвазию, способность к метастазированию.
· Генетическая концепция канцерогенеза подразумевает, что популяция опухолевых клеток – результат размножения, идущего от одной клетки – родоначальницы клона, претерпевающего опухолевую трансформацию.
· Основными мишенями генетического воздействия при опухолевой трансформации являются 3 класса регуляторных генов: протоонкогены, антионкогены и гены, контролирующие апоптоз. Мутантные аллели протонкогенов расцениваются как доминантные: они трансформируют клетки, несмотря на наличие их нормальных копий. В противоположность этому мутантные аллели генов-онкосупрессоров являются рецессивными и проявляются только в гомозиготном состоянии. Гены, контролирующие апоптоз, могут выступать и как анти-онкогены и как протоонкогены.
Дата добавления: 2015-03-26; просмотров: 1310;
