Валентность I. У атома лития электрон, находящийся на 2 s-подуровне, менее прочно связан с ядром, чем электроны первого энергетического уровня
s
У атома лития электрон, находящийся на 2 s-подуровне, менее прочно связан с ядром, чем электроны первого энергетического уровня, поэтому в химических реакциях атом лития может легко отдавать этот электрон, превращаясь в ион Li+ (ион - электрически заряженная частица). В этом случае ион лития приобретает устойчивую завершенную оболочку благородного газа гелия:
3Li+ 1s2.
Следует заметить, что, число неспаренных (одиночных) электронов определяет валентность элемента, т.е. его способность образовывать химические связи с другими элементами.
Так, атом лития имеет один неспаренный электрон, что обусловливает его валентность, равную единице.
Электронная формула атома бериллия:
4 Bе 1s2 2s2.
Электронно-графическая формула атома бериллия:
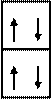 2 Валентность в основном
2 Валентность в основном
Дата добавления: 2015-03-23; просмотров: 1209;
