Основные виды диаграмм (5 видов).
Для характеристики изменений структуры сплавов в зависимости от состава и температуры строят диаграммы состояния. Они представляют собой графическое изображение равновесного или неравновесного состояния сплавов и строят их в координатах температура – состав.
1) Диаграмма состояния двойных сплавов, образующих при затвердевании смесь кристаллов чистых компонентов.Явления, происходящие при затвердевании таких сплавов, совершенно аналогичны тем, которые происходят при затвердевании раствора поваренной соли в воде. Рассмотрим в виде примера сплав свинца с сурьмой, структура которого относится к рассматриваемому типу.
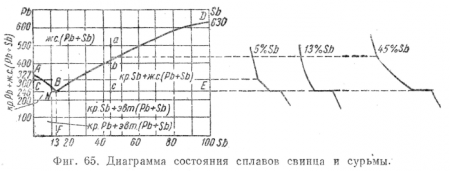 Чтобы получить диаграмму состояния сплавов системы свинец—сурьма, строим предварительно кривые охлаждения для сплавов с различным содержанием свинца и сурьмы, затем берем систему осей координат ХY и, откладывая по оси X весовые соотношения свинца и сурьмы, а по оси Y — температуры, переносим на нее с кривых охлаждения критические точки.
Чтобы получить диаграмму состояния сплавов системы свинец—сурьма, строим предварительно кривые охлаждения для сплавов с различным содержанием свинца и сурьмы, затем берем систему осей координат ХY и, откладывая по оси X весовые соотношения свинца и сурьмы, а по оси Y — температуры, переносим на нее с кривых охлаждения критические точки.
Чем больше будет взято для наблюдения сплавов с различным содержанием свинца и сурьмы, т. е. чем больше будет построено кривых охлаждения, тем более точно может быть построена диаграмма состояния.
Главных критических точек будет три: температура плавления свинца (327°), температура плавления сурьмы (630°) и температура плавления эвтектики этого сплава (246°), получающаяся, как показывает опыт, при 13% содержания в сплаве сурьмы.
Проследим за изменением в состоянии сплава с содержанием 45% Sb при охлаждении его от 500°. От а до b (фиг. 65) сплав находится в жидком состоянии и представляет собой одну фазу жидкого раствора; в точке b начинается выделение из жидкого раствора кристаллов Sb; в интервале от b до с сплав представляет смесь двух фаз — жидкого раствора и твердых кристаллов Sb, при этом состав жидкой фазы изменяется по линии ликвидуса bВ и в точке с доходит до концентрации 13% Sb. В точке с происходит затвердевание оставшегося жидкого сплава и распадение его на эвтектическую смесь кристаллов Рb и Sb. В период затвердевания эвтектики, пока сплав находится при температуре 246°, он представляет собой смесь трех фаз — жидкого раствора (Pb, Sb), кристаллов Рb и кристаллов Sb. Ниже точки с сплав представляет смесь двух фаз — кристаллов Рb и кристаллов Sb.
2) Диаграммы состояния двойных сплавов, способных образовать химические соединения, нерастворимые в твердом состоянии ни в одном из компонентов. Рассмотрим случай, когда компоненты сплава А и В способны образовать лишь одно химическое соединение С.
 Пусть для образования химического соединения С требуется Кс%В и (100— Кс)% А; если количество В будет меньше Кс%, то в результате взаимодействия А и В образуется С при некотором свободном остатке свободного A; при избытке же В сверх Кс% образуется С при наличии остатка свободного В. Диаграмма состояния таких сплавов из А и В представлена на фиг, 71.
Пусть для образования химического соединения С требуется Кс%В и (100— Кс)% А; если количество В будет меньше Кс%, то в результате взаимодействия А и В образуется С при некотором свободном остатке свободного A; при избытке же В сверх Кс% образуется С при наличии остатка свободного В. Диаграмма состояния таких сплавов из А и В представлена на фиг, 71.
Области этой диаграммы имеют следующие значения:
При концентрации, равной КэвтАс%, получим эвтектику (А + С).
При концентрации, равной Кс%, получим С.
При концентрации, равной Кэвтсв%у получим эвтектику (С + В).
Имеются металлы, способные образовать между собой не одно, а несколько химических соединений.
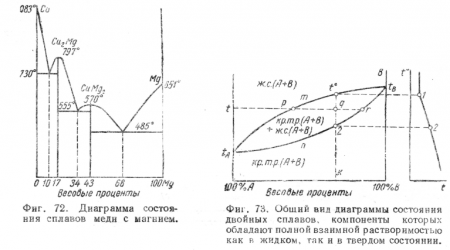 3)Диаграмма состояния двойных сплавов, компоненты которых обладают полной взаимной растворимостью как в жидком, так и в твердом виде.Если два тела способны сохранить взаимную растворимость не только в жидком, но и в твердом состоянии, то при затвердевании они образуют кристаллы смешанного состава. Вещества, входящие в состав кристаллов твердого раствора, могут содержаться в этих кристаллах в произвольных весовых отношениях.
3)Диаграмма состояния двойных сплавов, компоненты которых обладают полной взаимной растворимостью как в жидком, так и в твердом виде.Если два тела способны сохранить взаимную растворимость не только в жидком, но и в твердом состоянии, то при затвердевании они образуют кристаллы смешанного состава. Вещества, входящие в состав кристаллов твердого раствора, могут содержаться в этих кристаллах в произвольных весовых отношениях.
Если два тела способны к образованию твердых растворов, то при затвердевании жидких растворов этих тел из жидкости начинается выпадение кристаллов твердого раствора, более богатых компонентом, повышающим температуру плавления раствора. Таким образом, кристаллы твердого раствора имеют переменный состав; в случае медленного охлаждения состав кристаллов твердого раствора может выравниваться вследствие диффузии.
Допустим, что вещества А и В, имеющие температуры плавления tA и tB ,способны к образованию твердого раствора. Составим из этих веществ ряд смесей всевозможных концентраций В и А и построим для каждой смеси кривую охлаждения, подобную кривой на фиг. 73 (правая часть чертежа). Возьмем с каждой кривой охлаждения точки начала и конца затвердевания и перенесем их на диаграмму состояния, затем соединим все точки начала затвердевания одной линией и все точки конца затвердевания — другой. Первая из этих линий будет, очевидно, линией ликвидуса, а вторая — солидуса. В результате такого построения получим диаграмму состояния, представленную на фиг. 73: здесь tAmtB — линия ликвидуса и tAntB— линия солидуса.
При температурах, лежащих выше температуры, определяемой точкой 1 на кривой охлаждения, сплав состава К представляет
собой жидкую фазу; в интервале температур, определяемых точками 1 и 2, сплав имеет две фазы— жидкий раствор и кристаллы твердого раствора; при температурах, лежащих ниже температур, определяемых точкой 2, сплав представляет одну твердую фазу (твердый раствор). Возьмем сплав, содержащий К%В при температуре г; состояние этого сплава на диаграмме определяется точкой q. Из диаграммы видно, что при температуре t° сплав будет находиться частью в твердом и частью в жидком состоянии. Рассматривая линию tpqr, можно заметить, что при температуре t0 нацело затвердевает сплав, содержащий tr% В, и в совершенно жидком состоянии будет сплав, содержащий tp%B. С изменением температуры точка q будет перемещаться кверху или книзу по линии kq, а точки г и р будут скользить по линиям солидуса и ликвидуса; следовательно, состав твердой фазы сплава во время затвердевания будет изменяться по линии tAntB, а состав жидкой фазы — по линии tAmtB.
 4) Диаграмма состояния сплавов, обладающих полной взаимной растворимостью в жидком виде и ограниченной в твердом. Большинство металлов обладает способностью растворять в себе другие металлы или металлоиды лишь в ограниченной степени. Если такой ограниченной взаимной растворимостью обладают вещества А и В, то при затвердевании доэвтектических сплавов сначала будут выпадать кристаллы А, содержащие в растворе некоторое количество В, а при затвердевании заэвтектических сплавов кристаллы В, содержащие в растворе некоторые количества А; эвтектика же будет состоять из кристаллов двух твердых растворов.
4) Диаграмма состояния сплавов, обладающих полной взаимной растворимостью в жидком виде и ограниченной в твердом. Большинство металлов обладает способностью растворять в себе другие металлы или металлоиды лишь в ограниченной степени. Если такой ограниченной взаимной растворимостью обладают вещества А и В, то при затвердевании доэвтектических сплавов сначала будут выпадать кристаллы А, содержащие в растворе некоторое количество В, а при затвердевании заэвтектических сплавов кристаллы В, содержащие в растворе некоторые количества А; эвтектика же будет состоять из кристаллов двух твердых растворов.
Диаграмма состояний сплава из двух компонентов, обладающих полной взаимной растворимостью в жидком виде и ограниченной в твердом, представлена в общем виде на фиг. 75. Эта диаграмма будет вполне понятна, если мы проследим по ней за охлаждением нескольких сплавов, состав которых соответствует наиболее характерным областям диаграммы.
5)Перитектическсе превращение.Перитектическим называется такой вид превращения, при котором жидкий сплав, взаимодействуя с ранее образовавшимися кристаллами, образует новый вид кристаллов.
Перитектические превращения происходят при постоянной температуре.
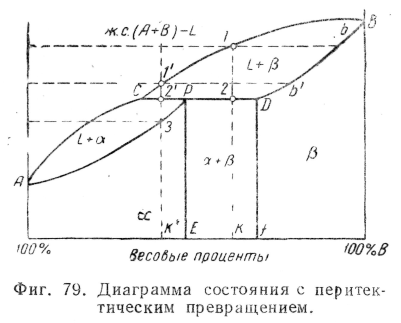
На фиг. 79 приведен общий вид диаграммы состояния с перитектическим превращением.
Линией ликвидуса здесь является линия АСВ, линией солидуса — APDB; перитектическое превращение происходит при температуре, определяемой отрезком CPD, параллельным оси X.
Проследим за охлаждением сплава, содержащего К% В.
Кристаллизация начинается в точке 1; содержание компонента В в образующихся кристаллах твердого раствора р определяется точкой b; при падении температуры от 1 до 2 содержание В в кристаллах твердого раствора меняется
Таким образом, после перитектического превращения этот сплав будет состоять из твердых растворов а и р; структура этих двух твердых фаз будет состоять из крупных участков ранее образовавшихся кристаллов b и участков, образовавшихся затем из кристаллов b и жидкого сплава кристаллов а. Следовательно, в результате перитектического превращения получается несходная с эвтектической структура, состоящая из сочетания участков двух фаз твердых растворов а и b.
Дата добавления: 2015-03-19; просмотров: 1218;
