НАРУШЕНИЯ ОБМЕНА ВИТАМИНОВ
Витамины- это группа органических веществ (незаменимые пищевые факторы, не синтезируемые в организме в необходимом количестве, не включающиеся в структуру тканей и не используемые организмом в качестве источника энергии), абсолютно необходимых для нормального развития и жизнедеятельности организма животных и человека. Они обеспечивают оптимальную скорость протекания биохимических реакций и физиологических процессов за счет выполнения непосредственно или в составе более сложных соединений каталитических и регуля-торных функций [Березов Т.Т.,Коровкин Б.Ф.,1998; Филиппович Ю.Б., 1999и др.].
Выделяют две группы витаминов: жирорастворимые (A, D, Е и К) и водорастворимые (BlfВ2, пантотеновая кислота, РР, В6, Bg, B12, H, С и Р). Кроме того, существуют так называемые витаминоподобные вещества (холин, липоевая, пангамовая, оротовая кислоты, инозит, убихи-нон, карнитин, витамин U и др.), обладающие некоторыми свойствами витаминов, но не являющиеся строго обязательными пищевыми факторами (нутриентами).Дефицит витаминоподоб-ных веществ не проявляется определенным специфическим симптомокомплексом.
Заболевания, развивающиеся при глубоком дефиците витаминов в организме (отсутствии поступления с пищей некумулируемых и несин-тезируемых эндогенно витаминов либо нарушении их обмена) и характеризующиеся клиническими симптомами, принято называть авитами-
Глава 11 / ПАТОФИЗИОЛОГИЯ ТИПОВЫХ НАРУШЕНИЙ ОБМЕНА ВЕЩЕСТВ
нозами (цинга, бери-бери, пеллагра, рахит и др.). В случае, если витамины поступают с пищей и/ или усваиваются в недостаточном количестве либо они запасаются или частично синтезируются в организме, клиническая картина заболевания (гиповитаминоз)менее специфична и характеризуется преобладанием общих, неспецифических проявлений умеренного дефицита витаминов (головокружение, раздражительность, головная боль, ослабление памяти, физическая и умственная утомляемость и т.д.). Недостаток витамина сначала ведет к мобилизации его запасов в организме и истощению тканевых депо (печень и жировая ткань для жирорастворимых витаминов), затем к биохимическим нарушениям (субклинический дефицит) и, наконец, к истинной недостаточности с выраженной клинической картиной заболевания. При недостаточности питания может иметь место дефицит не одного витамина, а нескольких (полигипо-или полиавитаминоз),приводящий к развитию сложной клинической картины. Гипервитами-нозы- патологические состояния, вызванные поступлением в организм чрезмерно большого количества витаминов и характеризующиеся нарушениями физиологических процессов, связанными со специфической ролью витаминов в обмене веществ, а отчасти имеющие характер неспецифического отравления. Более других токсичны жирорастворимые витамины А и D.
Гипо- и авитаминозы у человека и животных называют экзогенными(первичными), если их причиной является недостаточное поступление или полное отсутствие витаминов (или их предшественников) в пище при нормальных потребностях. Важнейшими причинами эндогенных(вторичных) гипо- и авитаминозов являются:
1) недостаточный синтез некоторых витаминов кишечной микрофлорой;
2) нарушения процессов всасывания витаминов при заболеваниях желудочно-кишечного тракта, печени, поджелудочной железы;
3) усиленный распад или конкурентная утилизация витаминов в кишечнике при наличии кишечных паразитов и патогенной микрофлоры;
4) поступление в организм антивитаминов (пищевых, лекарственных и др.)>
5) повышенные потери витаминов;
6) повышенная потребность в витаминах при некоторых физиологических и патологических состояниях (беременность, лактация, физичес-
кая и нервно-психическая нагрузка, тиреотоксикоз и др.);
7) нарушения обмена витаминов, связанные с заболеваниями органов, которые принимают участие в метаболизме витаминов, или с недостатком необходимых для метаболизма витаминов веществ;
8) врожденные нарушения обмена витаминов.
К врожденным нарушениям обмена и функций витаминов относятся витаминзависимыесостояния (корригируются мегадозами витаминов) и витаминрезистентныесостояния (введение даже высоких доз соответствующих витаминов не устраняет явлений их недостаточности). Клиническая картина врожденных нарушений обмена и функций витаминов (пиридоксин-зависимый судорожный синдром, пиридоксин-зависимая анемия, витамин D-резистентный рахит, витамин D-зависимый рахит и др.) мало отличается от клинической картины алиментарного авитаминоза. Причинами развития подобных заболеваний являются генетические дефекты, вызывающие нарушения как собственно обмена витаминов, который осуществляется при участии специфических белков и ферментов (нарушения процессов всасывания, транспорта, превращений витаминов в коферменты или в активные формы, нарушения взаимодействия ко-фермента с апоферментом, т. е. дефект образования холофермента), так и нарушения синтеза тех белков, при взаимодействии с которыми витамины или их активные формы осуществляют свои специфические функции в обмене веществ (наследственный дефект синтеза апофермента) (рис. 72).
Согласно данным эпидемиологических исследований, проведенных институтом питания РАМН, в различных регионах страны [Тутельян В.А., Спиричев В.Б., Шатнюк Л.Н. и др., 1993 -1999], рацион питания значительной части населения России характеризуется недостаточным содержанием эссенциальных факторов питания: витаминов, микроэлементов и др. Недостаток витамина С, по обобщенным данным, выявляется у 80 - 90% обследуемых; недостаточная обеспеченность витаминами В,, В2, В6, фолиевой кислотой - у 40-80%; 40-55% населения испытывают дефицит каротина. Дефицит витаминов является постоянно действующим неблагоприятным фактором во всех группах населения во всех регионах страны и зачастую носит характер полигиповитаминоза (витамин С, витамины груп-
Часть II. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ
Рис. 72. Возможные нарушения обмена и функций витаминов: 1 - нарушение всасывания в кишечнике;
2 - нарушение транспорта к органам и тканям;
3 - нарушение превращений в коферменты или активные формы; 4 - нарушение синтеза апофер-
ментов или специфических белков, взаимодействующих с витамином при реализации его функций;
5 - нарушение взаимодействия кофермента или иной
активной формы витамина с апоферментом или
специфическим белком (по В.Б. Спиричеву, 1977)
пы В, каротин), сочетающегося у значительной части детей, беременных и кормящих женщин с недостатком железа и развитием железодефицит-ной анемии. В ряде регионов полигиповитаминоз сочетается с недостаточным поступлением йода, селена, кальция, фтора и ряда других макро- и микроэлементов, что требует применения в терапии витамин-минеральных комплексов.
Знание этиологии и патогенеза нарушений обмена витаминов необходимо для проведения дифференциальной диагностики и патогенетической терапии данных состояний.
11.3.1. Жирорастворимые витамины Витамины группы А
Термин «витамин А» (антиксерофтальмичес-кий фактор) объединяет группу близких по химической структуре соединений - ретинол, ре-тиналь, ретиноевую кислоту, их эфиры.
Характерными симптомами недостаточности витамина А у человека и животных являются специфические поражения глаз, кожи, слизистых оболочек, торможение роста, снижение массы тела, общее истощение организма. Поражение эпителия кожи проявляется его ускоренной пролиферацией и патологическим ороговением, что сопровождается развитием фолликулярного папулезного гиперкератоза («жабья кожа»). Нарушение эпителизации вызывает сухость кожи, шелушение, развитие вторичных инфекций. При авитаминозе А поражается также эпителий слизистой оболочки мочеполовой и дыхательной систем, а также пищеварительного тракта, что вызывает (усугубляет) нарушение всасывания жирорастворимых витаминов. Снижение барьерной функции кожи и слизистых оболочек способствует проникновению в организм болезнетворных микробов и возникновению дерматитов, ларинготрахеобронхитов, пневмоний, циститов, пиелитов и т.д. Ороговение эпителия слезного канала приводит к его закупорке, развитию сухости конъюнктивы и роговой оболочки глаза (ксерофтальмия) с последующим конъюнктивитом, отеком, изъязвлением и размягчением роговицы (кератомаляция), так как глазное яблоко не омывается слезной жидкостью, обладающей бактерицидными свойствами. Может наблюдаться атрофия слезных желез. На склерах образуются очаги гиперкератоза (бляшки Бито). Исходом кератомаляции может быть помутнение роговицы (бельмо), приводящее к слепоте (амблиопия).Специфическим симптомом авитаминоза (гиповитаминоза) А является куриная, или сумеречная, слепота (гемералопия).Недостаточность витамина А проявляется прежде всего нарушением темновой адаптации -увеличением промежутка времени, необходимого для адаптации после перехода из освещенного помещения в темное. Наряду с этим увеличивается зрительный порог, т. е. минимальная интенсивность света, которая вызывает зрительные ощущения.
Витамин А обладает широким спектром биологического действия. Он участвует в процессах фоторецепции, необходим для роста тела, воспроизведения потомства, поддержания иммунологического и гематологического статуса, пролиферации и дифференцировки тканей (эпителии кожных покровов, слизистых, сперматоген-ный эпителий, костная ткань); влияет на мно-
Глава 11 / ПАТОФИЗИОЛОГИЯ ТИПОВЫХ НАРУШЕНИЙ ОБМЕНА ВЕЩЕСТВ
гие стороны обмена веществ: тканевое дыхание и энергетический обмен в тканях (стабилизирует митохондриальные мембраны и активирует синтез убихинона), обмен белков (воздействует на инициацию репликации), углеводов (участвует в синтезе мембранных гликопротеинов и глико-липидов), липидов (влияет на превращение ме-валоновой кислоты в холестерин), нуклеиновых кислот. Большинство из метаболических эффектов витамина А связано с его влиянием на стабильность и проницаемость клеточных мембран.
Развитие гемералопии при гиповитаминозе А связано с участием витамина в фотохимическом акте зрения. Светочувствительным пигментом сетчатки (палочек) является сложный белок родопсин, состоящий из липопротеина опсина и простетической группы, представленной 11-цис-ретиналем (рис. 73). На свету родопсин расщепляется на опсин и ретиналь, последний подвергается превращению в транс-форму. Фотоизомеризация ретиналя вызывает местную деполяризацию мембраны, что приводит к возникновению электрического импульса, который распространяется по нервному волокну. Цикл превращений светочувствительного пигмента завершается в темноте регенерацией родопсина (соединением опсина и 11-цис-ретяналя, который может синтезироваться из цис-ретинола или транс-ретиналя) и восстановлением чувствительности к свету слабой интенсивности. Потери ретиналя в цикле должны восполняться за счет поступления в организм ретинола с пищей. При дефиците витамина А наблюдается нарушение темно-вой фазы цикла - восстановления родопсина. Развивается дегенерация наружных сегментов палочек.
Глубокий дефицит витамина А может оказывать влияние на цветоощущение, так как он входит и в состав йодопсинов (светочувствительных пигментов колбочек, отвечающих за цветовое
зрение). Дефицит витамина А вызывает нарушение синтеза хондроитинсульфата, влияющее на формирование соединительной ткани, в том числе костной, из-за увеличения распада фосфо-аденозинфосфосульфата под действием лизосо-мальных сульфатаз, подавляемых ретиноидами.
В условиях гиповитаминоза А замедляется синтез гликопротеинов, нарушается рецепторный состав клеточных поверхностей, выработка гормонов, секретов, разрыхляется гликокаликс, нарушается структура межклеточного вещества, снижаются адгезивные свойства клеток. В клетках тормозится синтез РНК, падает активность ферментов, обеспечивающих защиту липидов от окисления. При недостатке витамина А вследствие нехватки ростовых факторов и медиаторов задерживается пролиферация эпителиальных и мезенхимных клеточных популяций, возможно, провоцируется апоптоз. Развивается функциональная неполноценность железистых эпи-телиев с их метаплазией. Страдает иммунитет, сперматогенез прекращается на стадии мейоза.
Дефицит витамина А ведет к нарушению про-тивосвертывающих механизмов крови (рост толерантности плазмы к гепарину, гиперфибрино-генемия).
У новорожденных детей практически нет запасов витамина А, поэтому при отсутствии его в диете быстро развивается авитаминоз с соответствующим симптомокомплексом, вплоть до летального исхода.
Вторичный гиповитаминоз Авозможен при печеночной недостаточности, так как в клетках печени ретинолэстераза освобождает ретинол, который транспортируется в крови в связанном с белком состоянии; при протеинурии - вследствие потери ретинолсвязывающего белка; при алкоголизме - вследствие недостатка цинка и ниацина, необходимых для метаболизма витамина А, а также нарушения всасывания ретино-
Рис. 73. Механизм нарушения сумеречного зрения при гиповитаминозе А
Часть ||. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ
ла из-за алкогольной мальабсорбции. Нарушение превращения провитаминов в витамин А с развитием каротинемической псевдожелтухи может возникать при гипотиреозе, так как активность р-каротиндиоксигеназы (фермента, превращающего (3-каротин в ретиналь) стимулируется гормонами щитовидной железы.
Недостаточность витамина А может развиваться при врожденном нарушении превращения Р-каротина в ретиналь, связанном с генетическим дефектом Р-каротиндиоксигеназы.
Генетический дефект, при котором увеличивается потребность в витамине А для поддержания нормального состояния эпителиальной ткани, лежит в основе фолликулярного кератоза Дарье. Наряду с изменениями кожи и слизистой оболочки полости рта у больных с данной патологией отмечаются отставание умственного развития и психозы.
Поступление в организм больших доз витамина А, превышающих во много раз физиологическую потребность, вызывает характерную картину интоксикации, известную под названием гипервитаминоза А. В клинической картине острой формы отравления у животных, часто заканчивающейся смертью, преобладают судороги и параличи. Хроническая форма характеризуется остановкой роста, потерей массы тела, спонтанными переломами длинных трубчатых костей (вследствие торможения остеогенеза и активации хондролитических процессов), кровоизлияниями во внутренние органы, дегенеративными изменениями эндокринных желез, печени, селезенки.
Гипервитаминоз А у человека может возникнуть в результате употребления продуктов, содержащих большое количество витамина А, либо токсических доз препаратов витамина А (50 тыс. ME в сутки при продолжительном применении или 1 - 6 млн ME однократно). Острый гипервитаминоз А чаще всего выражается в головокружении, тяжелой головной боли, сонливости, ступоре, диспепсических явлениях (понос, рвота), шелушении кожи. Хроническое отравление витамином А влечет за собой головную боль, сухой дерматит, выпадение волос, боль в суставах и костях при ходьбе и надавливании, отек вдоль трубчатых костей, повышенную ломкость костей, кальциноз связок, анорексию, потерю массы тела, гепатоспленомегалию, геморрагический синдром. Нередко наблюдаются симптомы экзо-фтальмии и повышения давления спинномозго-
вой жидкости, отек соска зрительного нерва, связанный с развитием ликворной гипертензии и сдавлением нервов в отверстиях костей черепа. Высокие дозы витамина А эмбриотоксичны. На фоне гипервитаминоза А, наряду с активацией фибринолиза (ретинол стимулирует продукцию активатора плазминогена клетками эндотелия), сопровождаемой гипофибриногенемией, проявляется рост антитромбиновой активности.
При гипервитаминозе А в клетках нарушаются окислительно-восстановительные реакции, ускоряются процессы гликозилирования, в ли-пидном слое мембран, изменяющих свои физико-химические свойства, появляются участки, обогащенные витамином А, гипертрофируется комплекс Гольджи, разрушаются мембраны митохондрий, цитоплазматического ретикулума, нарушается структура гликокаликса и межклеточных контактов. Клетки разобщаются, усиливается фагоцитоз. Развиваются слизистая метаплазия ороговевающих эпителиев, нарушение зрения, генерализованное аутоиммунное воспаление, дегенеративные изменения многих органов и систем (некроз гепатоцитов и клеток почечного канальцевого эпителия, фиброз печени).
Как гипо-, так и гипервитаминоз А сопровождаются активацией свободнорадикальных процессов, поскольку ретинол в гидрофобной области мембран клеток выполняет роль етерическо-го регулятора, определяющего доступность ненасыщенных жирных кислот, которые входят в состав фосфолипидов, для окисления.
Витамин А содержится в основном в продуктах животного происхождения (печень, цельное молоко, сливки, сметана, сливочное масло, сыр). Особенно богаты им печень и внутренний жир некоторых видов рыб (палтус, треска) и морского зверя (киты, моржи, тюлени, дельфины), белого медведя. Основным пищевым источником каротинов (провитаминов А) являются продукты растительного происхождения - морковь, красный перец, томаты, зелень петрушки, салат, шпинат, щавель, облепиха, шиповник и др. Суточная потребность в витамине А для взрослого человека - 1,5-3,0 мг, или 2-5 мг Р-каротина; для детей выше, чем для взрослых. Повышается при беременности, лактации, утомлении, продолжительном напряжении зрения.
Витамины группы D
Витамин D (кальциферол) - антирахитический фактор, его открытие связано с поисками
Глава 11 / ПАТОФИЗИОЛОГИЯ ТИПОВЫХ НАРУШЕНИИ ОБМЕНА ВЕЩЕСТВ
лечебного препарата для профилактики и лечения рахита. Основным источником витамина D является эндогенный синтез: до 80% необходимого количества витамина D3 (холекальциферо-ла) организм может синтезировать в коже (в макрофагальных клетках дермы) под воздействием ультрафиолетовых лучей из 7-дегидрохолес-терина (провитамина D3). В растениях и дрожжах содержится эргостерин (провитамин D2) -предшественник эргокальциферола (витамина
D2).
|
Дефицит кальциферола,часто проявляющийся у людей в современных условиях, неразрывно связан с образом жизни значительной части населения - скоплением людей в больших городах, сокращением времени пребывания на свежем воздухе. Уменьшение содержания витамина D в организме наблюдается при недостаточном поступлении его с продуктами питания при одновременном снижении эндогенного синтеза. Велика вероятность развития гиповитаминоза D у недоношенных детей, так как женское молоко содержит недостаточное его количество, а через плаценту витамин поступает в основном впоследнем триместре беременности. Эндогенный гипо- и авитаминоз D может возникать при нарушении переваривания и (или) всасывания
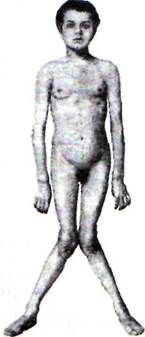
Рис. 74. Поздний рахит (по R. Berg, 1927)
липидов, в том числе жирорастворимых витаминов (механическая желтуха, холестаз, панкреатическая недостаточность); нарушении образования активных форм витамина: гидроксили-рования в печени (при циррозе) и в почках (при хронической почечной недостаточности); усилении распада (например, под влиянием ряда лекарственных препаратов, индуцирующих активность ферментов системы микросомального окисления при участии цитохрома Р450).
Уменьшение синтезаи/или поступления витамина D с пищей, нарушения метаболизма холекальциферолавызывают «кальципеничес-кий» рахит у детейи остеомаляцию у взрослых.Нарушения фосфорно-кальциевого обмена, играющие главную роль в патогенезе рахита, приводят к нарушению минерализации костной ткани, особенно в зонах роста трубчатых и черепных костей. Помимо нарушения минерализации остеоида, при рахите наблюдаются усиленное рассасывание костной ткани, вымывание кальция и фосфата из кости, потеря фосфата с мочой, что обусловлено гиперсекрецией парат-гормона (развитие вторичного гиперпаратирео-за), стимулируемой низким уровнем кальция в крови. Ухудшение энергообеспечения процессов костеобразования и минерализации костной ткани связано с нарушением всасывания и метаболизма цитрата при недостатке витамина D. Рахитические кости медленнее растут, не способны выдерживать нормальную статическую и динамическую нагрузки, легко подвергаются механическим деформациям, что обусловливает внешние проявления рахита со стороны скелета: искривление нижних конечностей, рук и позвоночника, утолщение эпифизов длинных трубчатых костей («рахитические браслеты»), «рахитические четки» на грудных концах ребер, «куриная грудь» с выступающей грудиной и сдавленными с боков ребрами, задержка закрытия родничков и прорезывания зубов, «лоб Сократа» (периостальные наслоения остеоида в области лобных и теменных бугров), краниота-бес (уплощение затылочных костей) (рис. 74,75). К ранним клиническим проявлениям рахита относятся раздражительность, мышечная гипотония (связанная не только с изменением нервной регуляции, но и с нарушением структуры и метаболизма мышечных волокон), тетания (в связи с системной гипокальциемией), облысение затылка, развитие бронхолегочных заболеваний,
Часть II. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ
Метаболизм и функции витамина D3
Схема 18
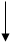 7-дегидрохолестерин
7-дегидрохолестерин
Кожа (облучение ультрафиолетом)
Холекальциферол (D3)
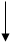 Печень (25-гидроксилаза)
Печень (25-гидроксилаза)
25-гидроксихолекальциферол (25-OHD,)
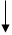 Почки (1а-гидроксилаза)
Почки (1а-гидроксилаза)
 |  | ||||||||
 |  | ||||||||
 |
| Влияние на органы, снабженные рецепторами к кальцитриолу |
| Регуляция мобилизации кальция и фосфатов из костной ткани |
 Регуляция процессов всасывания кальция и фосфатов в кишечнике
Регуляция процессов всасывания кальция и фосфатов в кишечнике
1,25-дигидроксихолекальциферол (1,25-(OH),D3 - кальцитриол)
 | |||
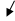 | |||
Регуляция реабсорбции
кальция и фосфатов в
почечных канальцах
связанное с ухудшением вентиляции легких и снижением иммунитета.
Недостаток витамина D у взрослых вызывает нарушение периостального окостенения (ос-теоид вырабатывается, но не минерализуется) -развивается остеомаляция. У больных отмечаются гипоцитратемия, гипофосфатемия, в тяжелых случаях - гипокальциемия, развивается ги-перпаратиреоз. При развитии злокачественных новообразований остеомаляция может быть связана с торможением образования кальцитриола

Ш\ it
Рис. 75. Тяжелый рахит у ребенка 2 лет, рядом
здоровый ребенок того же возраста (по R. Berg,
1927)
в почках пептидными факторами, синтезированными в опухолевых тканях.
Физиологически активной формой является не сам витамин D, а его метаболиты (в настоящее время их известно более 40 - 25-OHD , la,25-(OH)2D3, 24,25-(OH)2D,, 25,26-(OH)2D,, l,24,25-(OH)3D3 и др.), образующиеся в результате обменных превращений в тканях. Образование кальцитриола (1,25-дигидроксихолекаль-циферол [l,25-(OH)2D3]), поддерживающего уровень кальция и фосфора в сыворотке крови в узких физиологических границах, происходит в организме в несколько этапов. Фотохимически синтезированный в коже витамин D3 под воздействием гидроксилаз подвергается двум реакциям гидроксилирования: сначала в печени в 25-м положении (25-гидроксилаза), затем в почках в 1-м положении (1а-гидроксилаза) (схема 18). Образование активной формы витамина D3 в почках контролируется через систему обратных связей с обменом Са, Р, секрецией парати-реоидного гормона, кальцитонина, соматостати-на, пролактина, половых гормонов и инсулина. Избыток l,25-(OH)2D3 в организме ингибирует его образование.
Дефицит витамина D ведет к понижению концентрации кальция и фосфора в сыворотке крови и нарушениям деятельности многих систем организма: нервной, мышечной, костной, репродуктивной, иммунной. Регулирующий эффект витамина D в отношении кальций-фосфорного
Глава 11 / ПАТОФИЗИОЛОГИЯ ТИПОВЫХ НАРУШЕНИЙ ОБМЕНА ВЕЩЕСТВ
17 Зин №. 532
обмена достигается за счет воздействия кальци-триола на следующие процессы: реабсорбцию кальция и фосфатов в почечных канальцах, мобилизацию элементов из костной ткани, всасывание Са2* и фосфатов в кишечнике (наиболее весомый вклад в антирахитическое действие). В клетках кишечника под влиянием кальцитрио-ла происходит синтез Са-связывающего белка (кальбиндин, или холекальцин) и стимуляция транспорта Са2*. Остеогенез и ремоделирование костной ткани регулируются 24,25-(OH)2D3. Рецепторы к l,25-(OH)2D3 обнаружены, помимо органов-мишеней, таких как кишечник, костная ткань, почки, и в ряде других органов и тканей: коже, мозге, гипофизе, половых, молочных, паращитовидных железах и др. Биологические эффекты кальцитриола реализуются через взаимодействие его с рецепторами в ядре клеток, следствием чего является избирательная стимуляция процесса транскрипции ДНК, приводящая к синтезу молекул матричной РНК и трансляции кальцийсвязывающих белков и гормонов, регулирующих обмен Са2*. Витамин D не только влияет на процессы, непосредственно связанные с минеральным обменом, но также регулирует пролиферацию и дифференцировку различных типов клеток, в том числе клеток иммунной системы (макрофаги, Т- иВ-лимфоци-ты). Активированные цитокинами макрофаги могут синтезировать кальцитриол, который усиливает их способность к завершению фагоцитоза.
Избыток витамина D, к которому особенно чувствительны дети, оказывает токсическое действие на организм. К наиболее вероятным причинам гипервитаминоза Dотносятся: продолжительная передозировка или однократный прием токсической дозы витамина, активация почечного (при первичном гиперпаратиреозе) и внепочечного синтеза l,25-(OH)2D3 (в цитокинак-тивированных макрофагах при саркоидозе). Ги-первитаминоз D проявляется глубокими нарушениями гомеостаза Са2+ и фосфатов, которые не способны корректироваться нейрогумораль-ными системами организма. При избытке витамина D развивается усиленная резорбция костной ткани, которая не сопровождается соответствующей реутилизацией минеральных веществ, так как подавлены процесс образования кости и ее минерализация, что не связано с влиянием паратиреоидного гормона (при гипервитаминозе активность паращитовидных желез снижена).
Остеопения, которая развивается в этих условиях, является результатом торможения дифферен-цировки хондроцитов, дефицита остеобластов и остеонекроза, приводящего к дезинтеграции комплекса органического матрикса и минерального компонента. Развиваются гиперкальциемия, ги-перкальциурия, отмечаются отложения труднорастворимых солей (почечные конкременты, кальцификация почек, а также кровеносных сосудов, печени, легких, сердечной мышцы, стенок кишечника, приводящая к тяжелому и стойкому нарушению функций этих органов), снижение активности щитовидной железы и гонад, мышечная ригидность, гипертензия. Наблюдаются также неспецифические симптомы отравления: тошнота, диарея, потеря аппетита, головная боль, слабость. У детей гипервитаминоз D вызывает раннее зарастание родничков (с возможным формированием микроцефалии), прекращение роста скелета в длину, утолщение ди-афизов и эпифизов. Летальный исход при тяжелом гипервитаминозе D может быть вызван почечной недостаточностью, сдавлением мозга, ацидозом и гиперкальциемическими аритмиями.
В эксперименте показано, что избыток витамина D и его метаболитов может оказывать прямое повреждающее действие на мембраны клеток, усиливая в них процессы перекисного окисления липидов.
К наследственным нарушениям обмена и функций витамина D относятся витамин D-зависи-мый наследственный рахит I типа (дефект почечной lct-гидроксилазы) и витамин D-зависи-мый наследственный рахит II типа (дефект тканевых рецепторов кальцитриола).
Наибольшее количество витамина D3 содержится в продуктах животного происхождения -сливочном масле, желтке яиц, печени, рыбьем жире. Из растительных продуктов наиболее богаты витамином D2 растительные масла (подсолнечное, оливковое и др.). Суточная потребность в витамине D для взрослых - 10 - 25 мкг.
Витамины группы Е
Важнейшие проявления недостаточности витаминов группы Е(токоферолы, антистерильный фактор, витамин размножения) у экспериментальных животных (крысы, кролики, собаки, кошки и др.) - нарушения эмбриогенеза и дегенеративные изменения репродуктивных органов, приводящие к стерильности. У самок процесс оплодотворения яйца не нарушен, но раз-
Часть II. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ
вивающиеся патологические изменения в матке, дегенерация эмбриональной сосудистой системы приводят к внутриутробной гибели плода. У самцов происходит атрофия семенников с дегенерацией сперматогенных клеток, приводящая к полной или частичной стерильности. Наряду с этим отмечаются дистрофия скелетных и гладких мышц, миокарда (фрагментация мышечных волокон, микронекрозы, деструкция митохондрий, нарушение образования креатинфосфата); гипотонус, резкое органичение подвижности животных; жировое перерождение печени; эн-цефаломаляция, демиелинизация и глиоз в спинном мозге, атаксия, гипорефлексия, дизартрия, параличи конечностей.
Витамин Е депонируется в организме, поэтому признаки его недостаточности у человека обнаруживаются редко, за исключением населения тех стран, где растительные жиры (основные источники витамина в пище человека) почти не используются для питания. Уменьшение содержания витамина Е в сыворотке крови отмечается при недостаточности питания, нарушении всасывания (муковисцидоз, атрезия желчных протоков, стеаторея и др.), анемии при кваши-оркоре, гемолитической анемии у недоношенных, абеталипопротеинемии, отравлении некоторыми химическими веществами (например, акронитрилом), лучевом поражении, хронической ишемической болезни сердца, злокачественных новообразованиях, туберкулезе легких, неспецифических воспалительных процессах в легких, ожоговой болезни, язвенной болезни желудка и двенадцатиперстной кишки, проведении химиотерапии (стрептомицином, тубазидом).
Основная функция токоферолов, наиболее активных природных жирорастворимых антиок-сидантов, - регуляция интенсивности свободно-радикальных реакций в клетках, выражающаяся в ограничении скорости процессов перекис -ного окисления ненасыщенных жирных кислот в липидах биологических мембран. Токоферолы являются синергистами селена, как кофактора глутатионпероксидазы, участвующей в нейтрализации гидроперекисей липидов. Витамин Е защищает от перекисного окисления ненасыщенную боковую цепь витамина А, повышая его биологическую активность, восстанавливает ко-энзим Q, принимающий участие в окислительном фосфорилировании, регулирует активность фосфолипазы А2, участвующей в метаболизме арахидоновой кислоты - предшественницы про-
стагландинов и лейкотриенов. Регуляцию биосинтеза ферментов витамин Е осуществляет, возможно, на уровне транскрипции матричных РНК.
Витамин Е, являясь антиоксидантом, стабилизирует клеточные мембраны и обеспечивает нормальное течение биохимических процессов, поэтому недостаточное содержание токофероловв организме приводит к формированию различных проявлений так называемой мембранной патологии.Токоферолы реагируют с активными формами кислорода (гася центры инициации свободнорадикальных процессов), свободными радикалами ненасыщенных жирных кислот и их перекисями, обезвреживая их (обрывая уже инициированную цепную реакцию ПОЛ или замедляя ее), свободными жирными кислотами, повышение содержания которых рассматривается как патогенетический механизм повреждения клеточных структур, в частности скелетных и сердечной мышц. Мембраностабилизирующее действие токоферолов обусловлено также их способностью предохранять от окисления SH-rpyn-пы мембранных белков, в том числе ферментов, и образовывать в качестве структурного компонента мембран гидрофобные комплексы с ненасыщенными жирными кислотами, защищая мембраны от окисления.
Недостаточность токоферолов проявляется разнообразными симптомами, связанными со структурно-функциональными нарушениями мембран: гемолитическая анемия у недоношенных детей, атрофия семенников и бесплодие, рассасывание плода на ранних сроках беременности, мышечная дистрофия, развитие морфологических изменений в клетках паренхиматозных и эндокринных органов, сопровождающихся нарушением их функций (гибель клеток слизистой оболочки кишечника, появление участков некроза в печени, ткани мозга, особенно мозжечка, щитовидной железе и др.). При недостатке витамина Е наиболее выраженно повреждаются клетки быстро пролиферирующих тканей (зародышевые ткани, гемопоэтические клетки, сперматогенный эпителий, гепатоциты, слизистая оболочка кишечника, эндокринные органы), в которых осуществляется интенсивный мембраногенез, сопровождающийся снижением антиоксидантных резервов, а также клетки, в которых интенсивно образуются активные формы кислорода (нейроны и миоциты). Непосредственная причина мышечной дистрофии - выс-
Глава 11 / ПАТОФИЗИОЛОГИЯ ТИПОВЫХ НАРУШЕНИЙ ОБМЕНА ВЕЩЕСТВ
вобождение лизосомальных гидролаз, связанное, возможно, с нарушением обмена полиненасыщенных жирных кислот в лизосомальных мембранах.
Недостаток витамина Е сопровождается снижением содержания иммуноглобулина Е и количества Т- и В-лимфоцитов в периферической крови. Токоферолы участвуют в синтезе нуклеиновых кислот, гема микросомальных цитохро-мов и других гемсодержащих белков. При недостаточности витамина Е происходит снижение интенсивности тканевого дыхания, что объясняется влиянием а-токоферола на синтез убихино-на и его участием в предохранении сульфгид-рильных групп белков от окисления. При дефиците витамина Е снижается активность ферментных систем, функционально связанных с мембранами клеток, содержание в тканях креатин-фосфата и АТФ. Дефицит токоферолов сопровождается нарушением образования тромбоксанов и простациклинов (за счет торможения накапливающимися перекисями активности простаглан-динсинтазы) и снижением кальцийтранспорти-рующей способности микросомальной фракции клеток.
Гиповитаминоз Е возможен при наследственной абеталипопротеинемии в связи с нарушением транспорта витамина.
Симптомы гипервитаминоза Е у животных сходны с симптомами гиповитаминоза Е (поражение скелетных мышц, семенников, размягчение мозга). Ранние признаки интоксикации витамином Е у человека - резкое повышение содержания его в сыворотке крови и преходящая креатинурия. При значительной передозировке витамина наблюдаются замедление активации протромбиназы, тромбоцитопатии, гипокоагуля-ция, геморрагии, гипогликемия, диспепсия, головная боль, слабость, повышенная мышечная утомляемость, мышечные судороги. Избыток токоферолов может активировать ПОЛ, так как эти соединения способны образовывать свободные радикалы.
Источниками витамина Е для человека являются растительные масла (подсолнечное, хлопковое, кукурузное и др.), а также салат, капуста и семена злаков; из продуктов животного происхождения витамин Е содержится в мясе, сливочном масле, яичном желтке и др. Суточная потребность в витамине Е составляет около 5 мг.
Витамины группы К
К витаминам группы К (нафтохиноны, антигеморрагический фактор) относятся витамины К, (филлохинон) и К2 (менахинон). Активные метаболиты нафтохинонов, возможно, представляют собой их гидрохиноновые производные.
Авитаминоз Ку человека встречается нечасто, так как смешанная пища довольно богата витамином, который, кроме того, синтезируется микрофлорой кишечника. Витамин К-дефицит-ные состояния могут быть вызваны подавлением кишечной микрофлоры антибиотиками и сульфаниламидами, недостаточным поступлением витамина с пищей, нарушением всасывания жиров, в том числе жирорастворимых витаминов (энтерит, недостаток желчи при циррозе, механической желтухе), а также нерациональным лечением тромбозов и эмболии антикоагулянтами кумаринового ряда, являющимися антивитаминами К.
К-витаминная недостаточность проявляется снижением содержания в крови активных факторов свертывания крови II (протромбин), VII (проконвертин), IX (фактор Кристмаса) и X (фактор Стюарта - Прауэра), вследствие чего удлиняется время свертывания крови, тромбопластино-вое и протромбиновое время, снижается протром-биновый индекс, в плазме накапливаются некар-боксилированные предшественники факторов свертывания. При снижении протромбинового индекса ниже 35% развиваются геморрагические явления вплоть до обильных кровотечений, в первую очередь в областях тела, подвергшихся травмам (операционные раны, ушибы, гематомы в области пункции вен и т.п.), а также самопроизвольные паренхиматозные и капиллярные кровотечения. При более глубокой гипопро-тромбинемии развивается тяжелый геморрагический диатез с гематурией, наличием крови в рвотных массах, гематомами в различных областях тела, гемартрозом и т.д. Недостаточность витамина К у недоношенных детей, особенно подвергшихся асфиксии в родах, проявляется кровоизлияниями в желудочно-кишечном тракте, меленой, носовыми и небными кровотечениями, кровотечениями из культи пуповины. Без лечения погибает около 30% заболевших. При летальных исходах обнаруживают кровоизлияния в надпочечниках, печени, мозге, легких и других органах. Низкое содержание витамин К-зависимых факторов свертывания у новорож-
Часть II. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ
денных связано с отсутствием в первую неделю жизни в кишечнике микрофлоры, небольшим запасом витамина в печени и недостаточным содержанием витамина К в женском молоке.
Витамин К принимает участие в посттрансляционной модификации в печени белков, участвующих в сложном процессе свертывания крови: факторов И, VII, IX и X, что обеспечивает их физиологическую активность, а также влияет на состояние эндотелия кровеносных сосудов. Посттрансляционная модификация белков свертывания крови, требующая наличия витамина К, заключается в у-карбоксилировании остатков глутаминовой кислоты в их молекулах при участии у-глутамилкарбоксилазы. Витамин К функционирует в качестве кофактора карбоксили-рования. Предположительно его роль сводится либо к транспорту ионов НС03", включающихся в у-положение остатков глутаминовой кислоты, либо к активации водорода у-углеродного атома глутаминовой кислоты, либо к активации у-глутамилкарбоксилазы. Постсинтетическое карбок-силирование остатков глутаминовой кислоты необходимо для оптимального связывания факторами свертывания крови ионов Ca2t, посредством которого осуществляется прикрепление Зелков к полианионным поверхностям, что дает им возможность выполнять прокоагулянтные функции. Витамин К участвует также в карбок-силировании неколлагеновых белков костей, почечных белков, антитромботических белков С и S. Витамин К необходим для кальцификации . гтеоидной матрицы. Витамин К-зависимые Са~' -связывающие белки участвуют в почечной реаб-сорбции Ca2t. Дефицит витамина К может вызывать изменение агрегационной активности эритроцитов, связанное с дестабилизацией эрит-роцитарных мембран.
Повышенная дозировка витаминов К1 и К., вызывает у животных снижение концентрации гемоглобина и количества эритроцитов и в 1,5 -2 раза повышает содержание протромбина в крови; у людей обнаружено преходящее повышение свертывания крови. Гемолиз эритроцитов связан с повышением содержания метгемогло-5ина. Передозировка витамина К у новорожденных (и особенно недоношенных) детей может вызвать гемолитическую анемию, гепатоцеллю-иврное поражение и ядерную желтуху вследствие ■овышенного содержания билирубина в крови. Водорастворимые аналоги витамина К при пере-
дозировке вызывают гемолитическую анемию и поражение печени.
К растительным продуктам, богатым витамином К, относятся капуста, шпинат, салат, тыква, зеленые томаты, арахисовое масло, ягоды рябины и т.д. В животных продуктах, кроме печени свиньи, он почти нигде не содержится. Суточная потребность в витамине К точно не установлена, поскольку он синтезируется микроорганизмами кишечника (до 1,5 мг в сутки); считается достаточным количество 1 мг.
11.3.2. Водорастворимые витамины Витамин С
Необходимым пищевым фактором для человека, обезьян, морских свинок, некоторых птиц и рыб является витамин С (аскорбиновая кислота, антискорбутный, антицинготный фактор), отсутствие которого в рационе в течение даже короткого периода времени приводит к тяжелым последствиям для организма. Все другие животные не нуждаются в пищевом витамине С, поскольку у них он синтезируется в печени из глюкозы.
Аскорбиновая кислота активно всасывается в тощей кишке, формы гиповитаминоза С, вызванные нарушением ее абсорбции, неизвестны. Недостаточное поступление в организм витамина С вызывает развитие скорбута, цинги -болезни, сопутствующей человечеству на протяжении всей его истории.
К основным симптомам С-витаминной недостаточности относятся: ломкость кровеносных сосудов, общая слабость, апатия, повышенная утомляемость; снижение аппетита, задержка роста; восприимчивость к инфекциям,, анемия; ослабление фиксации зубов в лунках, геморрагический парадонтит с гингивитом. При тяжелой цинге развивается некротический процесс в области зева, мягкого неба, пищевода, челюстных костей. Поражения кровеносных сосудов служат причиной мелких точечных кровоизлияний под кожу (петехий), сопровождающихся перифолликулярным гиперкератозом с характерными папулами, имеющими кровяной венчик. Крупные подкожные экхимозы при тяжелой цинге могут изъязвляться. Отмечаются кровотечения и кровоизлияния в слизистых и серозных оболочках и внутренних органах, кровоизлияния в толщу мышц (преимущественно икроножных и бедра), в оболочки периферических
Глава 11 / ПАТОФИЗИОЛОГИЯ ТИПОВЫХ НАРУШЕНИЙ ОБМЕНА ВЕЩЕСТВ
нервов, между фасциями и вокруг сухожильных влагалищ. Ослабевает прикрепление надкостницы к костям, наблюдаются поднадкостничные кровоизлияния, субпериостальные переломы, серозный и серозно-геморрагический выпот в суставы, преимущественно коленные. Развиваются одышка, сердцебиение, ослабление сердечного толчка, увеличение поперечника сердца. Возможны увеличение селезенки, жировая инфильтрация печени. Угнетена моторная и секреторная деятельность желудка и кишечника. Терминальная стадия скорбута сопровождается кахексией, контрактурами, внутричерепными кровоизлияниями, возможен летальный исход.
У детей раннего возраста скорбут проявляется в виде болезни Меллера - Барлоу.Нарушение остеогенеза приводит к деформации грудной клетки с образованием болезненных цинготных «четок» в местах перехода хрящевой части ребра в костную, искривлению трубчатых костей нижних конечностей. В тяжелых случаях отмечаются геморрагический выпот в полости голеностопных и коленных суставов, отек голеней. Наблюдаются длительный субфебрилитет, болезненность конечностей при движении, при-пухание диафизов, отслойка надкостницы с под-надкостничными гематомами, позже обызвеств-ляющимися. Изменения в костях и кровоизлияния в костный мозг приводят к нарушению ге-мопоэза.
Витамин С участвует в реакциях гидрокси-лирования триптофана (синтез серотонина), ди-оксифенилаланина (образование норадреналина), оксифенилпирувата (синтез гомогентизиновой кислоты), стероидов (синтез кортикостероидов), Р-бутиробетаина (синтез карнитина). Активируя пролилгидроксилазу и лизилгидроксилазу, он обеспечивает гидроксилирование остатков пролива и лизина в проколлагене (образование коллагена). Кроме того, аскорбиновая кислота участвует в обмене железа, обеспечивая переход трехвалентного железа в двухвалентное в кишечнике и тем самым облегчая его всасывание, а также высвобождая железо из трансферрина в крови, что ускоряет его поступление в ткани. Аскорбиновая и дегидроаскорбиновая кислоты, составляя окислительно-восстановительную систему, участвуют в окислительно-восстановительных реакциях. Витамин С в зависимости от дозы может выступать в роли антиоксиданта или про-оксиданта. Антиокислительные эффекты витамина проявляются нейтрализацией активных
кислородсодержащих радикалов, реактивацией витамина Е, предохранением от окисления SH-групп белков, в том числе ферментов. Аскорбиновая кислота принимает участие в окислительном распаде тирозина и гемоглобина, активации гексокиназы.
Геморрагические явления и специфические изменения в костной и хрящевой тканях при недостаточности витамина С вызваны нарушениями постсинтетической модификации коллагена и изменениями в синтезе гликозаминогли-канов (хондроитинсульфатов и гиалуроновой кислоты). Наиболее сильно поражается коллаген базальных мембран кровеносных сосудов, насыщенный гидроксипролиновыми остатками. Молекулы тропоколлагена, в которых не подверглись гидроксилированию пролиновые и ли-зиновые остатки, не имеют достаточной механической прочности и легко расщепляются кол-лагеназами. Клиническая картина цинги определяется также нарушениями со стороны эндокринной системы (гипофункция надпочечников), иммуной системы (снижение выработки антител лимфоцитами и продукции защитных белков нейтрофилами), усилением распада и торможением синтеза белков, снижением активности гексокиназы. Гипохромная анемия при скорбуте может быть связана со снижением всасывания железа и повышенной кровоточивостью. Гиповитаминоз С сопровождается, как правило, дефицитом витамина Р, что усугубляет нарушения сосудистой проницаемости.
В больших количествах витамин С содержится в продуктах растительного происхождения: перце, салате, капусте, хрене, укропе, ягодах рябины, черной смородины, цитрусовых и т.д. Картофель относится к основным повседневным источникам витамина С. Из непищевых источников витамином С богаты шиповник, хвоя, листья черной смородины, экстракты из которых могут полностью удовлетворить потребность организма. Суточная потребность в витамине С для человека составляет 50 - 100 мг, она возрастает при физической и нервно-психической нагрузке, пребывании в условиях низкой и высокой температуры, при облучении, курении, беременности и лактации, инфекционных заболеваниях, хронических заболеваниях желудочно-кишечного тракта, при приеме антибиотиков и сульфаниламидов.
Часть II. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ
Витамин В1
Авитаминоз В,,проявляющийся заболеванием бери-бери,ранее широко распространенный в странах Дальнего Востока, сейчас встречается значительно реже. Различают несколько клинических типов недостаточности витамина В( (тиамина, антиневритного фактора): сухую (поли-невритную, паралитическую) форму, протекающую с преобладанием неврологических поражений (парезы, параличи) (рис. 76,77); отечную - с преимущественным поражением сердечно-сосудистой системы, хотя явления полиневрита при ней также отмечаются, и остро протекающую кардиальную форму болезни, нередко приводящую к летальному исходу в результате развития острой сердечной недостаточности. Зачастую в клинике наблюдаются частичные взаимопереходы форм заболевания. Бери-бериу человека нередко представляет собой полиавитаминоз, при котором организм испытывает недостаток также в витаминах В2, В6, РР, С и др.
При отсутствии или недостаточности тиамина клинические симптомы преимущественно связаны с нарушениями деятельности нервной и сердечно-сосудистой систем, а также секреторной и моторной функций пищеварительного тракта. Со стороны периферической нервной системы наблюдается симптоматика распространенного дегенеративного демиелинизирующего полиневрита с преимущественными поражениями нервов нижних конечностей, выражающаяся в расстройстве чувствительности и болях по ходу нервов. Возможно развитие контрактур, параличей нижних, а затем и верхних конечностей. Отмечаются изменения в психике: потеря памяти на недавние события, галлюцинации, фобические неврозы, снижение интеллекта. Нарушения деятельности сердечно-сосудистой системы проявляются одышкой, сердцебиением, болями в области сердца, отеками.
Вторичные гиповитаминозы Btмогут возникать в случае повышенного расхода витамина при обычном его поступлении с пищей (тиреотоксикоз, избыток углеводов в диете), а также при нарушении процессов всасывания из желудочно-кишечного тракта, усиленном выведении витамина после длительного применения диуретических средств, ослаблении процессов тканевого фосфорилирования тиамина. Синдром Вер-нике - Корсакова(форма тиаминовой недостаточности, развивающаяся у алкоголиков) харак-
теризуется энцефалопатией Вернике (мозжечковая атаксия, судороги, арефлексия, нистагм, дезориентация, спутанность сознания, паралич глазных мышц) икорсаковским психозом (неспособность усваивать информацию, ретроградная амнезия, дезориентировка во времени и пространстве, слабая способность сосредоточиваться, болтливость, иногда эйфория).
Модель бери-бери была получена на курицах (модель X. Эйкмана), голубях и лисицах (паралич Частека).
|
| Рис. 76. Паралич левой ноги при бери-бери (по R. Berg, 1927) |

|
| Рис. 77. Паралич кисти при бери-бери (по R. Berg, 1927) |
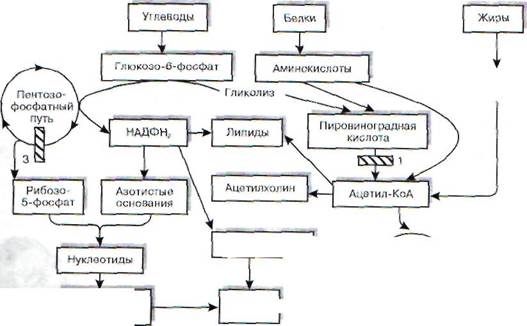
Молекулярной основой обменных нарушений, наблюдаемых при развитии В^гиповитаминоза, является снижение функциональной активности тиаминзависимых ферментов, занимающих ключевое положение в клеточном метаболизме (рис. 78). Тиаминдифосфат (тиаминпирофосфат) - коферментная форма витамина В, - входит в состав пируват- и а-кетоглутаратдегидрогеназ-ных ферментативных комплексов, катализирующих окислительное декарбоксилирование пи-ровиноградной и а-кетоглутаровой кислот. Аце-тил-КоА, образующийся в результате окислительного декарбоксилирования пировиноградной кислоты, либо попадает в цикл трикарбоновых кислот, где происходит его полное окисление с образованием С02, Н20 и АТФ, в том числе в
Глава 11 / ПАТОФИЗИОЛОГИЯ ТИПОВЫХ НАРУШЕНИЙ ОБМЕНА ВЕЩЕСТВ
цепи переноса электронов, либо принимает участие в синтезе холестерина, фосфолипидов, жирных и желчных кислот, ацетилхолина и стероидных гормонов, а-кетоглутаратдегидрогеназный комплекс, катализирующий окислительное де-карбоксилирование а-кетоглутаровой кислоты, является звеном цикла трикарбоновых кислот, обеспечивающего окисление продуктов расщепления белков, жиров и углеводов. Транскетола-за (ключевой фермент пентозофосфатного пути окисления углеводов), в состав которой входит тиаминдифосфат, участвует в переносе гликоль-альдегидного радикала от кетосахаров на альдо-сахара. Нормальное функционирование пентоз-ного цикла, являющегося основным источником НАДФН2 и рибозо-5-фосфата, представляет собой необходимое условие для осуществления биосинтеза нуклеиновых кислот, белков и липидов. Тиаминдифосфат также участвует в окислительном декарбоксилировании а-кетокислот, образующихся из аминокислот с разветвленной боковой цепью, что играет важную роль в процессах катаболизма белка.
Наряду с алиментарной недостаточностью витамина Bj известны заболевания, обусловлен-
ные врожденными нарушениями обмена и функций витамина: подострая некротизирующаг энцефаломиелопатия, или болезнь Лея, при которой нарушено образование коферментной формы витамина в мозговой ткани; перемежающаяся атаксия, обусловленная врожденным дефектом пируватдегидрогеназного ферментативного комплекса; тиаминзависимая форма болезнн «моча с запахом кленового сиропа», связанная с дефектом системы окислительного декарбокси-лирования разветвленных кетокислот.
При авитаминозе В, в крови и тканях происходит накопление а-кетокислот, пентозосахаров, с мочой в повышенных количествах выделяются аминокислоты и креатин. Нарушение окислительного декарбоксилирования приводит к накоплению пирувата и его недоокисленных метаболитов, оказывающих токсическое действие на ЦНС. Развиваются метаболический ацидоз, гипоэнергетические состояния в связи с нарушением метаболизма углеводов, нарушается работа ионных насосов нервных и мышечных к."( ток, в том числе кардиомиоцитов. В связи с ■ что для получения энергии организм начинает использовать больше белков и жиров, нарушж-
| р-окисление жирных кислот |
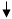

 Аминокислоты | Оксалоацетат цИТрат
Аминокислоты | Оксалоацетат цИТрат
ЦТК 1

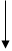 Сукцинил-КоА а-кетоглутарат
Сукцинил-КоА а-кетоглутарат
| Нуклеиновые кислоты |
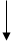
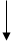
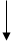 Белки НАДН2
Белки НАДН2
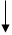 ------------ 2--------- )
------------ 2--------- )
АТФ
Рис. 78. Нарушения синтеза нуклеиновых кислот, белков, липидов, ацетилхолина, образования АТФ при гиповитаминозе В,: 1 - дефицит пируватдегидрогеназы; 2 - дефицит а-кетоглутаратдегидрогеназы; 3 - деф»-1
цит транскетолазы (по В.Б. Спиричеву, 1977)
Часть II. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕСС^
ется синтез жирных кислот, ацетилирование холина, превращение углеводов в жиры, развивается отрицательный азотистый баланс.
В токсичных дозах витамин Bj угнетает ферменты холинэстеразу и гистаминазу, вызывает дегрануляцию тучных клеток и острую аллергическую реакцию. Возможны кровоизлияния в кишечник, отек легких, судороги. Наиболее тяжелая реакция - анафилактический шок с потерей сознания, коллапсом и даже смертельным исходом. Развитие аллергических реакций может быть связано не только с величиной дозы витамина В,, но и с повышенной чувствительностью некоторых людей к тиамину.
Основное количество витамина Вх человек получает с растительной пищей. Много витамина В, содержится в дрожжах, пшеничном хлебе из муки грубого помола, оболочке и зародышах семян хлебных злаков, сое, фасоли, горохе, меньше - в картофеле, моркови, капусте. Из продуктов животного происхождения наиболее богаты витамином В1 печень, почки, мозг. Некоторые бактерии, населяющие кишечник животных, способны синтезировать витамин В,. Норма суточного потребления тиамина для взрослого человека составляет от 1,2 до 2,2 мг.
Витамин В2
Дефицит витамина В2(рибофлавина, витамина роста) может быть вызван как недостаточным поступлением его с пищей, так и нарушением всасывания витамина, связанным с инги-бирующим действием на флавокиназу ряда лекарственных препаратов (адриамицин, антидепрессанты и др.).
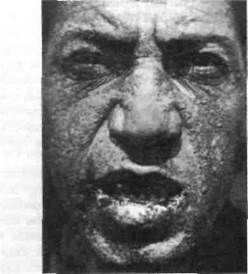
Острый арибофлавиноз,развивающийся при полном отсутствии витамина в пище у человека и животных, характеризуется внезапным развитием коматозного состояния и быстро наступающей гибелью. Недостаток рибофлавина у животных вызывает поражения кожных покровов (облысение, дерматиты с шелушением кожи и появлением эрозий), глаз (кератиты, катаракты), развитие гипохромной анемии. У собак отмечаются нарушение координации движений, а также процессов высшей нервной деятельности со снижением условных и безусловных рефлексов. У человека дефицит рибофлавина проявляется прежде всего хейлозом с мацерацией и трещинами на губах и ангулярным стоматитом (рис. 79). Могут развиваться дерматиты на носогуб-
|
| Рис. 79. Арибофлавиноз. Себорейные поражения кожи, ангулярный стоматит, хейлоз (по В.В. Ефремову, 1944) |
нои складке, крыльях носа, веках и ушах, волосистой части головы, мошонке и других частях тела. Отмечаются глосситы, сопровождающиеся чувством жжения языка, а также поражения глаз (васкуляризация роговой оболочки, блефариты, конъюнктивиты и кератиты); развиваются анемия, нервные расстройства, проявляющиеся мышечной слабостью, жгучими болями в ногах, атаксией, гиперкинезами. Рибофлавин входит в состав флавиновых коферментов (ФМН - флавинмононуклеотид и ФАД - флавинаденин-динуклеотид), являющихся, в свою очередь, про-стетическими группами ряда ферментов, катализирующих реакции дегидрирования исходного субстрата или промежуточного метаболита (ок-сидазы L- и D-аминокислот, глициноксидаза, ксантиноксидаза и др.); а также реакции, характеризующиеся переносом электронов и протонов не от исходного субстрата, а от восстановленных пиридиновых коферментов. Витамин В2, входящий в состав коферментов оксидоредуктаз, принимает участие в процессах окислительного фосфорилирования, окисления альдегидов, моноаминов, пуриновых оснований, углеводов и др. При гипорибофлавинозе вследствие недостатка флавопротеинов страдают в первую очередь высокоаэробные эпителии кожи и полости рта. Дефицит рибофлавина характеризуется снижением интенсивности окислительно-восстановительных превращений ксантина, аминокислот, уг-
Глава 11 / ПАТОФИЗИОЛОГИЯ ТИПОВЫХ НАРУШЕНИЙ ОБМЕНА ВЕЩЕСТВ
нетением ферментов ЦТК, (3-окисления жирных кислот, дыхательной цепи митохондрий. При гиповитаминозе В2 снижается детоксикационная активность оксидаз печени в отношении лекарственных препаратов.
Из пищевых продуктов богаты рибофлавином хлеб (из муки грубого помола), семена злаков, яйца, молоко, мясо, печень, свежие овощи и др. Суточная потребность в витамине В2 составляет 1,7 - 3,0 мг.
Дата добавления: 2015-03-19; просмотров: 3357;
