Дендритная ликвация и ее влияние на свойства сплавов. Можно ли устранить дендритную ликвацию?
Ликвация – неоднородность химического состава сплавов, возникающая при кристаллизации.
Ликвация обусловлена тем, что сплавы, в отличие от чистых металлов, кристаллизуются не при одной температуре, а в интервале температур.При этом состав кристаллов, образующихся в начале затвердевания, может существенно отличаться от состава последних капель кристаллизующегося маточного раствора. Чем шире температурный интервал кристаллизации сплава, тем сильнее развивается ликвация, причем наибольшую склонность к ней проявляют те компоненты сплава, которые наиболее сильно влияют на ширину интервала кристаллизации (для стали – сера, кислород, фосфор, углерод). Ликвация оказывает, как правило, вредное влияние на качество металла.
Дендритная ликвация может быть ослаблена продолжительным нагревом затвердевшего сплава при температурах, обеспечивающих достаточную скорость диффузии (несколько ниже солидуса). После такого нагрева, называемого диффузионным отжигом или гомогенизацией, дендритная структура литого сплава уже не выявляется и сплав состоит из однородных кристаллов твердого раствора.
Диффузионный отжиг – это термическая обработка, при которой главным процессом является устранение последствий дендритной ликвации.
Слитки из углеродистых сталей обычно не подвергают диффузионному отжигу, так как в них при нагреве под горячую обработку давлением из-за быстрой диффузии углерода в аустените дендритная ликвация успевает исчезнуть. Диффузионному отжигу подвергают слитки легированной стали с целью уменьшения дендритной или внутрикристаллитной ликвации, которая повышает склонность стали, обрабатываемой давлением, к хрупкому излому, к анизотропии свойств и возникновению таких дефектов, как шиферность (слоистый излом) и флокены (тонкие; внутренние трещины, наблюдаемые в изломе в виде белых овальных пятен).
Дендритная ликвация понижает пластичность и вязкость легированной стали. Поэтому слитки и крупные отливки нередко подвергают гомогенизирующему или диффузионному отжигу. Нагрев при диффузионном отжиге должен быть до высоких температур 1100-1200°С, так как только в этом случае более полно протекают диффузионные процессы, необходимые для выравнивания в отдельных объемах состава стали. Диффузия наиболее интенсивно протекает в начале выдержки, заметно снижаясь с течением времени. Поэтому во избежание образования большого количества окалины, уменьшения расхода топлива и увеличения производительности печей выдержка должна быть минимальной, обычно 15-20 ч. После выдержки садку охлаждают до 800-820°С в печи, а далее на воздухе.
Во многих случаях для уменьшения дендритной ликвации не проводят специального диффузионного отжига, а выполняют более высокий и длительный нагрев для горячей деформации. В результате диффузионного отжига получается крупное зерно. Этот недостаток устраняется при последующей обработке слитка давлением или в процессе последующей термической обработке.
Диаграмма состояния эвтектического типа для сплавов с частичной растворимостью одного компонента в другом в твердом состоянии. Атомы каких химических элементов образуют диаграммы такого типа? Постройте кривую охлаждения доэвтектического сплава и объясните превращения.
На рис. 19 приведен общий случай диаграммы состояния эвтектического типа, когда компоненты способны растворять друг друга в твердом состоянии до некоторого предела. Здесь линия А'еВ' - линия ликвидуса, линия А'abВ' - линия солидуса. Линия аа0 показывает изменение растворимости компонента В в А с изменением температуры, а линия bb0 - компонента А в В. Эти линии получили название линий предельной растворимости. Точки а и b характеризуют максимальную растворимость компонентов друг в друге в твердом состоянии, а точки а0 и b0 - предельную растворимость при комнатной температуре.
Рис. 19. Диаграмма состояния системы, компоненты которой образуют ограниченные твердые растворы и эвтектику.
Точка e пересечения двух ветвей ликвидуса А'е и B'e называется эвтектической точкой, а горизонталь, на которой лежит эвтектическая точка, - эвтектической горизонталью. Сплав, состав которого соответствует точке е, называют эвтектическим (т.е. легко расплавляющимся). Он кристаллизуется при самой низкой температуре. Сплавы, лежащие слева от эвтектической точки, находящиеся в пределах концентрации точек a и e, называют доэвтектическими, а сплавы, лежащие по другую сторону от нее, в пределах концентрации точек b и e, - заэвтектическими.
Поле диаграммы состоит из нескольких областей. В области Ж сплавы находятся в жидком состоянии, в области α - в состоянии твердого раствора компонента В в компоненте А, в области β - в состоянии твердого раствора компонента А в В. В области Ж+α имеем смесь жидкости с кристаллами α-твердого раствора, в области Ж+β - смесь жидкости с кристаллами β-твердого раствора, а в области α+β - смесь кристаллов двух твердых растворов α и β. Кроме указанных трех однофазных и трех двухфазных областей, на диаграмме имеется трехфазная область. Это эвтектическая горизонталь аb, где одновременно сосуществуют: жидкость состава точки е и твердые растворы α и β, составы которых определяются точками а и b соответственно.
Видно, что фрагменты представленной на рисунке диаграммы в области составов, левее точки a0 и правее точки b0 аналогичны рассмотренной выше диаграмме с неограниченной растворимостью компонентов в твердом и жидком состояниях. Поэтому кристаллизация сплавов в указанных областях составов будет протекать точно также, как и кристаллизация сплавов с полной взаимной растворимостью компонентов. После затвердевания сплавы, лежащие левее точки а0, будут состоять только из кристаллов твердого раствора α, а сплавы, лежащие правее точки b0, - из кристаллов β.
На примере сплава 1 проследим за кристаллизацией сплавов, ординаты которых проходят левее точки а, но правее точки а0. Выше кривой ликвидуса сплав представляет однородную жидкость. В точке l0 на кривой ликвидуса сплав оказывается насыщенным относительно кристаллов α-твердого раствора. При дальнейшем охлаждении из расплава начинают выделяться α-кристаллы, состав которых определяется точкой s0 пересечения горизонтали, проходящей через точку l0, с кривой солидуса. С понижением температуры, вплоть до Т1, составы жидкой и твердой фаз будут непрерывно изменяться в соответствии с линиями ликвидуса (участок l0l1) и солидуса (участок s0s1). Количественное соотношение фаз при той или иной температуре может быть вычислено по упомянутому выше правилу отрезков. При температуре Т1 жидкость полностью затвердевает, а состав α-кристаллов определится точкой s1. При последующем охлаждении до Т2 сплав остается однородным твёрдым раствором. В точке а1 α-твёрдый раствор становится насыщенным компонентом В. При дальнейшем охлаждении из α-твердого раствора начнут выделяться α-кристаллы. Их состав в этот момент будет соответствовать точке b1 на кривой растворимости bb0. Процесс выделения β-кристаллов будет продолжаться с понижением температуры, причем составы α и β фаз будут изменяться: α-кристаллов - по кривой а1а0, β-кристаллов - по кривой b1b0.
Вполне аналогично рассмотренному будет протекать кристаллизация сплавов, ордината которых проходит правее точки b1, но левее точки b0.
При этом с понижением температуры из β-твёрдого раствора начнут выделяться α-кристаллы. Составы α и β фаз будут изменяться согласно линиям предельной растворимости аа0 и bb0.
Рис. 20. К кристаллизации сплавов, ордината которых проходит через эвтектическую горизонталь.
На примере сплава 2 (рис. 20) рассмотрим кристаллизацию доэвтэктических сплавов, ордината которых проходит между точками a и e, т.е. пересекает эвтектическую горизонталь. При охлаждении до кривой ликвидуса (точка l0) в сплаве не происходит фазовых изменений. В интервале от Т0 до эвтектической температуры Те будет протекать двухфазное превращение Ж↔α-твёрдый раствор. В момент достижения температуры Те, состав твёрдого раствора определится точкой a, а жидкости - точкой е. В точке е, являющейся точкой пересечения двух ветвей ликвидуса, сплав становится насыщенным как компонентом А, так и компонентом В.
Следствием этого является одновременное выделение твёрдых растворов α и β. Так начинается трёхфазное эвтектическое превращение Ж↔α+β. Составы участвующих в превращении фаз неизменны и, как уже было отмечено, определяются точками: а - для α-твёрдого раствора, е - для жидкости, b - для β-твердого раствора. Трёхфазное превращение протекает при постоянной температуре и заканчивается в тот момент, когда затвердеет вся жидкость. Теперь сплав будет состоять из двух твёрдых фаз - α и β, между которыми устанавливается двухфазное равновесие α↔β.
При дальнейшем понижении температуры составы α и β-твёрдых растворов будут непрерывно изменяться вдоль кривых аа0 и bb0 соответственно. Из α-твёрдого раствора начнут выделяться β кристаллы, а из β-твёрдого раствора - α-кристаллы. Как видно, процесс будет аналогичен рассмотренному выше при охлаждении сплава 1 ниже точки а1 (рис. 19).
Кристаллизация заэвтектических сплавов, ордината которых проходит между точками е и b, протекает аналогично кристаллизации доэвтектических сплавов, рассмотренных на примере сплава 2. Только ниже линии ликвидуса вместо α-кристаллов выделяются β-кристаллы, из которых при дальнейшем охлаждении согласно кривой bb0 будут выделяться α-кристаллы.
В отличие от кристаллов, выпадающих непосредственно из жидкого расплава до достижения эвтектической температуры и получивших название первичных, кристаллы, выделившиеся из твёрдого раствора, называют вторичными. В рассматриваемом случае их обозначают символами αII и βII.
Из изложенного ясно, что в эвтектическом сплаве, т.е. сплаве 3 (рис. 20), ордината которого проходит через эвтектическую точку е, затвердевание жидкости начинается непосредственно одновременным выделением из нее α и β-твердых растворов. Таким образом, сразу начинается трехфазное превращение Ж↔α+β, за которым следует двухфазное равновесие α↔β. Смесь одновременно закристаллизованных двух твердых растворов α и β называют эвтектической смесью или просто эвтектикой.
Согласно энциклопедическому определению эвтектика - жидкая система, находящаяся в равновесии с твердыми фазами, число которых равно числу компонентов системы. При кристаллизации такой системы образуется механическая смесь твердых фаз того же состава (твердая эвтектика).
Для уяснения особенностей распада фаз α и β, обусловленного понижением температуры и сопровождающегося выделением фаз βII и αII, подчеркнем следующее. При охлаждении доэвтектических сплавов в результате неизбежного распада имеющейся в них β-фазы (заметим: присутствующей в эвтектике и в виде вторичной фазы βII) также образуется и вторичная α-фаза (αII). Эта фаза сливается с окружающими ее зернами первичной фазы α и в виде самостоятельной структурной составляющей в сплавах не наблюдается. Поэтому на диаграмме состояния отмеченная особенность выделения αII не указывается.
То же самое можно сказать и о фазе βII при кристаллизации заэвтектических сплавов.
Рис. 21. Схема структур сплавов 1, 2 и 3 (см. рис.19, 20) при комнатной температуре.
Вторичные кристаллы αII и βII, выделяющиеся из эвтектических составляющих, объединяются с соответствующими фазами эвтектики и поэтому структурно не обнаруживаются.
Структуры некоторых сплавов приведены на рис. 21.
Рассматривая представленную на рис. 19 диаграмму состояния с точки зрения правила фаз, отметим следующие характерные особенности. Очевидно, что трехфазовому превращению Ж↔α+β, т.е. одновременному выделению твердых фаз α и β из раствора Ж, насыщенного обоими компонентами, должны предшествовать двухфазные равновесия Ж↔α и Ж↔β.
Первое из равновесий описывается кривыми А'e и А'а и отвечает выделению из жидкости кристаллов α-твердого раствора. Второе описывается кривыми B'e и B'b и отвечает выделению кристаллов β-твердого раствора. Вариантность превращений Ж↔α и Ж↔β определяется из правила фаз как C=3-2=1. Одна степень свободы указывает на то, что процесс кристаллизации как α-твердого раствора, так и β-твердого раствора будет протекать в интервале температур. До тех пор, пока жидкость насыщена кристаллами только одного вида - α или β, - протекает, соответственно, один из двухфазных процессов.
Как только для составов, расположенных между точками a и b, температура понизится до эвтектической, достигается некоторое новое предельное состояние жидкости: она становится насыщенной одновременно обоими видами кристаллов. Таким образом, в равновесии оказываются три фазы постоянного состава: α- и β- кристаллы, составы которых соответствуют точкам a и b, и жидкость эвтектического состава. Вариантность двухкомпонентной системы, находящейся в трех фазах, равна нулю: C=3-3=0. Поэтому эвтектическое превращение протекает при постоянной температуре.
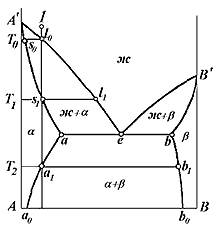
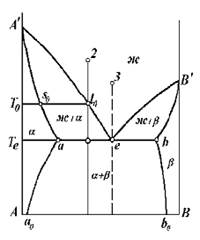
Рис 19 рис 20
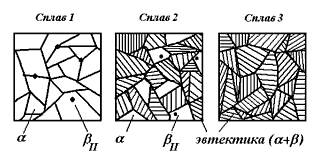 рис 21
рис 21
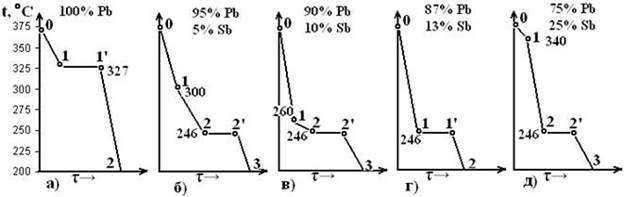
Рассмотрим построение ДС на примере сплава из 2-х взаимнонерастворимых в твердом состоянии компонентов, химически не взаимодействующих, но неограниченно растворимых в жидком состоянии. Таким примером может служить система Pb-Sb. Строим кривые охлаждения для ряда сплавов:
Дата добавления: 2015-03-19; просмотров: 7227;
