Гидроксилсодержащие растворители (ДВС-растворители)
В гидроксилсодержащих растворителях имеют место специфические эффекты. Так, водородные связи в спиртах стабилизируют анионы с локализованным зарядом, например:
R–COO– ··· H–O–R' ; F– ··· H–O–R'; HO– ··· H–O–R'
Метанол и этанол – «водоподобные» растворители
Простая схема равновесий
Шкала pH
Стандартное состояние:
Гипотетический одномолярный или одномоляльный раствор ионов H+ со свойствами бесконечно разбавленного раствора.
Перенос протона осуществляется через молекулу растворителя
В 1-бутаноле неполная диссоциация солей становится уже явной
Это важно, так как используются буферные системы
| Растворитель | 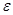
| 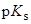
| 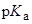 бензойной кислоты бензойной кислоты
| Параметр A в уравнении Дебая–Хюккеля |
| Вода | 78.4 | 14.00 | 4.20 | 0.51 |
| Метанол | 32.7 | 17.2 | 9.40 | 1.89 |
| Этанол | 24.3 | 19.5 | 10.25 | 2.96 |
| 1-Бутанол | 17.4 | 21.6 | 11.5 | 4.88 |
| 2-Метил-2-пропанол | 12.5 | 26.8 | 15.0 | 8.02 |
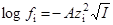
В трет-бутаноле не только выше значения 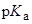 , но и могут возникать такие сложные частицы, которые не характерны для н-спиртов. Так, для HCl и HBr в трет-бутаноле Кольтгоф и Чантуни обнаружили, наряду с обычной диссоциацией, образование более сложных частиц, например: HBr2–, (HBr)2Br– и H2Br+, и аналогично – для HCl.
, но и могут возникать такие сложные частицы, которые не характерны для н-спиртов. Так, для HCl и HBr в трет-бутаноле Кольтгоф и Чантуни обнаружили, наряду с обычной диссоциацией, образование более сложных частиц, например: HBr2–, (HBr)2Br– и H2Br+, и аналогично – для HCl.
Дата добавления: 2014-12-09; просмотров: 1868;
