Равновесия в кислых и основных растворителях
Равновесия в ледяной уксусной кислоте, в фтороводороде, в муравьиной кислоте, в серной кислоте, в пиридине, гидразине и в жидком аммиаке
Здесь наряду с сольватацией важную роль играет и сольволиз
Значения 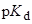 в ледяной уксусной кислоте (
в ледяной уксусной кислоте ( 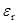 = 6.3,
= 6.3, 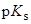 = 14.45) 20-25 оС
= 14.45) 20-25 оС
| Электролит | 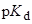
|
| Кислота | |
| Хлорная | 4.9–5.8 * |
| Трифторметансульфоновая | 4.7–5.5 * |
| Бромоводородная | 6.47 |
| Серная (по первой ступени) | 7.25–8.2 * |
| Метансульфоновая | 8.58 |
| пара-Толуолсульфокислота | 8.46–8.89 * |
| Хлороводородная | 8.55–8.85 * |
| Азотная | 9.38 |
| Трихлоруксусная | 11.64 |
| Соль | |
| Ацетат натрия | 6.68 |
| Ацетат аммония | 6.40 |
| Ацетат пиридиния | 6.10 |
| Перхлорат натрия | 5.48 |
| Хлорид калия | 6.88 |
* Разнобой значений, полученных в разные годы различными авторами, связан с как экспериментальными трудностями, так и со сложностью обработки результатов кондуктометрических и потенциометрических измерений.
Сила оснований нивелируется: в большинстве своём они легко превращаются в соответствующие ацетаты (HB+CH3COO–).
Следы воды могут сильно влиять на протекание кислотно-основных процессов в ледяной уксусной кислоте, но следует иметь в виду, что связывание H2O путем введения уксусного ангидрида приводит, например, к превращению серной кислоты в сульфоуксусную, HOOC–CH2–SO2OH, через стадию образования смешанного ангидрида (CH3CO)–O–SO2OH.
В муравьиной кислоте ( 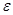 = 56.2,
= 56.2, 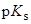 = ) иначе, минеральные кислоты сильно диссоциированы.
= ) иначе, минеральные кислоты сильно диссоциированы.
В жидком HF
Протонирование ароматических углеводородов
РАВНОВЕСИЯ В ЖИДКОМ HF
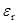 = 83.6 при 0 оС
= 83.6 при 0 оС
2 HF  H2F+ + F–
H2F+ + F–
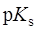
 12
12
Ar + HF  ArH+ + F–
ArH+ + F–
Ar + 2 HF  ArH+ + HF2–
ArH+ + HF2–
C6H6 + HF + BF3  C6H7+ + BF4–
C6H7+ + BF4–
Дата добавления: 2014-12-09; просмотров: 1574;
