Окислення глюкози лугом.
4.3.1.Хід роботи: в пробірку поміщають 4 краплі розчину глюкози і добавляють 2 краплі розчину їдкого натру. Нагрівають суміш до кипіння і кип’ятять 2-3 хв.
4.3.2. Спостереження: розчин жовтіє, а потім коричневіє.
4.3.3. Хімізм реакцій:
4.3.4. Висновок:Пройшла якісна реакція
4.4.Доведення наявності гідроксильних груп в сахарозі. Відсутність відновлюючої здатності у сахарози.
4.4.1. Хід роботи: в пробірку поміщають 1 краплю сахарози , 5 крапель розчину лугу , 4 краплі води і 1 краплю сульфату міді. З’являється синє забарвлення сахарату міді. Розчин сахарату міді нагрівають до кипіння (нагрівають тільки верхню частину).Сахароза в цих умовах не окислюється, що вказує на відсутність в її молекулі альдегідної групи.
4.4.2. Спостереження: з’являється синє забарвлення купром (ІІ) сахарату.
4.4.3. Хімізм реакцій:
4.4.4. Висновок: сахароза в цих умовах не окислюється.
4.5.Кислотний гідроліз сахарози.
4.5.1. Хід роботи: в пробірку поміщають 1 краплю сахарози , 1 краплю 2н HCI, 3 кр. води і обережно нагрівають 20-30 хв. Половину розчину відливають в другу пробірку і добавляють туди 4-5 крапель розчину лугу і 3-4 краплі води. Потім добавляють 1 краплю розчину сульфату міді і нагрівають верхню частину синього р-ну до кипіння. До іншого розчину сахарози (1 пробірка) добавляють кристалик резорцина, 2 краплі HCI (конц.) і нагрівають до кипіння.
4.5.2.Спостереження: з’являється оранжево-жовтий колір.
4.5.3. Хімізм реакцій:
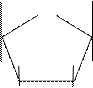
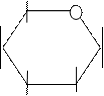

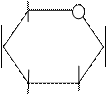 СН2ОН СН2ОН Н СН2ОН СН2ОН ОН
СН2ОН СН2ОН Н СН2ОН СН2ОН ОН
Н Н О Н Н О
Н +НОН Н


 ОН Н О Н ОН ОН Н Н ОН
ОН Н О Н ОН ОН Н Н ОН
НО СН2ОН ОН Н СН2ОН
 Н ОН ОН Н Н ОН ОН Н
Н ОН ОН Н Н ОН ОН Н
4.5.4. Висновок: α – Д глюкоза, β – Д фруктоза.
4.6.Наявність відновлюючої здатності у лактози.
4.6.1. Хід роботи: в пробірку поміщають 1 кр. розчину лактози, 3 кр. розчину лугу і добавляють 1 кр. розчину СuSO4, Добавляють 4-5 краплин води і нагрівають до кипіння.
4.6.2. Спостереження: оранжево-жовте забарвлення.
4.6.3. Хімізм реакцій:
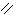
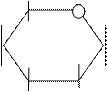 СН2ОН СН2ОН О
СН2ОН СН2ОН О
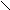
 НО Н С + Сu(OH)2
НО Н С + Сu(OH)2

 Н Н
Н Н
 ОН Н О ОН Н
ОН Н О ОН Н
Н Н Н
 Н ОН Н ОН
Н ОН Н ОН
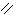
 СН2ОН СН2ОН О
СН2ОН СН2ОН О
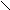
 НО Н С
НО Н С
 Н Н
Н Н
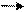
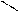 ОН Н О ОН Н
ОН Н О ОН Н
Н Н Н
 Н ОН Н ОН
Н ОН Н ОН
4.6.4. Висновок: Лактоза – відновлюючий дисахарид.
КОНТРОЛЬНІ ЗАПИТАННЯ:
1. Описати хімічні властивості глюкози, фруктози, сахарози, лактози.
2.За допомогою яких реакцій можна відрізнити глюкозу і фруктозу.
3.Які властивості глюкози не можна пояснити її альдегідною формулою?
4.При спиртовому бродінні глюкози виділилось 11,2 м3 вуглекислого газу .Обчислить маси використаної глюкози і одержаного спирту.
5. Скільки можна одержати глюкози з 1т картоплі ,яка містить 22% крохмалю,якщо вихід глюкози становить 80% від теоретичного ?
ЛІТЕРАТУРА :
А.В. Аверина , А.Я, Снегирева "Лабораторный практикум по органической химии" .Гл. 12 . досл.170-174,176,178, 180,181.
Дата добавления: 2014-12-08; просмотров: 1105;
