Основные свойства
Являясь алмазоподобными полупроводниками, соединения типа A2B6 кристаллизуются в структуре цинковой обманки кубического (сфалерит) или гексагонального (вюрцит) типа. Химическая связь носит смешанный ковалентно-ионный характер. По сравнению с полупроводниками типа A3B5 в халькогенидах сильнее выражена ионная составляющая связи, что обусловлено большими различиями в электроотрицательностях элементов, образующих соединение. С ростом средней атомной массы во всех трех гомологичных рядах закономерно уменьшаются ширина запрещенной зоны и температура плавления соединений. Одновременно возрастает подвижность носителей заряда. Из-за увеличения межатомных расстояний прочность химических связей падает при переходе от сульфидов к селенидам и далее – к теллуридам.
Таблица 12.1 Физико-химические свойства соединений А2В6 (при Т = 300 К)
| Соединения | Плотность, г/см3 | Микро-твердость, МПа | Температура плавления, оС | Энергия атомизации, кДж/моль | Ширина запрещенной зоны, эВ | Подвижность носителей тока, м2/(В×с) | |
| электро- нов | дырок | ||||||
| ZnS | 4,08 | 3,67 | 0,014 | 0,0005 | |||
| ZnSe | 5,26 | 2,7 | 0,07 | 0,0028 | |||
| ZnTe | 5,7 | 2,12 | 0,145 | 0,03 | |||
| CdS | 4,82 | ‒ | 2,4 | 0,035 | ‒ | ||
| CdSe | 5,81 | 1,88 | 0,06 | 0,005 | |||
| CdTe | 5,86 | 1,51 | 0,18 | 0,06 | |||
| HgS | 7,73 | ‒ | 1,8 | 0,025 | ‒ | ||
| HgSe | 8,26 | ‒ | 0,2 | 1,8 | ‒ | ||
| HgTe | 8,46 | 0,01 | 2,5 | 0,01 |
В пределах каждой группы соединений-гомологов наблюдается закономерное изменение важнейших свойств в зависимости от роста порядковых номеров компонентов в Периодической системе (табл. 12.1). При переходе от сульфидов к селенидам и теллуридам симбатно температуре плавления уменьшаются энергия атомизации, теплота образования и ширина запрещенной зоны соединений A2B6. Но уменьшение ширины запрещенной зоны, как и в соединениях А3В5, происходит намного быстрее, чем энергии атомизации и других свойств. Это особенно характерно для халькогенидов ртути: если сульфид имеет ширину запрещенной зоны 1,8 эВ, теллурид по существу уже представляет собой полуметалл. В каждой группе соединений-аналогов при переходе от сульфидов к селенидам и теллуридам растет доля ковалентно-металлической связи за счет уменьшения ионной составляющей. В результате четко фиксируется закономерный рост подвижности электронов. Сульфиды, в которых представлена значительная доля ионной связи, характеризуются небольшими подвижностями электронов; теллуриды, наоборот, имеют весьма значительные подвижности носителей вследствие малой степени ионности. Селениды металлов подгруппы цинка занимают промежуточное положение.
При повышенных температурах все соединения A2B6 разлагаются в соответствии с реакцией:
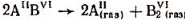
Присутствие в паровой фазе молекул АВ хотя полностью и не исключается, но для большинства соединений их концентрация мала и можно принять, что диссоциация является полной. Равновесное давление паров летучих компонентов сильно зависит от температуры.
Важная особенность полупроводников типа A2B6 состоит в том, что многие из них проявляют электропроводность лишь одного типа независимо от условий получения и характера легирования кристаллов. Проводимость соединений типа A2B6 может быть значительно (на несколько порядков) изменена путем термообработки в парах собственных компонентов. При термообработке преимущественно возникают те дефекты, энергия образования которых меньше. В сульфидах и селенидах доминирующим типом дефектов являются вакансии в анионной подрешетке.
Химическая чистота является хотя и необходимым, но недостаточным условием для получения кристаллов соединений типа A2B6 с заданными свойствами. Требуется обязательно управлять степенью дефектности кристаллической решетки, т.е. концентрацией вакансий. Самокомпенсация сульфидов и селенидов собственными дефектами структуры является основной причиной, препятствующей обращению типа электропроводности при их легировании. К этому следует добавить, что акцепторы обладают малой растворимостью в полупроводниках A2B6 и, как правило, образуют глубокие уровни.
Технология выращивания монокристаллов полупроводниковых соединений A2B6 разработана гораздо менее полно, чем технология полупроводников типа A3B5. Широкозонные полупроводники A2B6 представляют собой в технологическом отношении трудные объекты, так как обладают высокими температурами плавления и высокими давлениями диссоциации в точке плавления. Синтез исходных соединений A2B6, в частности порошка для люминофоров, чаще всего осуществляют по реакциям обменного разложения, протекающим в водной среде.
12.2.2 Основные виды соединений типа A2B6
Сульфид цинка, сернистый цинк, ZnS – цинковая соль сероводородной кислоты. Белый порошок, плотность 3,98‒4,09 г/см³. При обычном давлении не плавится, под давлением 15 МПа (150 атм.) плавится при 1850 °C. Во влажном воздухе сульфид цинка окисляется до сульфата; при нагревании на воздухе образуется ZnO и SO2. В воде нерастворим, в кислотах растворяется с образованием соответствующих солей и выделением сероводорода. В присутствии следов меди, кадмия, серебра и др. приобретает способность к люминесценции.
В природе ZnS встречается в виде минералов сфалерита (цинковая обманка) – основного сырья для получения цинка – и вюрцита (рис. 12.3).
Сульфид цинка может быть получен пропусканием сероводорода через растворы солей цинка. Сульфид цинка может быть получен при воздействии ударных волн на смесь порошков цинка и серы.
Применяется для создания люминофоров: ZnS:Ag (с синим цветом свечения) – для цветных кинескопов; (Zn, Cd)S:Ag – для рентгеновских трубок, ZnS:Cu (с зеленым цветом свечения) – для светящихся табло, панелей. Сульфид цинка ‒ полупроводниковый материал, используемый, в частности, в полупроводниковых лазерах.


Рис. 12.3 Структура сфалерита (слева) и вюрцита
Сульфид кадмия – химическое вещество с формулой CdS, существует в виде минералов гринокит и хоулиит, которые встречаются в виде жёлтых налетов на сфалерите (ZnS) и смитсоните. Гринокит имеет гексагональную структуру вюрцита. Он имеет желтоватый цвет с удельной массой 4,7 г/см³ и твердостью по шкале Мооса 3,8. Хоулиит имеет кубическую структуру сфалерита (цинковой обманки). Так как эти минералы не широко распространены в природе, то для промышленного использования и научно-технических разработок сульфид кадмия получают путем синтеза.
Синтезированные красители кадмия, основанные на сульфиде кадмия, ценятся за их хорошую температурную стабильность во многих полимерах, например, инженерном пластике. С добавлением селена в формулу можно получать цвета красителей в диапазоне от зелёно-жёлтого до красно-фиолетового. Погодное сопротивление для этого красителя равно 8, что показывает устойчивость красителя к УФ излучению.
Сульфид кадмия является широкозонным полупроводником с шириной запрещённой зоны 2,42 эВ при 300 K. Это свойство CdS, полезное в оптоэлектронике, используется как в фоточувствительных, так и в фотогальванических устройствах. Его используют для изготовления фоторезисторов (приборов, электрическое сопротивление которых меняется в зависимости от освещенности). Сульфид кадмия действует как люминофор (также в смеси с сульфидом цинка). Монокристаллы сульфида кадмия используются как детекторы элементарных частиц.
Селенид ртути (HgSe) является полупроводником n-типа проводимости, что объясняется внедрением атомов ртути в междоузлия или вакансиями в подрешетке селена. Наиболее вероятное значение ширины запрещенной зоны селенида ртути 0,2 эВ, хотя в литературе встречаются данные как в сторону большей, так и меньше указанной величины. Для кристаллов HgSe с концентрацией электронов не менее 3,5⋅1017 см-3 подвижность их достигает 18 500 см2/(В⋅с) при 300 К. Легированием не удается получить селенид ртути р-типа. Исследованием термо- и гальваномагнитных эффектов в селениде ртути было показано, что подвижность электронов в нем лимитируется рассеянием на акустических фононах. Это служит доказательством преимущественной ковалентной межатомной связи в селениде ртути. Теллурид ртути (HgTe) – полуметалл, хотя его можно считать полупроводником с очень малой шириной запрещенной зоны (порядка 0,01 эВ). HgTe может быть в основном р-типа проводимости. Одной из особенностей теллурида ртути является то, что его состав может иметь значительные отклонения от стехиометрического (число атомов ртути и теллура в кристалле не равны). Поэтому свойства HgTe во многом определяются отклонениями от стехиометрического состава и наличием точечных дефектов, которые влияют на электрические свойства как атомы посторонних примесей. Поэтому данные о типе и проводимости HgTe противоречивы.HgTe представляет собой практически чёрные кубические кристаллы с постоянной решётки 6,46 Å при 300 К. Твердость по шкале Мооса 2÷2,5. Объёмный модуль упругости около 42 ГПа, прочность около 300 МПа. При обычных условиях устойчива кристаллическая структура типа сфалерита. По электрическим свойствам представляет собой полуметалл, то есть при 0 К валентные зоны соприкасаются, но не перекрываются, поэтому, в отличие от полупроводников его проводимость не равна 0 при 0 К, но как у полупроводников растёт при росте температуры из-за перекрытия валентной зоны и зоны проводимости.
Получают HgTe прямым синтезом из элементов − длительным нагреванием металлического теллура в парах ртути при повышенном давлении в запаянной кварцевой ампуле. Эпитаксиальные монокристаллические плёнки HgTe могут быть получены методом газовой эпитаксии при разложении элементоорганических соединений теллура и ртути.
Теллурид свинца (PbTe) – химическое соединение свинца и теллура, кристаллизующееся в структуре NaCl с решеткой, состоящей из гране-центрированных кубических решеток Рb и Те, смещенных одна относительно другой на половину диагонали куба. Узкозонный прямозонный полупроводник группы A2B6 с шириной запрещённой зоны 0,32 эВ при 300 K. Используется для создания фоторезисторов, работающих в инфракрасной области спектра. Известен как термоэлектрический материал. Встречается в природе в виде минерала алтаита.
Теллурид свинца имеет необычно высокую для полупроводников диэлектрическую проницаемость (ε = 410 при 300 K), величина которой увеличивается до 3000 при охлаждении до 4,2 K. По этой причине теллурид свинца относится к виртуальным сегнетоэлектрикам.
12.2.3 Применение полупроводников типа А2В6
Из всех соединений типа A2B6 по масштабам применения выделяются сульфид цинка ZnS и сульфид кадмия CdS. Первый является основой для многих промышленных люминофоров, а второй широко используется для изготовления фоторезисторов, обладающих высокой чувствительностью в видимой области спектра. Предпочтение отдают люминофорам с кубической структурой ввиду повышенной яркости свечения.
Важной особенностью сульфида цинка является то, что он образует непрерывный ряд твердых растворов с CdS, CdSe, ZnSe. При этом добавка CdS стабилизирует гексагональную модификацию, а добавка ZnSe – кубическую. Недостатком электролюминесцентных устройств на основе сульфида цинка является относительно высокая скорость деградации приборов (ухудшения их свойств), обусловленная усилением ионного характера химической связи, стимулирующим процессы электролиза.
Узкозонные полупроводники типа A2B6 представляют интерес для создания приемников далекого ИК излучения. Особое внимание привлекают твердые растворы CdxHg1-xTe, спектр фоточувствительности которых перекрывает атмосферное «окно прозрачности» в области 8÷14 мкм.
Пленки из селенида и теллурида ртути, благодаря высокой подвижности электронов, применяют для изготовления высокочувствительных датчиков Холла. Высокая эффективность излучательной рекомбинации в полупроводниках типа A2B6 позволяет использовать монокристаллы этих соединений в качестве рабочего тела полупроводниковых лазеров, возбуждаемых электронным пучком.
Тонкие пленки и поликристаллические слои халькогенидов свинца обладают высокой фоточувствительностью в далекой ИК области спектра, причем «красная» граница внутреннего фотоэффекта с понижением температуры смещается в длинноволновую область. Благодаря хорошим фотоэлектрическим свойствам халькогениды свинца широко используются для изготовления фоторезисторов.
Одна из главных причин повышенного интереса к твердым растворам на основе халькогенидов свинца связана с использованием этих материалов для изготовления фотоприемников с высокой спектральной чувствительностью в диапазоне «атмосферного окна» 8÷14 мкм, которое соответствует максимуму излучения абсолютно черного тела при 300К.
Перспективно использование твердых растворов Рb1-xSnxTe для инжекционных лазеров с излучением в спектральном диапазоне до 30 мкм. Это значение соответствует максимальной длине волны излучения для полупроводниковых лазеров.
12.3 Полупроводниковые соединения группы AIVBIV
Из полупроводниковых соединений этой группы наибольшее применение нашел карбид кремния SiC (карборунд).
Чистый карбид кремния стехиометрического состава − бесцветные кристаллы с алмазным блеском. Технический SiC может иметь разнообразную окраску: белую, серую, желтую, зеленую и черную. Цвет материала зависит от сырья и технологии получения кристаллов и определяется как типом и количеством примеси, так и степенью отклонения состава от стехиометрического. Карбид кремния кристаллизуется в двух модификациях: при температурах менее 2000оС − в кубической типа сфалерита (β-SiC), и при более высоких температурах − в гексагональной (α-SiC). Для высокотемпературной гексагональной модификации карбида кремния характерно явление политипизма: обнаружено более 50 политипных модификаций α-SiC.
12.3.1 Свойства карбида кремния
Карбид кремния − единственное полупроводниковое бинарное соединение АIVВIV. Тип связи − ковалентный, доля ионной составляющей порядка 10%. Ширина запрещенной зоны для кристаллов SiC составляет 2,39 эВ, для различных модификаций SiC ширина запрещенной зоны может иметь значение в пределах от 2,36 до 3,34 эВ. Большие значения ширины запрещенной зоны позволяют создавать на его основе полупроводниковые приборы, сохраняющие работоспособность при температурах до 600 оС. Собственная электропроводность из-за большой ширины запрещенной зоны наблюдается лишь при температурах выше 1400 оС. Подвижность носителей заряда низкая. Монокристаллы карбида кремния, легированные примесями элементов V группы (азот, фосфор, мышьяк, сурьма, висмут), а также литием и кислородом имеют n-тип проводимости и зеленую окраску. Элементы III группы (бор, алюминий, галлий, индий) и элементы II группы (бериллий, магний, кальций) являются акцепторами. При этом кристаллы имеют p-тип проводимости и голубую или черную окраску. В случае отклонения состава от стехиометрического в сторону кремния кристаллы обладают электропроводностью n-типа, в случае избытка углерода − p-типа.
Карбид кремния тугоплавок (Тпл = 2830 °С), химически стоек, по твердости уступает лишь алмазу и нитриду бора: твердость по шкале Мооса − 9,1÷9,5; микротвердость 330÷360 МПа. Карбид кремния обладает высокой термической, химической и радиационной стойкостью, устойчивостью к окислению подобно многим окалиностойким сплавам и химическим соединениям. Заметно окисляется только при температурах выше 800 оС. Карбид кремния химически стоек и в других средах: он не реагирует с минеральными кислотами любых концентраций, включая и плавиковую кислоту. При комнатной температуре химически взаимодействует с ортофосфорной кислотой, и смесью азотной и фтористоводородной кислот − при температуре 200 оС. Водяной пар реагирует с карбидом кремния, только начиная с 1300÷1400 оС.
Вплоть до 1100 оС с карбидом кремния совершенно не взаимодействует азот. Инертен он также в среде водорода и углекислого газа. В среде хлора теряет устойчивость при сравнительно низких температурах, разлагаясь по реакциям:
SiC + 2Cl2 = SiCl4 + C (при 100 оС);
SiC + 4Cl2 = SiCl4 + CCl4 (при 1000оС).
Карбид кремния активно разлагается с образованием соответствующих силикатов при сплавлении с едкими и углекислыми щелочами и перекисями.
Существует примерно 250 кристаллических форм карбида кремния. Полиморфизм SiC характеризуется большим количеством схожих кристаллических структур, называемых политипами. Они являются вариациями одного и того же химического соединения, которые идентичны в двух измерениях, но отличаются в третьем. Таким образом, их можно рассматривать как слои, сложенные в стопку в определенной последовательности.
Альфа-модификация карбида кремния (α-SiC) является наиболее часто встречающимся полиморфом. Эта модификация образуется при температуре свыше 1700 °C и имеет гексагональную решётку, кристаллическая структура типа вюрцита.
Бета-модификация (β-SiC), с кристаллической структурой типа цинковой обманки (аналог структуры алмаза), образуется при температурах ниже 1700 °C. До недавнего времени β-форма имела сравнительно небольшое коммерческое использование, однако в настоящее время в связи с использованием его в качестве гетерогенных катализаторов интерес к ней увеличивается.
Карбид кремния является полупроводником, тип проводимости которого зависит от примесей. Проводимость n-типа получается при легировании азотом или фосфором, а p-тип − с помощью алюминия, бора, галлия или бериллия. Металлическая проводимость была достигнута за счет сильного легирования бором, алюминием и азотом. Сверхпроводимость была обнаружена в политипах 3C-SiC:Al, 3C-SiC:B и 6H-SiC:B при одинаковой температуре − 1,5 К.
Таблица 12.2 Свойства основных политипов карбида кремния
| Политип | 3C (β) | 4H | 6H (α) |
| Кристаллическая структура | Цинковая обманка (кубич.) | Гексагональная | Гексагональная |
| Постоянные решётки, Å | 4,359 | 3,073; 10,053 | 3,073; 15,11 |
| Плотность, г/см³ | 3,21 | 3,21 | 3,21 |
| Ширина запрещенной зоны, эВ | 2,36 | 3,23 | 3,05 |
| Модуль объемного сжатия, ГПа | |||
| Теплопроводность, Вт/(см·К) | 3,6 | 3,7 | 4,9 |
12.3.2 Получение карбида кремния
Поликристаллический карбид кремния получают в электрических печах при температуре 1800÷2300 оС путем восстановления двуокиси кремния углеродом:
SiO2 + 3C = SiC + 2CO.
В качестве сырья при производстве технического карбида кремния используют кварцевый песок с минимальным содержанием примесей и малозольный кокс или антрацит, или нефтяной кокс. Для повышения газопроницаемости шихты в нее иногда вводят древесные опилки. В шихту также вводят поваренную соль, количество которой влияет на цвет карборунда.
Из-за высоких значений температуры и давления, при которых существует расплав карбида кремния, классические методы получения из него монокристаллов не применимы. Используют методы выращивания кристаллов SiC из газовой фазы или из растворов в расплаве. Большое распространение получил метод сублимации. В этом методе рост кристаллов карбида кремния происходит из газовой фазы в графитовых тиглях в атмосфере инертных газов при температуре 2500÷2600 оС. Эпитаксиальные слои и твердые растворы на основе карбида кремния можно получать всеми известными методами, используемыми в полупроводниковой технологии. Технология формирования структур карбида кремния на подложках кремния принципиально не отличается от процессов получения кремниевых пленок. Гетероэпитаксиальные слои выращивают методом газофазной эпитаксии в открытой системе. В качестве газа-носителя используется водород диффузионной очистки; в первой зоне свободный углерод связывается с водородом и переносится в зону роста полупроводниковой пленки.
12.3.3 Применение карбида кремния
Монокристаллический SiC используют для изготовления радиационностойких светодиодов, обладающих очень высокой надежностью и стабильностью работы. Его можно использовать для изготовления высокотемпературных силовых полупроводниковых приборов, полевых транзисторов, туннельных диодов, счетчиков частиц высокой энергии, терморезисторов,
Из поликристаллического SiC выращивают монокристаллы или путем дробления получают порошки. Поликристаллический SiC используют в производстве нелинейных резисторов (варисторов). Для этих целей изготавливают многофазные материалы на основе порошкообразного SiC, скрепленного связующим веществом. Кроме того, на основе порошкообразного SiC производят высокотемпературные нагреватели, волноводные поглотители, а на основе пленок аморфного SiC − светодиоды и солнечные элементы. SiC является перспективным полупроводниковым материалом для высокотемпературной и высокочастотной электроники.
Благодаря высокой химической стабильности, огнеупорности и износостойкости карбид кремния находит широкое применение в качестве огнеупора в металлургической промышленности. Применяется в машиностроении для футеровки термических печей; в химическом аппаратостроении, где он подвержен абразивному воздействию твердых пылевидных продуктов в газовых потоках. Используется для изготовления коррозионно- и эрозионностойких сопельных вставок, насадок и распылителей; для изготовления деталей теплообменной аппаратуры и деталей насосов для перекачки кислых растворов и других коррозионноактивных жидкостей. Огнеупорные изделия, а также изделия конструкционного назначения на основе карбида кремния изготовляют с использованием различного вида связок − керамических, кремния, нитрида кремния. Интересно использование карбида кремния в электротехнике - для изготовления нагревателей высокотемпературных электропечей сопротивления (силитовые стержни), грозоразрядников для линий передачи электрического тока, нелинейных сопротивлений, в составе электроизолирующих устройств и т. д.
Благодаря высокой твердости, химической устойчивости и износостойкости карбид кремния широко применяется как абразивный материал (при шлифовании), для резания твердых материалов, точки инструментов.
В настоящее время существует большой интерес в использовании данного вещества в качестве полупроводникового материала в электронике, где его высокая теплопроводность, высокое электрическое поле пробоя и высокая плотность электрического тока делают его перспективным материалом для высокомощных устройств. Карбид кремния имеет очень низкий коэффициент теплового расширения (4,0×10−6K) и он не испытывает фазовые переходы из-за которых может произойти разрушение монокристаллов.
Карбид кремния используется в сверхбыстрых высоковольтных диодах Шоттки, N-МОП-транзисторах и в высокотемпературных тиристорах. По сравнению с приборами на основе кремния и арсенида галлия приборы из карбида кремния имеют следующие преимущества:
- в несколько раз большая ширина запрещённой зоны;
- в 10 раз большая напряженность поле электрического пробоя;
- высокие допустимые рабочие температуры (до 600 °C);
- теплопроводность в 3 раза больше, чем у кремния, и почти в 10 раз больше, чем у арсенида галлия;
- устойчивость к воздействию радиации;
- стабильность электрических характеристик при изменении температуры и отсутствие дрейфа параметров во времени.
Из почти двухсот пятидесяти модификаций карбида кремния только две применяются в полупроводниковых приборах — 4H-SiC и 6H-SiC.
Проблемы с интерфейсом элементов, основанных на диоксиде кремния, препятствуют развитию n-МОП-транзисторов и БТИЗ (биполярные транзисторы с изолированным затвором), основанных на карбиде кремния. Другая проблема заключается в том, что сам SiC пробивается при высоких электрических полях в связи с образованием цепочек дефектов упаковки, но эта проблема может быть решена совсем скоро.
История светодиодов из SiC весьма примечательна: первые светодиоды с использованием SiC были продемонстрированы в 1907 году. Первые коммерческие светодиоды были также на основе карбида кремния. Желтые светодиоды из 3C-SiC были изготовлены в Советском Союзе в 1970-х годах, а синие (из 6H-SiC) по всему миру в 1980-х. Производство вскоре остановилось, потому что нитрид галлия показал в 10÷100 раз более яркую эмиссию. Эта разница в эффективности связана с неблагоприятной непрямой запрещенной зоной SiC, в то время как нитрид галлия имеет прямую запрещенную зону, которая способствует увеличению интенсивности свечения. Тем не менее, SiC по- прежнему является одним из важных компонентов светодиодов − это популярная подложка для выращивания устройств из нитрида галлия, также он служит теплораспределителем в мощных светодиодах.
Карбид кремния используется для производства графена с помощью графитизации при высоких температурах. Это производство рассматривается как один из перспективных методов синтеза графена в больших масштабах для практических применений.
Дата добавления: 2014-12-04; просмотров: 4022;
