БИНАРНЫЕ ПОЛУПРОВОДНИКОВЫЕ СОЕДИНЕНИЯ
Общее число элементарных полупроводников невелико, их электрофизические свойства не настолько разнообразны, чтобы удовлетворить требованиям современной полупроводниковой техники. Число же полупроводниковых соединений практически неограниченно и, следовательно, всегда найдутся вещества с нужными для практики свойствами. Лучше других изучены бинарные полупроводниковые соединения. Вероятно, большинство двойных соединений, известных в неорганической химии, в той или иной степени проявляет полупроводниковые свойства. Сюда относятся многочисленные оксиды металлов, сульфиды, селениды, теллуриды, нитриды, фосфиды, карбиды, силициды и т.п. В основу классификации бинарных полупроводниковых соединений можно положить следующие принципы: – кристаллохимический (по структуре), – по расположению исходных элементов в Периодической системе (см. табл. 10.1), например, соединения AIIBVI, – по названию анионообразователя (силициды, арсениды и т. п.). Классификация бинарных полупроводниковых соединений по названию анионообразователей чаще всего применяется для оксидов, сульфидов, селенидов и т. п. Такая классификация относится лишь к соединениям, образованным по правилам валентности. Такие полупроводники, как ZnSb и CdSb, нельзя называть антимонидами цинка и кадмия, так как, согласно рациональной номенклатуре неорганической химии, ими являются соединения Zn3Sb2 и Cd3Sb2. To же относится к NaSb, KSb, ZnAs2, CdAs2 и другим полупроводникам. Поэтому удобна классификация полупроводниковых соединений по расположению исходных элементов в Периодической системе. Некоторые из них (например, AIIIBVI) начали синтезировать и исследовать в последние десятилетия. Другие же (например, AIIBVI) давно известны в химии, хотя их полупроводниковые свойства начали изучаться в последнее время. Соединения типа AIIIBV и AIIBVI имеют наибольшее практическое значение. Они являются изоэлектронными аналогами алмаза, кремния, германия и α-олова. Это значит, что общая сумма валентных электронов во всех этих соединениях равна 8. По ряду своих важных свойств эти вещества проявляют сходство с кремнием и германием. Для них всех характерно координационное число 4. Кроме бинарных полупроводников известны тройные и более сложные соединения, содержащие в своем составе три и большее число компонентов. К сложным полупроводникам также относят твердые растворы из элементарных полупроводников и полупроводниковых соединений, обладающие полупроводниковыми свойствами. 12.1 Полупроводниковые соединения AIIIBV Полупроводниковые соединения AIIIBV (или А3В5) образуются в результате взаимодействия элементов III и V групп Периодической системы. В III группе соединения типа АIIIВV образуют элементы бор и алюминий, а также металлы подгруппы галлия (исключение составляет таллий). В V группе соединения типа AIIIBV дают азот, фосфор, мышьяк и сурьма. Висмут не образует соединений рассматриваемого ряда. Наиболее известны девять соединений AIIIBV, образующиеся сочетанием, с одной стороны, Al, Ga, In и, с другой, – фосфора (фосфиды), мышьяка (арсениды) и сурьмы (стибиды, или антимониды). Полупроводниковые соединения AIIIBV образуют гомологический ряд, в котором наблюдается закономерное изменение многих свойств при изменении атомных номеров компонентов (см. Приложение 6). В настоящем параграфе рассмотрены основные материалы из этой группы соединений, имеющие наибольшее практическое применение. 12.1.1 Структура соединений группы AIIIBV Соединения типа AIIIBV кристаллизуются в решетке цинковой обманки или сфалерита. Одни атомы (безразлично AIII или BV) занимают вершины и центры граней куба, а другие – центры четырех (из восьми) малых кубов (рис. 12.1). Значит, структура AIIIBV аналогична структуре алмаза с той только разницей, что центры малых кубов заняты атомами другого вида по сравнению с вершинами и центрами граней большого куба. В элементарной ячейке, показанной на рис. 12.1, находятся четыре атома одного вида и четыре – другого, т.е. всего восемь атомов. Таким образом, в кристаллической решетке AIIIBV каждый атом AIII соединен с четырьмя атомами BV и, наоборот, каждый атом BV тетраэдрически окружен четырьмя атомами AIII. Поэтому весь кристалл можно рассматривать как совокупность бесконечно повторяющихся звеньев –А–В–, в которых кратчайшее расстояние между AIII и BV зависит от природы этих атомов.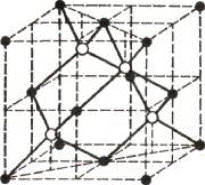
Рис 12.1– Сфалеритная структура соединений химических связей в соединениях AIIIBV:
черные кружки – атомы A3; белые – атомы B5
Для соединений AIIIBV характерен особый тип химической связи, называемой донорно-акцепторной. Из четырех ковалентных связей, которыми каждый атом встраивается в решетку, три образуются обобществлением валентных электронов атомов A3 и B5, а четвертая связь осуществляется неподеленной парой валентных электронов атомов B5. На рис. 12.2 такие электроны изображены крупными точками. Образование этой связи соответствует энергетически выгодному переходу электронов от атома B5 в энергетическое состояние, общее для донора (атомов B5) и акцептора (атома A3). В каждой ковалентной связи максимум электронной плотности смещен в сторону атома с более высокой электроотрицательностью, т.е. электронные облака стянуты к узлам решетки, где находятся атомы B5.
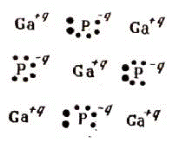
Рис. 12.2 Схема образования донорно-акцепторных связей в A3B5 на примере фосфида галлия
Благодаря такой поляризации связей атомы A3 приобретают некоторый эффективный положительный заряд, а атомы B5 – отрицательный. Величина этого эффективного заряда (±q) определяет степень ионности соединения, которая закономерно изменяется при переходе от одного соединения к другому в соответствии с положением химических элементов в Периодической таблице Д. И. Менделеева. Полупроводниковые соединения A3B5 образуют гомологический ряд, в котором наблюдается закономерное изменение многих свойств при изменении атомных номеров компонентов.
Большинство соединений A3B5 характеризуется незначительными отклонениями от стехиометрического состава, поэтому они относительно просты по механизму легирования, в них легко формируются электронно-дырочные переходы. Как правило, введение избытка одного из компонентов в среду кристаллизации не сказывается существенно на электрофизических свойствах материала. Исключение составляют нитриды, в которых возникают трудности с инверсией типа электропроводности. В частности, нитрид галлия независимо от условий получения кристаллов всегда проявляет электропроводность n-типа.
Примеси замещения в кристаллической решетке соединений A3B5 распределяются таким образом, чтобы не возникало центров с большим избыточным зарядом. Поэтому примеси элементов II группы – Be, Mg, Zn и Cd, образующие твердые растворы замещения, всегда занимают в решетке A3B5 узлы металлического компонента и при этом являются акцепторами благодаря меньшей валентности по сравнению с валентностью замещаемых атомов. В то же время примеси элементов VI группы (S, Se, Те) всегда располагаются в узлах B5 и играют роль доноров.
Более сложным характером отличается поведение примесей элементов IV группы. Поскольку в этом случае при замещении атомов одной из двух подрешеток имеется избыток или недостаток лишь одного валентного электрона, то атомы примесей IV группы могут занимать как узлы A3, так и B5, проявляя при этом донорные или акцепторные свойства соответственно. Замещение должно сопровождаться наименьшей деформацией кристаллической решетки. Поэтому критерием донорного или акцепторного действия примесей может служить соответствие размеров замещающего и замещаемого атомов. В большинстве случаев атомы примесей элементов IV группы локализуются в одной из подрешеток. Например, в антимониде индия кремний и германий замещают только атомы сурьмы и являются акцепторами, а в арсениде индия замещают индий и являются только донорами. Однако в некоторых соединениях наблюдается амфотерное поведение этих примесей. Так, в арсениде и фосфиде галлия наблюдается парное вхождение атомов кремния и германия в кристаллическую решетку соединения с одновременным замещением узлов A3 и B5. В зависимости от степени легирования, температуры роста и состава кристаллизационной среды имеет место преимущественное вхождение этих примесей в ту или иную подрешетку.
Примеси элементов 3-б и 5-б подгрупп обычно замещают соответственно атомы A3 и B5 в решетке соединения, образуя нейтральные центры. Растворимость этих элементов в большинстве случаев столь велика, что удается получать кристаллы твердых растворов во всем диапазоне концентраций.
Существенной особенностью процесса диффузии в полупроводниках A3B5 является его зависимость от давления паров летучего компонента группы B5, которое определяет концентрацию дефектов в решетке. Установлено, что в арсениде галлия с ростом давления паров мышьяка коэффициент диффузии акцепторных примесей уменьшается, а донорных увеличивается. Это связано с тем, что с ростом давления мышьяка уменьшается концентрация вакансий мышьяка в кристаллической решетке и увеличивается концентрация вакансий галлия. Соответственно смещается равновесие между количеством примесных атомов, находящихся в узлах и междуузлиях. Аналогичные закономерности имеют место и в других полупроводниках типа A3B5.
Доноры в соединениях типа A3B5 характеризуются крайне низкими значениями коэффициентов диффузии. Чтобы проникновение доноров достигло измеримых размеров, необходимы высокая температура (в пределах 200÷300°С от точки плавления основного вещества) и продолжительное время диффузии. Это приводит к нарушению (эрозии) поверхности из-за переноса летучего элемента V группы под влиянием небольших градиентов температуры внутри ампулы. Кроме того, диффузия таких доноров, как S, Se и Те, осложняется образованием на поверхности полупроводника слоя сложного фазового состава (химических соединений типа Ga2S3).
12.1.2 Арсенид галлия
GaAs – один из основных полупроводниковых материалов, относящийся к классу соединений AIIIBV. Благодаря удачному сочетанию свойств он занимает второе место (после кремния) по своему значению в современной электронной технике. Арсенид галлия имеет неплохие теплофизические характеристики, достаточно большую ширину запрещенной зоны, высокую подвижность электронов, благоприятные особенности зонной структуры, обуславливающие возможность прямых межзонных переходов носителей заряда. Разработаны технологии получения материала с хорошими изолирующими свойствами и высокой прозрачностью в инфракрасной области спектра.
Свойства арсенида галлия. Кристаллы GaAs кристаллизуются в решетке сфалерита. Постоянная решетки при 300К равна 5,653 Å, расстояние между ближайшими соседними атомами 2,45 Å; относительная молекулярная масса 144,63; число атомов в 1 см3 4,42·1022; плотность GaAs в твердом состоянии 5,32 г/см3, в жидком состоянии – 5,71 г/см3; температура плавления Тпл= 1238 оС; равновесное давление паров мышьяка в точке плавления ~ 1.105 Па (0,98 атм), что в значительной мере усложняет технологию его получения. Твердость по минералогической шкале 4,5; температурный коэффициент линейного расширения ТКЛР = 6,4×10-6 К-1; ширина запрещенной зоны 1,43 эВ; диэлектрическая проницаемость статическая 13,1, высокочастотная 10,89.
Электрофизические свойства нелегированного арсенида галлия в сильной степени зависят от состава и концентрации собственных точечных дефектов, концентрации фоновых примесей и режимов термообработки слитков. Для получения монокристаллов n- и p-типа проводимости с заданной концентрацией носителей заряда используют легирование электрически активными примесями. Основными легирующими примесями при получении монокристаллов n-типа являются S, Se, Te, Si, Sn, а при получении монокристаллов p-типа – Zn.
Арсенид галлия не взаимодействует с водой, но активно разлагается под действием кислот с выделением токсичного арсина. Удельная скорость растворения арсенида галлия существенно возрастает в смесях кислот. При нагреве на воздухе до 300 оС арсенид галлия не окисляется. Арсенид галлия относится к числу разлагающихся соединений: начиная с 600 оС, разлагается с выделением мышьяка. Расплавленный арсенид галлия очень активен и взаимодействует практически со всеми известными материалами, используемыми для изготовления плавильных контейнеров. Поэтому наибольшее распространение в технологии арсенида галлия нашел синтетический кварц, а при получении высокочистого полуизолирующего арсенида галлия применяют пиролитический нитрид бора.
Одной из основных технологических характеристик GaAs является плотность дислокаций Nd (число линий дислокаций, пересекающих единицу поверхности кристалла). Характер распределения и величина плотности дислокаций оказывает влияние на рабочие параметры изготавливаемых на его основе приборов. В производстве светодиодов применяют кристаллы с Nd = (5-10).103 см-2, в производстве лазеров – с Nd = 5.102 см-2. Присутствие дислокаций в активных областях светоизлучательных структур, изготовленных на сильно легированных пластинах GaAs n- и p-типа проводимости, приводит к быстрой деградации характеристик прибора. В связи с этим низкая плотность дислокаций является основным требованием к материалу. Характер распределения дислокаций и их плотность влияют также на распределение параметров СВЧ-приборов по площади пластины нелегированного полуизолирующего (ПИ) GaAs. Это связано с перераспределением собственных точечных дефектов вблизи дислокаций.
Плотность дислокаций в кристаллах полупроводников определяется термопластической деформацией, которая успевает пройти в кристалле в процессе релаксации термоупругих напряжений, т.е. зависит от условий получения (метода выращивания), диаметра кристалла и концентрации легирующей примеси.
Методы получения кристаллов арсенида галлия.Получение малодислокационных и бездислокационных кристаллов GaAs является сложной технологической задачей, к настоящему времени практически нерешенной. Исключение составляют сильно легированные кристаллы, так как введение легирующих примесей при достижении определенного уровня легирования сопровождается эффектом «примесного упрочнения» − снижения плотности дислокаций − в кристаллах арсенида галлия.
В промышленном производстве монокристаллов GaAs используются три метода выращивания:
– метод Чохральского с жидкостной герметизацией расплава слоем борного ангидрида (Liquid Encapsulated Czochralski − LEC), используется в основном для получения нелегированного ПИ-GaAs;
– метод горизонтальной направленной кристаллизации (ГНК) в вариантах «по Бриджмену» (Horizontal Bridgman − HB) или «кристаллизации в движущемся градиенте температуры» (Horizontal Gradient Freeze − HGF), используется для получения кристаллов n-типа проводимости, легированных кремнием;
– метод вертикальной направленной кристаллизации (ВНК) в тех же двух вариантах (Vertical Bridgman − VB Vertical и Gradient Freeze − VGF), используется для получения как легированных донорными примесями кристаллов, так и для получения нелегированного арсенида галлия.
Метод LEC является одним из основных в производстве монокристаллов GaAs. При выращивании монокристаллов арсенида галлия методом Чохральского с жидкостной герметизацией расплава необходимо учитывать, что процесс осуществляется при достаточно больших осевых и радиальных градиентах температуры вблизи фронта кристаллизации, т.е. в области максимальной пластичности материала. Очевидным следствием роста кристалла при высоких градиентах температуры при таких условиях является высокая плотность дислокаций, типичные значения которой составляют от 1×104 до 2×105 см-2 в зависимости от диаметра слитка.
В целях снижения температурных градиентов и соответственно снижения плотности дислокаций было предложено несколько модификаций метода. Одной из таких модификаций является выращивание в условиях полной герметизации растущего кристалла. Однако при малых радиальных градиентах температуры, характерных для этого метода, затруднено поддержание диаметра растущего кристалла. Этот метод не позволяет выращивать достаточно длинные кристаллы, что делает его непригодным для промышленного использования. Более эффективным является метод Чохральского с контролируемым давлением паров мышьяка. В нем исключается разложение выращенного слитка. Использование этого метода позволило значительно снизить плотность дислокаций в монокристаллах арсенида галлия. Недостатком этого метода является высокая стоимость оборудования.
Основным вариантом технологии LEC стал совмещенный процесс синтеза и выращивания монокристалла в установке «высокого давления» (с рабочим давлением 60÷70 атм. при синтезе и 20÷30 атм. при выращивании). Для получения арсенида галлия с высоким удельным сопротивлением − ПИ-GaAs − используют высокочистые галлий и мышьяк, тигли из пиролитического нитрида бора и управление содержанием фонового углерода, определяющим величину удельного сопротивления и подвижности носителей заряда в материале. При низких концентрациях углерода (1×1015 ат/см3) обеспечиваются наилучшие с точки зрения использования в технологии ионной имплантации свойства GaAs, при достаточно высоком содержании углерода (3×1015 ат/см3) кристаллы имеют высокое удельное сопротивление (108 Ом×см), что важно при использовании ПИ-GaAs в качестве подложек в эпитаксиальных технологиях.
Основным направлением развития технологии LEC является увеличение диаметра выращиваемых монокристаллов при одновременном увеличении массы загрузки, что продиктовано необходимостью повышения экономической эффективности производства. Доминирующее положение в структуре производства LEC-ПИ-GaAs пока занимают монокристаллы диаметром 100 мм, но уже более 20% продаж приходится на пластины диаметром 150 мм.
Монокристаллы GaAs, легированные кремнием с низкой плотностью дислокаций, выращивают методом ГНК в кварцевых контейнерах. Однако используемые контейнерные материалы имеют низкую механическую прочность, что не позволяет получить кристаллы большого диаметра. Применение метода ВНК частично устраняет присущие методу ГНК недостатки и позволяет получать легированные кремнием кристаллы диаметром до 100 мм с низкой плотностью дислокаций.
Применение арсенида галлия. Основное применение имеют:
1) Нелегированный полуизолирующий (ПИ)GaAs с высоким удельным сопротивлением (107 Ом.см). Используется при изготовлении высокочастотных интегральных схем (ИС) и дискретных микроэлектронных приборов. Помимо высокого удельного сопротивления монокристаллы нелегированного GaAs, применяемые в производстве высокочастотных приборов (особенно с использованием технологий ионной имплантации), должны иметь высокие значения подвижности носителей заряда и высокую макро- и микроскопическую однородность распределения свойств как в поперечном сечении, так и по длине выращенных слитков.
2) Сильнолегированный кремнием GaAs n-типа проводимости с низкой плотностью дислокаций. Применяется при изготовлении светодиодов и лазеров. Монокристаллы сильно легированного кремнием (1017÷1018 см-3) GaAs, помимо высокой проводимости, должны обладать достаточно совершенной кристаллической структурой. Они широко используется в оптоэлектронике для изготовления инжекционных лазеров, свето- и фотодиодов, фотокатодов, являются прекрасным материалом для генераторов СВЧ-колебаний (так называемых генераторов или диодов Ганна). Применяются для изготовления туннельных диодов, способных работать при более высоких температурах, чем кремниевые, и на более высоких частотах, чем германиевые.
3) Монокристаллы ПИ-GaAs, легированные хромом, используют в инфракрасной оптике.
4) Монокристаллы GaAs, легированные цинком или теллуром, применяют в производстве оптоэлектронных приборов.
5) GaAs в качестве компонента входит в состав многих тройных и четверных твердых растворов.
12.1.3 Арсенид индия
Арсенид индия (InAs) – химическое соединение индия и мышьяка. Прямозонный полупроводник группы AIIIBV с шириной запрещённой зоны 0,36 эВ. Кристаллическая структура кубическая (структура сфалерита). Плотность 5,67 г/см3, Тпл = 942 оС, диэлектрическая проницаемость ε = 14,6.
Арсенид индия устойчив на воздухе и в парах воды до Т ≈ 300 °С. Взаимодействует с концентрированной соляной и серной кислотами, водными растворами сильных окислителей (например, Н2О2), смесями азотной, фтористоводородной и уксусной кислот, а также азотной и соляной кислот с Н2О2. Эти смеси используют для травления поверхности кристаллов арсенида индия с целью обнаружения дефектов и удаления загрязнений.
Получают арсенид индия в кварцевых ампулах взаимодействием расплава In с парами As, давление которых составляет 32,7 кПа при 800÷900 °С. Монокристаллы выращивают по методу Чохральского вытягиванием из-под слоя флюса жидкого В2О3 в атмосфере инертного газа (Аr, Не, N2) при давлении 40÷50 кПа (основной способ), направленной кристаллизацией из расплава при давлении паров As 32,7 кПа. Эпитаксиальные пленки InAs выращивают следующими методами:
− осаждением из раствора InAs в расплаве In при 650÷700 °С;
− осаждением из газовой фазы: пары AsCl3 или НС1 пропускают над расплавом In, образовавшиеся при этом хлориды In переносятся в зону реакции и взаимодействуют с парами AsCl3 или AsH3 при 700 °С, давая InAs;
− методом молекулярно-лучевой эпитаксии (реакцией молекулярных пучков In и As в вакууме 10 Па с последующим осаждением на нагретую до 400÷500 °С подложку).
Для получения монокристаллов и пленок со свойствами полупроводников n- или р-типа используют добавки соответственно Те, Se, Sn или Zn, Cd, Mn. Арсенид индия − полупроводникoвый материал для фотоприемников ИК излучения, датчиков эффекта Холла. Используется для создания сверхвысокочастотных транзисторов, светодиодов и фотодиодов, работающих в инфракрасной области спектра, датчиков магнитного поля, для создания массивов квантовых точек.
Дата добавления: 2014-12-04; просмотров: 9948;
