Пиридин
Пиридин – представитель шестичленных гетероциклов с одним гетероатомом, в качестве которого выступает атом азота
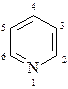
Монометилпиридины называются пиколинами, диметилпиридины – лутидинами, триметилпиридины – коллидинами. Насыщенный пиридиновый цикл носит название пиперидина.
Пиридин стал известен с 1851 г., когда его выделили из костяного масла, а несколько позже – из каменноугольной смолы (1854 г.)
Методы получения. Как уже было отмечено, пиридин выделяется из каменноугольной смолы. К сожалению, содержание его в этом источнике не превышает 0,1%.
Из синтетических методов получения пиридина значение имеют методы, основанные на превращениях акролеина и насыщенных и ненасыщенных альдегидов.
По методу Чичибабина (1937 г.) замещенные пиридины получают из альдегидов и аммиака (лучше использовать альдегидоаммиаки) при нагревании при 250оCв присутствии ацетата аммония
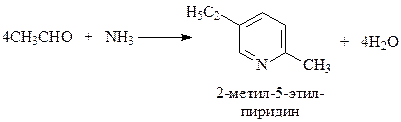
В реакцию с аммиаком может вступить и непредельные альдегиды

Практически важный синтез замещенных пиридинов основан на нагревании смеси диенового углеводорода и нитрила при 400оС
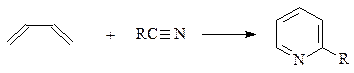
Метод получения пиридина из ацетилена и аммиака был разработан Реппе. Реакция протекает в присутствии сложных никелевых или кобальтовых катализаторов
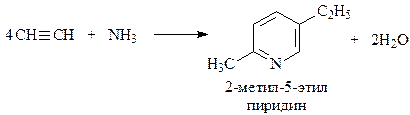
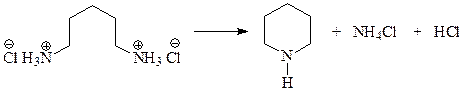
Соединение с насыщенным пиридиновым кольцом – пиперидин – можно получить нагреванием гидрохлорида пентаметилендиамина
Из более сложных синтезов приведем синтез коллидина по Ганчу. В этом синтезе из ацетоуксусного эфира и альдегида (в виде альдегидоаммика) получают этиловый эфир 2,4,6-триметил-1,4-дигидропиридин-3,5-дикарбоновой кислоты. В полученном продукте азотистой кислотой окисляют два водорода и создают, тем самым, замещенное пиридиновое кольцо. Затем следует стадия гидролиза и декарбоксилирования

Химические свойства. Пиридин представляет собой почти правильный шестиугольник, все атомы которого лежат в одной плоскости. По геометрическим параметрам пиридиновое кольцо похоже на бензольное
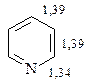
Атомы углерода в пиридине находятся в sp2-гибридном состоянии. На образование ароматического секстета пять углеродов дают по одному р-электрону, а шестой электрон поставляет атом азота, тот, который не участвует в гибридизации. Ось этой орбитали перпендикулярна к плоскости расположения всех атомов и связей пиридинового кольца. Из трех гибридных орбиталей азота две используются на образование σ-связей с двумя соседними атомами углерода, а на третьей орбитали находится неподеленная пара электронов
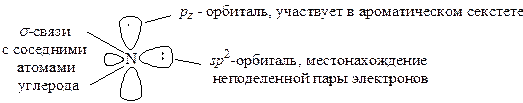
В соответствии с приведенным строением – пиридин представляет собой циклическое, плоское образование с хюккелевским числом р-электронов (4n+2=6 при n=1) и обладает ароматическим характером. Кроме того, за счет неподеленной пары электронов азота – основностью.
Картину строения пиридина дополняет значительный дипольный момент (2,26 D) пиридина, обусловленный большой электроотрицательностью атома азота, а также неравномерное распределение плотности π-электронного облака у атомов гетероцикла. Методом молекулярных орбиталей Хюккеля получено следующее распределение π-зарядов на атомах пиридинового кольца
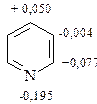
Отсюда видно, что пиридиновое кольцо обеднено электронами, особенно 2- и 4-положения. При этом имеется незначительная π-электронная избыточность в β-положениях.
Известно, что пиридин способен вступать:
- в реакции присоединения с участием атома азота,
- в реакции электрофильного замещения,
- в реакции нуклеофильного замещения,
- проявить основность.
Рассмотрим превращения пиридина более подробно.
Дата добавления: 2014-12-24; просмотров: 8166;
