Распределение энергии по степеням свободы.
Среднее значение энергии одной молекулы 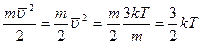 . Если бы мы посчитали отдельно
. Если бы мы посчитали отдельно 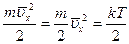 , то получили бы величину ровно в три раза меньшую, чем полная энергия. Такие же значения и для
, то получили бы величину ровно в три раза меньшую, чем полная энергия. Такие же значения и для 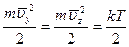 .
.
Таким образом, если вы молекула могла двигаться только вдоль оси 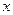 , ее средняя энергия была бы
, ее средняя энергия была бы 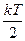 . Говорят, что у молекулы, которая может совершать только одномерные движения – одна степень свободы:
. Говорят, что у молекулы, которая может совершать только одномерные движения – одна степень свободы: 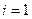 . Это значит. Что нужна только одна переменная, чтобы описать движение частицы. Для материальной точки таких переменных нужно 3:
. Это значит. Что нужна только одна переменная, чтобы описать движение частицы. Для материальной точки таких переменных нужно 3: 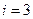 . Если же молекула может еще и вращаться, то число степеней свободы увеличивается. Средняя энергия, приходящаяся на одну степень свободы вращательного движения, а также на одну колебательную степень свободы (как потенциальной , так и кинетической) равна
. Если же молекула может еще и вращаться, то число степеней свободы увеличивается. Средняя энергия, приходящаяся на одну степень свободы вращательного движения, а также на одну колебательную степень свободы (как потенциальной , так и кинетической) равна 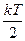 .
.
Теорема о равнораспределении энергии по степеням свободы: на все степени свободы статистической системы приходится одна и та же энергия 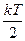 . Это не относится к потенциальной энергии системы во внешних полях.
. Это не относится к потенциальной энергии системы во внешних полях.
Средняя энергия одной молекулы 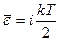 , где число степеней свободы
, где число степеней свободы 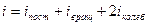 .
.
 Расхождение теории теплоемкости идеального газа с экспериментом.
Расхождение теории теплоемкости идеального газа с экспериментом.
Например, для некоторого количества идеального газа: 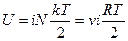 , его молярная теплоемкость
, его молярная теплоемкость 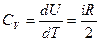
Для двух атомных молекул всего может быть 3-поступательных, 2-вращательных, 1-колебательная степени свободы. По расчетам для водорода (идеального газа) теплоемкость не зависит от температуры 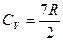 .
.
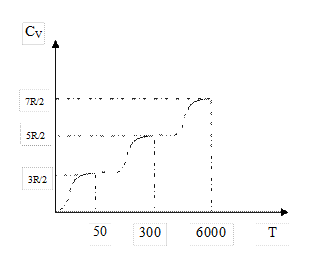
Зависимость теплоемкости молекулярного водорода от температуры, полученная в ходе экспериментов, дается на графике 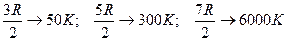 .
.
Молекула водорода ведет себя при низкой температуре как точечная частица, у которой отсутствуют внутренние движения, при нормальной температуре – как жесткая гантель и наряду с поступательным движением также совершает вращательные движения, а при очень высокой температуре к этим движениям добавляются также колебательные движения атомов, входящих в молекулу. Объяснить эту зависимость классической теории не удалось.
Отличие экспериментальной кривой от теоретической прямой имеет квантовое объяснение. При низких температурах вращательные и колебательные степени свободы «выключены», т.е. они не возбуждаются. При температурах ~116К могут возбуждаться вращательные степени свободы, а при температурах ~ 4100К возбуждаются и колебательные степени свободы. Однако переход от одного режима движения к другому происходит не скачком при определенной температуре, а постепенно в некотором интервале температур. Это объясняется тем, что при определенной температуре возникает лишь возможность перехода молекул в другой режим движения, но эта возможность не реализуется сразу всеми молекулами, а лишь их частью.
Дата добавления: 2019-10-16; просмотров: 866;
