Таким образом, зная явный вид функции для идеального газа можно определить явный вид зависимостей значения молярных теплоемкостей.
Вспомним, что вывести сами уравнения состояния на основе начал ТД нельзя. Для каждой конкретной системы они определяются эмпирически, т.е. берутся из опыта, или находятся методами статистической физики. Так что в рамках ТД они считаются заданными при определении системы.
Для не слишком крайних условий явный вид функции 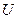 для идеального газа может быть определен исходя из теоремы о равнораспределении энергии по степеням свободы. Доказательство теоремы мы рассмотрим в разделе статистической физики, а сейчас воспользуемся теоремой. Уточним, что степенями свободы называют независимые переменные. Число степеней свободы
для идеального газа может быть определен исходя из теоремы о равнораспределении энергии по степеням свободы. Доказательство теоремы мы рассмотрим в разделе статистической физики, а сейчас воспользуемся теоремой. Уточним, что степенями свободы называют независимые переменные. Число степеней свободы 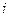 это число независимых переменных полностью задающих положение тела в пространстве.
это число независимых переменных полностью задающих положение тела в пространстве.
Теорема: на каждую степень свободы молекул при поступательном и вращательном движении приходится 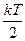 энергии. На колебательную степень свободы -
энергии. На колебательную степень свободы - 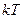 энергии.
энергии.
Энергия колебательных движений системы очень велика, она обусловлена относительным смещением ядер, и тепловое движение при обычных температурах не может возбуждать колебательные степени свободы молекул системы. Тогда, т.к. 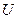 энергия всех частиц системы, то внутренняя энергия для одного моля вещества идеального газа:
энергия всех частиц системы, то внутренняя энергия для одного моля вещества идеального газа:
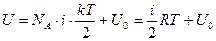 , учли, что
, учли, что 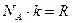 , т.к. постоянная Больцмана это универсальная газовая постоянная на одну молекулу.
, т.к. постоянная Больцмана это универсальная газовая постоянная на одну молекулу. 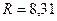 Дж/моль·К,
Дж/моль·К, 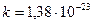 Дж/К.
Дж/К.
Тогда явный вид зависимостей для молярных теплоемкостей в процессах при постоянном объеме и давлении над идеальным газом:
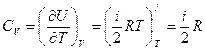
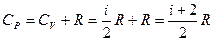 .
.
Мы видим, что достаточно знать для данной системы сорт молекул и количество степеней свободы молекулы, чтобы вычислить значения молярных теплоемкостей и внутреннюю энергию моля вещества.
| Вид молекул |
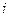 число степеней свободы число степеней свободы
| 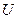 на 1 моль вещества на 1 моль вещества
|
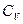
|
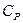
| 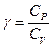
|
| Одноатомные | (поступательные ст.св.) | 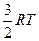
| 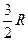
| 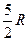
| 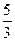
|
| Двухатомные | (3 пост.+2 вращательные ст. св.) | 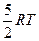
| 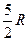
| 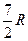
| 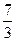
|
| Трехатомные и многоатомные | (3 пост.+3 вращательные ст. св.) | 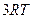
| 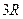
| 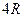
| 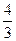
|
1. Одноатомная молекула - 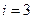 ст.св. (поступательного движения).
ст.св. (поступательного движения).
2. Двухатомная молекула - 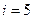 ст.св. (3 поступ.+2 вращательного движения)
ст.св. (3 поступ.+2 вращательного движения)
3. Трехатомная молекула - 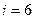 ст.св. (3 поступ. +3 вращ.)
ст.св. (3 поступ. +3 вращ.)
Дата добавления: 2019-10-16; просмотров: 734;
