Свойства карбкатионов
1.Карбкатионы образуются в полярных средах под действием поляризованных реагентов по схемам:
R3C:H + Br+ 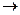 HBr + R3C+
HBr + R3C+
CH2=CH2 + Br+ 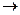 CH2+-CH2Br
CH2+-CH2Br
2.Устойчивость карбкатионов увеличивается от первичного к третичному
CH3 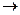 C+
C+ 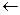 CH3 > CH3
CH3 > CH3 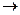 CH+
CH+ 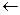 CH3 > CH3
CH3 > CH3 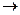 CH2+
CH2+
CH3
Причина – увеличение количества элетродонорных групп, окружающих заряженный атом углерода.
3.Химические превращения карбкатионов.
а) соединение с анионом: R+ + A- 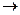 RA
RA
б) отщепление протона (от наименее гидрированного из 2-х соседних звеньев:
CH3-C+-CH2-CH3 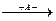 CH3-C=CH-CH3 + HA
CH3-C=CH-CH3 + HA
CH3 CH3
2-метил-2-бутен
в) присоединение к непредельному углеводороду:
R+ + CH2=CH2 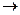 R-CH2-CH2+
R-CH2-CH2+
Рассмотрим остальные химические свойства олефинов.
4.Присоединение Н2SO4 к олефинам происходит в соответствии с правило Марковникова, т.к. реагент очень полярный, и реакция всегда идет по ионному электрофильному механизму.
HOSO2OH 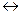 H+ + O-SO2OH
H+ + O-SO2OH
CH2 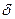 -=CH
-=CH  CH3 + H+
CH3 + H+  CH3
CH3  CH+
CH+  CH3
CH3 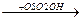 CH3-CH-CH3
CH3-CH-CH3
OSO2OH
более устойчив, чем первичный изопропиловый эфир
серной кислоты
Реакция присоединения Н2SO4 идет тем легче, чем больше радикалов окружает остаток этилена, т.е. чем больше электронная плотность у ненасыщенных атомов углерода.
 Так, СН2=СН2 (этилен) – присоединяет только концентрированную Н2SO4; СН2=СН-СН3 (пропилен) – присоединяет 78% кислоту; СН2=С-СН3 (изобутилен) – присоединяет 65% кислоту. СН3
Так, СН2=СН2 (этилен) – присоединяет только концентрированную Н2SO4; СН2=СН-СН3 (пропилен) – присоединяет 78% кислоту; СН2=С-СН3 (изобутилен) – присоединяет 65% кислоту. СН3
5.Присоединение воды требует катализатора и также происходит только в соответствии с правилом Марковникова.
СH2 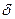 -=CH
-=CH 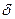 +
+ 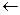 CH3 + H+OH
CH3 + H+OH 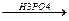 CH3-CHOH-CH3
CH3-CHOH-CH3
Пропилен ИПС
6.Гипогалоидирование – присоединение гипогалогентных кислот НОГал. (Гал2 в присутствии щелочи).
Cl : Cl + Na+OH- 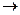 NaCl + HO-Cl+ хлорноватистая кислота
NaCl + HO-Cl+ хлорноватистая кислота
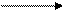 HO-Cl+ + CH3
HO-Cl+ + CH3 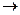 CH
CH 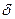 +=CH2
+=CH2 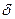 - CH3-CH-CH2
- CH3-CH-CH2
OH Cl
Пропиленхлоргидрин
Реакции окисления
Благодаря легкости разрыва p-связи олефины хорошо окисляются. Различаются следующие виды реакций окисления:
1.С разрывом только p-связи.
а) окисление по Вагнеру – действие разбавленного водного раствора KMnO4 при комнатной температуре – приводит к образованию гликолей
СH2=CH2 + O 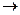 CH2-CH2 + HOH
CH2-CH2 + HOH 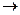 CH2-CH2
CH2-CH2
(KMnO4) O OH OH
+H2O
окись этилена этиленгликоль
б) окисление надкислотами (реакция Прилежаева) приводит к образованию окисей.
O
СH2=CH2 + C6H5-C-O-OH 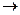 CH2-CH2 + C6H5C
CH2-CH2 + C6H5C
O O OH
надбензойная кислота бензойная кислота
2.Окисление с разрывом углеродной цепи происходит при действии сильных окислителей и при нагревании, например:
KMnO4 + H2SO4; продуктами реакций могут быть кетоны и карбоновые кислоты
O O
CH3-C=CH-CH3 + 3O 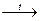 CH3-C + CH3-C
CH3-C + CH3-C
CH3 CH3 OH
2-метил-2-бутен
3.Озонирование – окисление озоном О3.
При действии озона сначала происходит его присоединение по двойной связи с образованием озонидов.
O-O-O O – O CH3
СH2=C-CH3 + O3 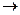 CH2-C-CH3
CH2-C-CH3 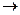 CH2 C
CH2 C
CH3 CH3 O CH3
Озониды разлагаются водой, давая альдегиды и кетоны, в зависимости от наличия заместителей
O-O-O O O
CH2-C-CH3 + H2O  H2O2 + CH2 + C-CH3
H2O2 + CH2 + C-CH3
CH3 CH3
По строению образующихся соединений можно легко установить местоположение двойной связи в олефине.
Дата добавления: 2017-06-02; просмотров: 777;
