ПОТРЕБЛЕНИЕ КИСЛОРОДА МИКРООРГАНИЗМАМИ. МАССОПЕРЕДАЧА КИСЛОРОДА И ДИОКСИДА УГЛЕРОДА В БИОТЕХНОЛОГИЧЕСКОМ ПРОЦЕССЕ
Для начала необходимо четко определить, что же такое массообмен.
Массообмен -самопроизвольный и необратимый процесс переноса массы части вещества в пространстве с неоднородным полем химического потенциала в направлении уменьшения этого химического потенциала.
Массопередача - массообмен через поверхность раздела или проницаемую стенку между двумя веществами или фазами.
Массоотдача - массообмен между движущейся средой и поверхностью раздела с другой средой.
Иными словами, в контексте биотехнологического процесса, можно сказать, что массообмен происходит между жидкими и газовыми фазами через полупроницаемую мембрану (клеточную стенку). Если рассматривать массообмен в этом ключе, то такой процесс принято называть массопередачей. Здесь внутри стенки осуществляется массопроводность, а снаружи с обеих сторон – массоотдача.
Принято считать, что диффузионные процессы, протекающие в биореакторах, не накладывают заметных ограничений на максимально проявляющуюся функциональную активность клеток и клеточных структур; главное при этом - поддержание массообмена (и прежде всего - кислорода в системе «газ – жидкость» применительно к аэробным организмам) на оптимальном уровне. При выращивании биообъекта в реакторе образуется сложная система массопередачи О2, а именно – «газ – жидкость - твердое тело», понимая под твердым телом биообъект. Названная тройная система легко расчленяется на три самостоятельные системы: «газ – жидкость», «жидкость – жидкость» и «жидкость - твердое тело». Это можно продемонстрировать следующим образом.
Перемещение О2 в этих системах неравноценно по интенсивности и зависит от растворимости газа в жидкой фазе, от мощности барботажа, размера пузырьков, скорости вращения вала и формы мешалки, химического состава питательной среды, температуры, толщины невозмущаемых слоев жидкости вокруг газового пузырька и клетки, от наличия и химического состава капсул, толщины и особенностей клеточной стенки и клеточной мембраны биообъекта и некоторых других причин. Зона невозмущенного слоя жидкости вокруг клетки может не формироваться в случаях образования ее вокруг пузырька и клетки одновременно. Тогда и путь перемещения кислорода от газового пузырька в клетку сокращается. Следует иметь ввиду, что при избытке растворенного кислорода проявляется его токсическое действие на биообъект. Вот почему желателен автоматический контроль за поддержанием оптимальных концентраций кислорода в среде для соответствующих культур. Теперь известны РО-статы (приборы для поддержания необходимого уровня растворимого О2), обеспечивающие подобный контроль.
Если молекула кислорода приобретает дополнительный электрон, то образуются свободные кислородные радикалы: супероксидный (О2) , гидроксильный (ОН-) и синглетный кислород ('О2). Эти радикалы – потенциальные деструкторы липидов, белков, нуклеиновых кислот. В частности, к ним чувствительны клеточные мембраны, в которых первичной мишенью выступают липиды, протоны которых взаимодействуют с радикалами и наступает так называемая «липидная пероксидация» с образованием пероксидов.
Известно, что с возрастанием температуры окружающей среды растворимость кислорода в воде уменьшается. Таким образом, для переноса кислорода из одной фазы в другую необходимо добиться разницы его концентрации в разных фазах с преобладанием в направлении от газового пузырька к клетке. Но поскольку растворимость кислорода в воде и водных растворах мала, необходимо подавать его в биореактор в несколько повышенных количествах, добиваясь указанной разницы в фазовых системах. При этом достигается некая критическая концентрация кислорода в культуральной среде, когда все аэробные клетки насыщаются кислородом. Для клеток микроорганизмов показатели таких концентраций приходятся на диапазон 0,003 - 0,05 ммоль/л (примерно 0,1 - 10% наибольшей растворимости кислорода в воде) или, применительно к воздуху, от 0,5 до 50%-го насыщения. Так, для клеток кишечной палочки критическая концентрация растворенного кислорода составляет 0,0082 ммоль/л при 38°С, для пеницилла – продуцента пенициллина при 24°С – около 0,022 ммоль/л, для Saccharomyces cerevisiae при 20°С - 0,0037 ммоль/л. Для некоторых мицелиальных грибов, например, Myxothecium verrucaria, удельная потребность в кислороде становится наивысшей в начале лаг-фазы размножения клеток, хотя плотность клеточной биомассы продолжает нарастать. В тоже время общая потребность в кислороде достигает максимума в конце лаг-фазы и начале стационарной фазы, то есть удельная скорость размножения клеток достигается своего пика раньше, чем скорость использования кислорода.
Скорость переноса кислорода рассчитывают на единицу объема биореактора, исходя из отношения произведения плотности потока и площади поверхности раздела фаз (газ - жидкость) к объему жидкой фазы в реакторе:
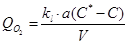
где kl – коэффициент массопередачи; С* - концентрация растворенного вещества в жидкой фазе, находящейся в равновесии с газовой фазой; а – площадь поверхности раздела фаз «газ – жидкость»; V – объем жидкой фазы. Если весь кислород, поступающий в жидкую среду, быстро усваивается клетками, тогда С = 0 и массообмен кислорода здесь максимален.
Средняя объемная скорость поглощения кислорода (Q*02 моль×с/л) в объеме V выражается уравнением:
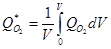
Когда гидродинамические условия в биореакторе, концентрация кислорода и отношение площади поверхности раздела фаз к объему одинаковы, тогда QО2 равна Q*О2. Обычно при вполне благоприятном аэрировании среды концентрация клеток в биореакторе может достигать величины 108/мл . Исходя из усредненных размеров клеток бактерий по диаметру 1 мкм, дрожжей – 7 мкм, нитчатых грибов – 20 мкм объемы их в процентах к объему среды составят около 0,005, 1,8 и 2 соответственно, то есть бактериальная масса будет примерно в 400 раз меньше грибной массы. Удельная поверхность раздела всех клеток будет 3 см2/см3 – для бактерий, 154 см2/см3 – для дрожжей и 30 см2/см3 – для нитчатых грибов. Следовательно, эффективная поверхность в данных примерах будет больше у дрожжей. Поэтому адекватная доставка кислорода – как лимитирующего фактора зависит от морфофункциональных особенностей культивируемого биообъекта и условий его выращивания.
На скорость потребления кислорода биообъектом влияют:
- Возраст культуры (делящиеся, или размножающиеся клетки потребляют кислорода больше, чем неделящиеся);
- Межклеточная адгезия. Когда при выраженной адгезии образуются агломераты, или комочки клеток, и, напротив, при малой или совсем не проявляющейся адгезии клетки находятся в изолированном состоянии друг от друга;
- От быстроты динамических изменений в среде выращивания биообъекта (например, в производстве экзополисахаридов, продуцируемых аэробными микроорганизмами, заметно возрастающая вязкость среды снижает поступление О2 к клеткам);
- Скорость накопления биомассы клеток – чем больше биомасса, тем скорость поглощения кислорода быстрее снижается, то есть зависимость здесь обратно пропорциональная;
- Качество источников питания, подлежащих окислению. Для сравнения можно назвать такие источники углерода, как глюкоза и предельные углеводороды из нефти. Молекулы глюкозы в питательной среде и в клетках одинаковы, так как степень восстановленности атомов углерода в данных молекулах одинаковы. Поэтому и отношение потребленного кислорода к количеству превращенной глюкозы меньше, чем это имеет место в случае использования углеводородов;
- Пеногасители, добавляемые к вспенивающимся культуральным жидкостям в процессе выращивания некоторых биообъектов. Так, например, натрия лаурилсульфат в концентрации 10 млн-1 снижает коэффициент массопередачи кислорода на 56% (в сравнении с водой);
- Продукты метаболизма, например, секретируемые белки, также снижают массопередачу кислорода.
Действие всех перечисленных факторов проявляется во времени и сказывается не только на показателях массообмена, но и теплообмена – ферментации протекают в растворах неньютоновских псевдопластичных жидкостей. В биотехнологических процессах теплообмен – постоянно учитываемый и контролируемый фактор – либо требуется подача тепла, например, в случаях стерилизации питательных сред или при культивировании анаэробов при 55 - 56°С (биологическая обработка отходов в безкислородных условиях), либо, напротив, необходим отвод тепла, образующегося в биореакторах, в которых выращивают аэробные клетки. В этих целях пользуются рубашками аппаратов, в которые подается горячая или холодная вода, змеевиками, в монтированными внутри аппаратов, «выносными» теплообменниками и др. Взаимосвязь скоростей отвода и образования теплоты описывается уравнением:
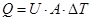
Где Q – теплота; U – общий коэффициент теплообмена; А – площадь поверхности теплообмена; DT – характерная межфазная разность температур между культуральной жидкостью и нагревающей (охлаждающей) жидкостью. Под общим коэффициентом теплообмена (U) понимают количество теплоты, передаваемое в единицу времени через единичную поверхность при разности температур в 1°С. Поэтому и теплообмен в общем виде можно определить как перераспределение тепловой энергии между взаимодействующими фазами в биореакторе. Теплообмен зависит отряда факторов:
Ламинарного или турбулентного движения теплоносителя;
- Толщины и качества материала стенок биореактора;
- Вязкости среды;
- Скорости потока при полунепрерывном и непрерывном способах культивирования биообъектов;
- Характера охлаждения биореактора.
Познание этих факторов является необходимым для конструирования оптимальных биореакторов и наиболее выгодного проведения биотехнологических процессов. Массообмен в биологических системах связан не только с доставкой кислорода к клеткам аэробных видов и теплообменом, но и с выделением диоксида углерода как конечного продукта различных катализируемых реакций, транспортом других веществ через клеточные мембраны (в том числе – анаэробных организмов).
Диоксид углерода может находиться в четырех различных формах, с различной степенью растворяясь в воде: СО32- ,НСО3-, Н2СО3 и CO2. Растворимость СО2 зависит от рН жидкости и он переносится через границу раздела фаз «газ – жидкость» лишь в растворенном виде. Для оценки газообмена при культивировании отдельных биообъектов, а также в целях контроля за микробами – загрязнителями зерна, пищевых продуктов, других жидких и плотных материалов используют специальное оборудование типа «О2/СО2-респирометров», в том числе – с компьютерным контролем.
Транспорт питательных веществ через мембраны клетки осуществляется различными путями в системах «жидкость – твердое тело»: простой (пассивной) диффузией, облегченной диффузией и благодаря активному транспорту, а у ряда эукариотических организмов – с помощью эндоцитоза. В нормальном состоянии мембрана непроницаема для большинства полярных молекул, но некоторые газы (С02,N2) и водные растворы многих веществ свободно диффундируют через мембрану благодаря соответствующим концентрационному и электрохимическому градиентам. Градиент концентраций – это разность концентраций, а диффузия – суммарное перемещение вещества, зависимое от градиента концентраций. Электрохимический потенциал складывается из суммы зарядов диффундируемых веществ. Электроны медленно проходят через мембрану, и чем больше их заряд, тем меньше транспорт. При пассивной диффузии молекула растворенного вещества не изменяет свою первоначальную молекулярную форму. Значение свободной энергии (DG) при этом всегда отрицательно.
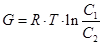
Где С1 – область пониженной концентрации вещества; С2 – область повышенной концентрации вещества. Ионизированные и полярные молекулы, плохо растворимые в полярных растворителях, обычно не транспортируются через мембрану пассивной диффузией. Для этого существует механизм облегченной диффузии, или сопряженного транспорта, когда вещество связывается с молекулой-переносчиком, локализованной на наружной поверхности мембраны. Образующийся комплекс достигает внутренней поверхности мембраны, где и разъединяется, перенеся молекулу во внутрь клетки.
Облегченная диффузия осуществляется при участии мембранных пор, генерирующих ион-проводящие пути; ионофоров - пептидов, формирующих ионные каналы (например, декапептиды – антаманид у базидиомицетов, грамицидин С у некоторых бацилл и др.); интегральных и периферических мембранных белков, действующих взаимосвязано (например, пермеазы и др.). Транспорт веществ при облегченной диффузии протекает не линейно (как при пассивной диффузии), а с определенным уровнем насыщения, после которого возрастание разности концентраций вещества не сказывается на скорости его переноса. Этот вид транспорта кинетически сходен с ферментативным катализом.
Дата добавления: 2017-03-29; просмотров: 4759;
