Электрохимическая размерная обработка металлов и сплавов
Область транспассивности (область 5 на рис. 15.7) также широко используется в практике. В этой области происходит высокоскоростное анодное растворение металлов и сплавов. Растворение с высокой скоростью широко используется в практике электрохимической размерной обработки металлов (ЭХРО). Для этого используется катод-инструмент определённой формы, изготовленный из меди или нержавеющей стали.
Устанавливается малый межэлектродный зазор (МЭЗ) между катодом-инструментом и заготовкой, катод-инструмент подводится к поверхности и через зазор с высокой скоростью прокачивается электролит. При этом происходит копирование формы электрода – инструмента (катода) на заготовке, являющейся анодом.
Чем выше плотность тока (скорость растворения), тем будет выше скорость обработки и точность копирования электрода-инструмента. Анодное растворение металла при этом происходит в области транспассивного растворения. Наличие пассивности в области низких плотностей тока и высокой скорости растворения в области транспассивности, обеспечивают высокую точность ЭХРО. Так, например, резкий переход из пассивности в область транспассивности для железа и стали в растворах NaClO3 обеспечивает высокую точность копирования при ЭХРО в таких электролитах. ЭХРО широко применяется в тех случаях когда:
- необходимо обрабатывать материалы, обработка которых затруднена на обычных металлорежущих станках;
- нужно осуществлять обработку деталей сложной формы. В этом случае посредствам копирования формы катода-инструмента на заготовке удается уменьшить количество операций, необходимых при механической обработке;
- имеет место совокупность вышеперечисленных условий.
Вопросы и упражнения
1. Найдите графически скорость коррозии (в мг/с·см2) и величину потенциала коррозии железа при водородной деполяризации, если плотность тока обмена для реакции
Fe → Fe+2 + 2 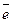
равна 10-9 А/см2, наклоны анодной и катодной тафелевских кривых равны 100 мВ/порядок, а при коррозии железа образуется его соль с концентрацией 10-1 моль/л.
2. Определите потенциал и скорость коррозии металла при кислородной деполяризации, если катодная кривая восстановления растворенного кислорода определяется кривой К на рисунке, величина равновесного потенциала металла равна – 0,35 В, плотность тока обмена для этой реакции 10-7 А/см2, а тафелевский наклон кривой анодного растворения металла равен 50 мВ/порядок.
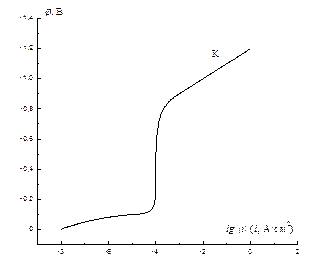
3. Анодная поляризационная кривая имеет вид, изображенный на рискнке. Определите скорость коррозии этого металла при водородной деполяризации, если плотность тока обмена выделения водорода на этом металле равна 10-8 А/см2, а тафелевский наклон кривой выделения водорода 100 мВ/порядок.
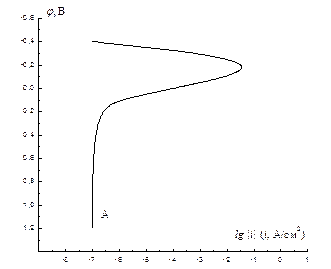
4. Определите графически потенциал и скорость коррозии металла, имеющего равновесный потенциал –0,6 В, величину тока обмена 10-6 А/см2 при тафелевском наклоне 100 мВ/порядок, если плотность предельного диффузионного тока катодного восстановления кислорода равна 10-3 А/см2, а коррозия происходит при кислородной деполяризации.
5. Определите потенциал и скорость коррозии, анодная поляризационная кривая для которой имеет вид А на рисунке, если сопряженная анодному растворению реакция восстановления окислителя имеет равновесный потенциал +0,4 В, плотность тока обмена для этой реакции равна 10-9 А/см2, а тафелевский наклон 50 мВ/порядок.
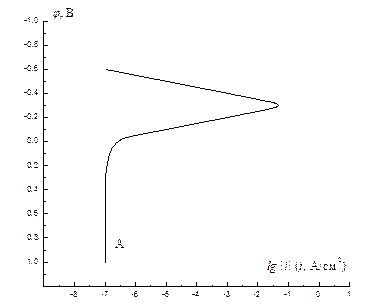
Дата добавления: 2017-01-29; просмотров: 1108;
