Строение атома и Периодический закон
Основные понятия химии
Химия – наука о составе, строении, свойствах и превращениях веществ.
Атомно-молекулярное учение.Вещества состоят из химических частиц (молекул, атомов, ионов), которые имеют сложное строение и состоят из элементарных частиц (протонов, нейтронов, электронов).
Атом – нейтральная частица, состоящая из положительного ядра и электронов.
Молекула – устойчивая группа атомов, связанных химическими связями.
Химический элемент – вид атомов с одинаковым зарядом ядра. Элемент обозначают
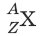
где X – символ элемента, Z – порядковый номер элемента в Периодической системе элементов Д.И. Менделеева, A – массовое число. Порядковый номер Z равен заряду ядра атома, числу протонов в ядре атома и числу электронов в атоме. Массовое число A равно сумме чисел протонов и нейтронов в атоме. Число нейтронов равно разности A – Z.
Изотопы – атомы одного элемента, имеющие разные массовые числа.
Относительная атомная масса(Ar) – отношение средней массы атома элемента естественного изотопического состава к 1/12 массы атома изотопа углерода 12С.
Относительная молекулярная масса(Mr) – отношение средней массы молекулы вещества естественного изотопического состава к 1/12 части массы атома изотопа углерода 12С.
Атомная единица массы(а.е.м) – 1/12 часть массы атома изотопа углерода 12С. 1 а.е. м = 1,66 × 10-24 г.
Моль – количество вещества, содержащее столько структурных единиц (атомов, молекул, ионов), сколько содержится атомов в 0,012 кг изотопа углерода 12С. Моль – количество вещества, содержащее 6,02 • 1023 структурных единиц (атомов, молекул, ионов).
n = N/NA , где n – количество вещества (моль), N – число частиц, a NA – постоянная Авогадро. Количество вещества может обозначаться также и символом v.
Постоянная Авогадро NA = 6,02 • 1023 частиц/моль.
Молярная масса M (г/моль) – отношение массы вещества m (г) к количеству вещества n (моль):
М = m/n, откуда: m = М • n и n = m/М.
Молярный объем газаVM (л/моль) – отношение объема газа V (л) к количеству вещества этого газа n (моль). При нормальных условиях VM = 22,4 л/моль.
Нормальные условия:температура t = 0°C, или Т = 273 К, давление р = 1 атм = 760 мм. рт. ст. = 101 325 Па = 101,325 кПа.
VM = V/n, откуда: V = VM • n и n = V/VM.
В результате получается общая формула:
n = m/M = V/VM = N/NA.
Эквивалент– реальная или условная частица, взаимодействующая с одним атомом водорода, или замещающая его, или эквивалентная ему каким-либо другим способом.
Молярная масса эквивалентов Мэ – отношение массы вещества к количеству эквивалентов этого вещества: Мэ = m/n (экв ).
В реакциях обмена зарядов молярная масса эквивалентов вещества
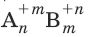
с молярной массой М равна: Мэ = М/(n × m).
В окислительно-восстановительных реакциях молярная масса эквивалентов вещества с молярной массой М равна: Мэ = М/n(ē), где n(ē) – число переданных электронов.
Закон эквивалентов– массы реагирующих веществ 1 и 2 пропорциональны молярным массам их эквивалентов. m1/m2 = МЭ1/МЭ2, или m1/МЭ1 = m2/МЭ2, или n1 = n2, где m1 и m2 – массы двух веществ, МЭ1 и МЭ2 – молярные массы эквивалентов, n1 и n2 – количества эквивалентов этих веществ.
Для растворов закон эквивалентов может быть записан в следующем виде:
cЭ1 • V1 = cЭ2 • V2 , где сЭ1, сЭ2, V1 и V2 – молярные концентрации эквивалентов и объемы растворов этих двух веществ.
Объединенный газовый закон: pV= nRT, где p – давление (Па, кПа), V – объем (м3, л), n – количество вещества газа (моль), T – температура (К), T (К) = t (°C) + 273, R – константа, R = 8,314 Дж/(К × моль), при этом Дж = Па • м3 = кПа • л.
Строение атома и Периодический закон
Корпускулярно-волновой дуализмматерии – представление о том, что каждый объект может иметь и волновые, и корпускулярные свойства. Луи де Бройль предложил формулу, связывающую волновые и корпускулярные свойства объектов: λ = h/(mV), где h – постоянная Планка, λ – длина волны, которая соответствует каждому телу с массой m и скоростью V. Хотя волновые свойства существуют для всех объектов, но наблюдаться они могут лишь для микрообъектов, имеющих массы порядка массы атома и электрона.
Принцип неопределенности Гейзенберга: Δ(mVx) • Δх > h/2n или ΔVx • Δx > h/(2πm), где m – масса частицы, x – ее координата, Vx – скорость в направлении x, Δ – неопределенность, погрешность определения. Принцип неопределенности означает, что нельзя одновременно сколь угодно точно указать положение (координату x) и скорость (Vx) частицы.
Частицы с маленькими массами (атомы, ядра, электроны, молекулы) не являются частицами в понимании этого механикой Ньютона и не могут изучаться классической физикой. Они изучаются квантовой физикой.
Главное квантовое число n принимает значения 1, 2, 3, 4, 5, 6 и 7, соответствующие электронным уровням (слоям) К, L, M, N, О, Р и Q.
Уровень– пространство, где расположены электроны с одинаковым числом n. Электроны разных уровней пространственно и энергетически отделены друг от друга, поскольку число n определяет энергию электронов Е (чем больше n, тем больше Е) и расстояние R между электронами и ядром (чем больше n, тем больше R).
Орбитальное (побочное, азимутальное) квантовое число l принимает значения в зависимости от числа n: l = 0, 1,…(n – 1). Например, если n = 2, то l = 0, 1; если n = 3, то l = 0, 1, 2. Число l характеризует подуровень (подслой).
Подуровень – пространство, где расположены электроны с определенными n и l. Подуровни данного уровня обозначаются в зависимости от числа l: s – если l = 0, p – если l = 1, d – если l = 2, f – если l = 3. Подуровни данного атома обозначаются в зависимости от чисел n и l, например: 2s (п = 2, l = 0), 3d (n = 3, l = 2) и т. д. Подуровни данного уровня имеют разную энергию (чем больше l, тем больше Е): Es< E < ЕА < … и разную форму орбиталей, составляющих эти подуровни: s-орбиталь имеет форму шара, p -орбиталь имеет форму гантели и т. д.
Магнитное квантовое число m1 характеризует ориентацию орбитального магнитного момента, равного l, в пространстве относительно внешнего магнитного поля и принимает значения: – l,…-1, 0, 1,…l, т. е. всего (2l + 1) значение. Например, если l = 2, то m1 = -2, -1, 0, 1, 2.
Орбиталь(часть подуровня) – пространство, где расположены электроны (не более двух) с определенными n, l, m1. Подуровень содержит 2l+1 орбиталь. Например, d – подуровень содержит пять d-орбиталей. Орбитали одного подуровня, имеющие разные числа m1, имеют одинаковую энергию.
Магнитное спиновое числоms характеризует ориентацию собственного магнитного момента электрона s, равного ½, относительно внешнего магнитного поля и принимает два значению: +½ и _½.
Электроны в атоме занимают уровни, подуровни и орбитали согласно следующим правилам.
Правило Паули:в одном атоме два электрона не могут иметь четыре одинаковых квантовых числа. Они должны отличаться по меньшей мере одним квантовым числом.
Из правила Паули следует, что на орбитали могут располагаться не более двух электронов, на подуровне может содержаться не более 2(2l + 1) электронов, на уровне содержится не более 2n2 электронов.
Правило Клечковского:заполнение электронных подуровней осуществляется в порядке возрастания суммы (n + l), а в случае одинаковой суммы (n + l) – в порядке возрастания числа n.
Графическая форма правила Клечковского.

Согласно правилу Клечковского, заполнение подуровней осуществляется в следующем порядке: 1s, 2s, 2р, 3s, Зр, 4s, 3d, 4р, 5s, 4d, 5р, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p, 8s,…
Хотя заполнение подуровней происходит по правилу Клечковского, в электронной формуле подуровни записываются последовательно по уровням: 1s, 2s, 2p, 3s, 3p, 3d, 4s, 4р, 4d, 4f и т. д. Таким образом, электронная формула атома брома записывается следующим образом: Br(35ē) 1s22s22p63s23p63d104s24p5.
Электронные конфигурации ряда атомов отличаются от предсказанных по правилу Клечковского. Так, для Сr и Cu:
Сr(24ē) 1s22s22p63s23p63d54s1 и Cu(29ē) 1s22s22p63s23p63d104s1 .
Правило Хунда (Гунда):заполнение ор-биталей данного подуровня осуществляется так, чтобы суммарный спин был максимален. Орбитали данного подуровня заполняются сначала по одному электрону.
Электронные конфигурации атомов можно записать по уровням, подуровням, ор-биталям. Например, электронная формула Р(15ē) может быть записана:
а) по уровням)2)8)5;
б) по подуровням 1s22s22p63s23p3 ;
в) по орбиталям

Примеры электронных формул некоторых атомов и ионов:
V(23ē) 1s22s22p63s23p63d34s2 ;
V3+(20ē) 1s22s22p63s23p63d24s0 .
Химическая связь
Дата добавления: 2016-04-23; просмотров: 986;
