Структурные полисахариды злаковых культур – овса и ячменя и их биоконверсия
В зерне злаковых культур одну из основных частей зерновки представляют собой оболочки. Они различаются по структуре и свойствам. Оболочки выполняют защитную функцию, их делят на плодовые и семенные. По мнению Хинтона в оболочках сосредоточено до 70% клетчатки и большая часть золообразующих элементов. По данным Н.А. Родионовой клеточная стенка оболочек зерна злаков (пшеничное зерно) содержит 64% арабиноглюкуронксилана, 29% целлюлозы, 6% нецеллюлозного глюкана, 8,3% лигнина и 9,2% белка [259, 260].
Целлюлоза составляет основу оболочек зерна злаковых культур и является основным структурообразующим компонентом клеточных стенок. Общее число глюкозных остатков в макромолекуле целлюлозы порядка 6000-12000, что соответствует молекулярной массе 1-2 млн. единиц [19]. Целлюлоза - представляет собой линейный полисахарид, состоящий из остатков β- D глюкопиранозы, основным повторяющимся структурным элементом полисахарида является целлобиоза. Элементарные звенья макромолекул целлюлозы имеют конформацию кресла, то есть гидроксильные группы у первого и четвертого атомов глюкозы отличаются расположением относительно плоскости кольца. Остатки глюкозы в ангидроглюкозной цепи повернуты относительно друг друга на 180º. Ангидроглюкозные цепи стабилизированы внутримолекулярными водородными связями между остатками глюкозы при взаимодействии гидроксильной группы ОН – при шестом, втором и третьем углеродных атомах, и кислорода кольца. Следовательно, β-1-4 глюкан представляет собой жесткую ленту. Конформация целлюлозы дает возможность реализации внутри- и межмолекулярных взаимодействий [64, 73, 102, 288, 290].
Как и все гидрофильные линейные полимеры, целлюлоза обладает склонностью к образованию элементарных фибрилл (из 40-60 молекул), в которых группы параллельно расположенных цепей макромолекул связаны между собой множеством водородных связей. Первичная фибрилла представляет собой наименьшее надмолекулярное звено целлюлозы. Первичные фибриллы целлюлозы образуются благодаря межмолекулярным взаимодействиям кислорода одной цепи и гидроксильной группы другой. Современная точка зрения на структуру целлюлозы имеет в своей основе теорию аморфно-кристаллического строения. Макромолекулы целлюлозы в первичных фибриллах образуют однородные высокоупорядоченные кристаллические зоны, которые чередуются с неоднородными менее упорядоченными аморфными зонами.
В кристаллических зонах целлюлозы существует трехмерный дальний порядок в расположении цепей целлюлозы. В аморфных участках дальний порядок отсутствует и сохраняется лишь общая продольная направленность цепей. В аморфных участках относительно легко могут происходить реакции целлюлозы с другими веществами. Наличием кристаллических областей обусловлена высокая механическая прочность и нерастворимость целлюлозы, тогда как набухание и высокая реакционная способность связана с более легкопроницаемыми для химических реагентов аморфными участками. [106]. Первичные фибриллы целлюлозы соединяются между собой с помощью водородных связей в микрофибриллы, которые являются основными звеньями строения волокон целлюлозы. Микрофибриллы состоят из нескольких первичных фибрилл, поперечное сечение их составляет примерно 100х200А, длина - около 600А. Целлюлозные волокна характеризуются индексом кристалличности. Этот показатель характеризует плотность упаковки целлюлозы и соотношение аморфных и кристаллических участков. Участки микрофибрилл, в которых ангидроглюкозные цепи располагаются в параллельных друг другу плоскостях, образуют кристаллы, называемые мицеллами. Межмицеллярные промежутки называются паракристаллическими и лишь они доступны для воды.
Между первичными фибриллами в микрофибрилле находится лигнин и гемицеллюлоза. Гетерогенность структуры целлюлозы, наличие кристаллических и аморфных областей, а также межфибриллярных капилляров приводит к тому, что волокна целлюлозы имеют макро - и микропоры. Пористая система в целлюлозе организована так, что проходит через всю ее структуру как сложная сеть каналов различного диаметра [106, 290, 291].
Гемицеллюлозы представляют собой гетерополисахариды, содержащие остатки различных гексоз, пентоз и их производных, со степенью полимеризации от 50 до 200. Гемицеллюлозы фракционируют на гемицеллюлозы А, экстрагируемые разбавленной щелочью (5-10%), и гемицеллюлозы Б, экстрагируемые более концентрированной щелочью (17,5-24%). В гидролизатах гемицеллюлоз различных растений идентифицируют следующие моносахара: глюкозу, галактозу, арабинозу, ксилозу, маннозу и уроновые кислоты [111, 304, 312, 339, 350, 384]. Среди гемицеллюлоз наиболее распространены различные ксиланы (арабиноксиланы, глюкуроноксиланы, арабиноглюкуроноксиланы). В меньшем количестве встречаются маннаны (галактоманнаны, глюкоманнаны, глюкогалактоманнаны) и галактаны (арабиногалактаны и другие). У однодольных растений главным компонентом гемицеллюлоз являются ксиланы, в основе строения которых лежит β-1,4-ксилановый остов с ответвлениями, представляющими собой одиночные 4-0-метилглюкуронозильные остатки, связанные с С-2-атомами ксилозы остова. Арабиноглюкуроноксилан водородными связями соединен с цепями микрофибрилл целлюлозы. Водородные связи образуются за счет кислорода глюкозидных связей цепи ксилоглюкана и первичной гидроксильной группы глюкозного остатка при углеродном атоме целлюлозы. Арабиноглюкуроноксилан имеет боковые цепи из остатков уроновых кислот и нейтральных сахаров [260, 352]. Химические свойства гемицеллюлоз обусловлены наличием в мономерах ряда гидроксильных групп, карбоксильных групп и полуацетальной гликозидной связи. Часть этих группировок метоксилирована и ацетилирована (ксиланы, маннаны), часть образует сложноэфирные связи с другими компонентами клеточных стенок – лигнином, белками. Возможны простые эфирные ацетальные и другие связи. Арабиноксиланы эндосперма пшеницы, тритикале, овса, ячменя ковалентно связаны с феруловой кислотой [364].
В небольшом количестве в оболочках представлены пектиновые вещества и лигнин. Пектиновые вещества содержатся в зерне пшеницы в форме нерастворимого протопектина, который является цементирующим материалом, и в форме растворимого пектина. Главная цепь пектиновых веществ состоит из рамногалактурона, в котором остатки галактуроновой кислоты связаны между собой 1,4-гликозидными связями и с рамнозилом 1,2-гликозидными связями [356]. Наличие рамнозы в цепи полисахарида нарушает линейную структуру макромолекул. К главной цепи ковалентно присоединены боковые цепи – арабинан, галактан или их комбинация [375, 398]. Карбоксильные и гидроксильные группы макромолекул рамногалактуронана обусловливают водосвязывающую способность пектиновых веществ.
Лигнин - один из важнейших компонентов растительной биомассы, основными его предшественниками являются, n-кумаровый, конифериловый и синаповый спирты. Макромолекула лигнина образуется в результате сочетания феноксильных радикалов. Большинство мономерных единиц связано прочными углеродными связями дифенильного или алкиларильного типа. Существующие простые эфирные связи, за исключением α- арилового простого эфира, тоже довольно устойчивы к гидролизу. Степень полимеризации лигнина значительно меньше, чем у целлюлозы и гемицеллюлозы и равна 3. Лигнин заполняет межфибриллярное пространство кристаллической структуры целлюлозы и тем самым в той или иной степени определяет доступность элементарной целлюлозы для ферментных комплексов.[19, 105, 270,272,310].
В состав оболочек входят также в небольшом количестве белки. Белки оболочек представлены структурным арабиногалактановым гликопротеидом экстенсином, до 50% аминокислот в котором составляет гидроксипролин, кроме того, этот белок обеднен метионином. Общее содержание углеводной части составляет около 45% от массы гликопротеида, а по некоторым данным – даже 74%. Углеводная часть белка представлена арабинотетраолигосахаридами, состоящими из остатков арабинозы, соединенных β-(1,2) и β-(1,3)-связями. Арабинотетраолигосахариды присоединены к гидроксильным остаткам гидроксипролина с помощью гликозидных связей. Вытянутые молекулы экстенсина образуют стержень, а тетрасахариды стабилизируют полипептидную цепь в конформации жесткого прута [260]. На рисунке 1 представлена схема строения первичной клеточной стенки по Albersheim [349].
Поперечный и продольный слои плодовой оболочки связаны непрочно и при увлажнении между ними образуются пустоты [9].
Химические соединения, входящие в состав оболочек зерна, выполняют различные физиологические функции. Целлюлозные фибриллы представляют структурообразующий и каркасный элемент; гемицеллюлозы, и пектиновые вещества участвуют в процессе осморегуляции, адсорбции, при растяжении растительной клетки, и в формировании тургора; лигнин и структурные белки формируют физиологический и биохимический барьеры от микробиологической инфекции из-за структурной прочности и токсичности их для микроорганизмов [323].
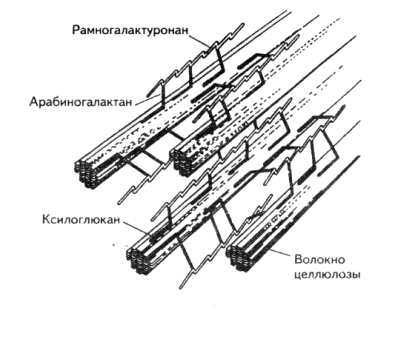
Рисунок 1 – Строение первичной стенки растительной клетки (по Albersheim P.).
В настоящее время известны лишь основные черты взаимодействия различных полисахаридов и гликопротеидов в клеточных стенках. На поверхности микрофибрилл целлюлозы вероятно имеется ксилоглюкановый монослой, формирующийся за счет водородных связей. Вполне вероятно также нековалентное связывание целлюлозой определенной части глюкуроноарабиноксилана – другой гемицеллюлозы клеточных стенок. Обнаружены и ковалентные связи между ксилоглюкановыми цепями и пектиновыми полисахаридами. Наиболее значимый тип нековалентной связи осуществляется посредством ионов кальция. Ион кальция хелатирует карбоксильные группы четырех галактуронозильных остатков двух соседних полисахаридных цепей. [352, 404].
В клеточных стенках сосредоточены также слизистые вещества, которые являются продуктами нормального метаболизма растений и служат как пищевым резервом, так и веществами, удерживающими воду. Слизистые вещества злаков были выделены более 100 лет назад. В 1988 году O, Sullivan выделил из ячменя, пшеницы и ржи две фракции слизистых веществ ά- и β-амилан. В зарубежных работах слизистые вещества называют водорастворимыми пентозанами. По определению Голенкова В.Ф., под слизистыми веществами понимают группу водорастворимых гетерополисахаридов, состоящих, главным образом, из пентозанов и гексозанов, важнейшей особенностью которых является высокая вязкость водных растворов [44].
Кретович В.Л. и Петрова И.С. установили, что по мере созревания зерна понижается количество водорастворимых пентозанов, так как они расходуются на образование гемицеллюлоз, а при прорастании зерна этот процесс протекает в обратном направлении [125]. При частичном ферментативном гидролизе гемицеллюлозы разрушаются до водорастворимых пентозанов [304]. Структура молекул водорастворимых пентозанов имеет разветвленное строение. Установлено [408], что нерастворимые в 80% растворе сернокислого аммония слизистые вещества содержат высокомолекулярный пентозан. Пентозановая фракция слизистых веществ, состоящая из арабинозы и ксилозы, входит в группу растительных ксиланов, которые имеют ксилозную цепь с присоединенными цепями других нейтральных сахаров и уроновых кислот. Ксилозная цепь образована остатками β-Д-ксилопиранозы. Боковые цепи образованы L-арабинофуранозой. Пентозановая фракция зерновых культур различается степенью полимеризации и числом боковых цепей. Вторая фракция слизистых веществ, глюкозан, обозначаемая часто как β-глюкан, имеет неразветвленную цепь из остатков β-Д-глюкопиранозы, связанных в положении 1-3, 1-4 и, возможно, незначительно 1-6. Однако структура арабиноксилана и глюкозановой фракции окончательно не выяснена. Предполагается, что различия в физических свойствах зависят от соотношения пентозановой и глюкозановой фракций, от степени разветвления арабиноксилановой фракции и от степени полимеризации, то есть от размера молекул. Слизистые вещества уже при комнатной температуре поглощают до 800% воды, образуя вязкие растворы. Вязкость растворов зависит от содержания пентозанов и количества белков в слизистых веществах [412].
Гидротермическая обработка растительного сырья приводит к деструкции некрахмальных полисахаридов. Наиболее устойчивым компонентом клеточных стенок является целлюлоза. При гидротермической обработке целлюлоза частично набухает и возрастает ее эластичность. Деструкция гемицеллюлоз начинается при температуре 70-80ºС. Процессу подвергаются обе фракции гемицеллюлоз, образующиеся при этом растворимые продукты переходят в раствор [406]. Наряду со снижением количества общих гемицеллюлоз происходит увеличение содержания легкогидролизуемой фракции А за счет увеличения растворимости при тепловой обработке трудногидролизуемой фракции Б. Деструкция протопектина начинается при температуре 60ºС. В процессе деструкции протопектина при гидротермической обработке происходит распад связей между цепями рамногалактуронана с другими компонентами клеточных стенок и гидролиз самих цепей макромолекул рамногалактуронана, что приводит к образованию растворимых продуктов деструкции с различной молекулярной массой. Деструкция пектиновых веществ и гемицеллюлоз приводит к нарушению всего полисахаридного комплекса матрикса клеточных стенок [164]. Известно, что увеличение содержания слизистых веществ наблюдается не только при гидротермической обработке, но и при проращивании зерна злаковых культур в результате гидролиза гемицеллюлоз. При этом существенно снижается вязкость слизистых веществ, что обусловлено образованием низкомолекулярных продуктов [148]. Для ускорения процесса деструкции некрахмальных полисахаридов и проведения его при более низких температурах используют ферментные препараты целлюлолитического действия.
Характерным свойством, присущим целлюлазному комплексу, является явление синергизма, выражающееся во взаимном увеличении скорости и глубины гидролиза целлюлозы до конечных продуктов при совместном действии ферментов целлюлазного комплекса по сравнению с индивидуальным действием этих компонентов [19, 288, 289].
Основные минимальные требования к составу целлюлазного комплекса заключаются в том, чтобы он имел высокую эндоглюканазную и целлобиазную активность [272, 290].
Некрахмальные полисахариды или как их называют некоторые из авторов - гумми-вещества, выделенные из различных хлебных злаков содержат β-глюкан и пентозы, дающие при кислотном гидролизе ксилозу и арабинозу. В гумми-веществах, выделенных из эндосперма ячменя, β-глюкан составляет 80-85%. из ячменя β-глюкана можно выделить до 0,444%, из овса - 0,262% и из других злаков- < 0,1%.
Гемицеллюлоза состоит из левовращающего глюкана и пентозанов, дающих при кислотном гидролизе ксилозу и арабинозу.
В зерне злаков различают два типа гемицеллюлоз - мякинный и эндосперменный. Гемицеллюлоза первого типа находится в оболочке зерна и содержит до 70% ксилана, 15-20% арабана, 3-5% уронового альдегида и только 6% глюкана. Она относительно устойчива к действию ферментов и при проращивании зерна не играет важной биологической роли. Гемицеллюлоза второго типа входит в состав клеточных стенок эндосперма. Она содержит 77% глюкана, 17% ксилана и 6% арабана. Эта гемицеллюлоза экстрагируется разбавленной щелочью и переводится в растворимое состояние под действием ферментов. В гидролизатах из отрубей и зерновой шелухи часто содержатся также в небольшом количестве галактоза и 3-5% уроновых кислот.
Таким образом, гемицеллюлоза и гумми-вещества зерен хлебных злаков представляют собой сложные смеси некрахмальных полисахаридов, основными компонентами которых является левовращающий глюкан и пентозы. Несмотря на различную растворимость гемицеллюлозы и гумми-вещества ячменя они, по-видимому, значительно не различаются между собой химическим строением индивидуальных полисахаридов, входящих в их состав. Аспиналл [17,18](считает более правильным классифицировать эти полисахариды не по их растворимости, а по химическому строению, и делит их на два класса: класс β-глюканов и класс пентозанов.
Ячменный β-глюкан, как показали Прис и Мак-Лео., сконцентрирован в эндосперме. Стенки клеток эндосперма построены в основном из нерастворимого в воде β-глюкана, входящего во фракцию гемицеллюлозы.
β-глюкан ячменя представляет собой β-глюкозид неразветвленной линейной цепи [38], в которой звенья из глюкозы соединены β-1,3- и β-1,4-связями. В β-глюкозиде содержится примерно 70% β-1,4-связей и 30% β-1,3-связей [37]. Причем в молекуле β-глюкана имеются повторяющихся β-1,3-связей или число их незначительно [22,33].
На основании расчетов предполагается, что молекула β-глюкана состоит, очевидно, из единиц, содержащих две β-1,4-связи, и единиц, содержащих три β-1,4-связи, разделенных одиночными β-1,3-связями.
β-глюкан обладает свойствами, которые очень важны для его биологических функций. Он обеспечивает прочность клеточных стенок и не может образовывать кристаллические формы, как целлюлоза. По-видимому, это и обуславливает его хорошую растворимость в воде и легкую гидролизуемость ферментами [29].
Как показали Прис и Хобкирк, основная часть пентозанов ячменя находится в оболочке зерна и около 25% - в клеточных стенках эндосперма. Большая часть пентозанов нерастворима в воде.
Ячменный арабиноксилан состоит из главной цепи единиц β-D-ксилопиранозы, соединенных между собой β-1,4 связями, и боковых цепей, состоящих из L-арабинофуранозы. Боковые цепи присоединяются к ксилопиранозной цепи через β-1,2- и β-1,3- связями.
Подобную структуру имеют также щелочерастворимые пентозаны эндосперма овса, а по данным Бишона и Витакера, пшеничной соломы и ржаной муки.
Более сложное строение имеют арабиноксиланы оболочек зерна и зерновой шелухи, в состав боковых цепей которых могут входить ксилоза в пиранозной форме, а также метиловые эфиры глюкуроновой кислоты, присоединенные к главной цепи ксилана β-1,3- и β-1,2-связями.
Таким образом, различия в структуре ксиланов обусловлены природой сахарного остатка в боковых цепях этих полисахаридов, а также распределением и длиной боковых цепей.
По данным различных исследователей, молекулярная масса β-глюкана колеблется от нескольких десятков до сотен тысяч, что, очевидно, обуславливается способами его получения и очистки. Вычисленная Игараши и сотр. [26]. На основании данных седиментации и диффузии молекулярная масса β-глюкана равна 220000. Разные фракции гумми-веществ, выделенные Дьюртоффом, имели молекулярные массы, равные 50000, 190000 и 200000.
Молекулярная масса ячменного арабиноксилана несколько меньше, и по определению Подрацкого, равна 58800.
Нерастворимые в воде фракции β-глюкана и арабиноксилана, входящие в состав гемицеллюлозы эндосперма, очевидно, имеют большую молекулярную массу, чем эти же соединения, входящие в состав гумми-веществ. Массарт и Ван Сумере считают β-глюкан и арабиноксилан гемицеллюлозы предшественниками полисахаридов, входящих в состав гумми-веществ. Таким образом, гумми-вещества являются как бы декстринами гемицеллюлозы.
Разница в растворимости гумми-веществ и гемицеллюлозы может быть обусловлена степенью ветвления молекулы арабиноксилана [34], а также соединением полисахарида с белком.
Водорастворимые некрахмальных полисахариды ячменя и овса, особенно β-глюкан, образует очень вязкие растворы. Так, по данным Сперроу, удельная вязкость 0,5%-ного раствора β-глюкана, выделенного из разных сортов канадского ячменя, варьирует от 2,04 до 6,5.
Содержание гумми-веществ в ячмене и овсе подвержено большим колебаниям. По данным Приса, количество гумми-веществ у разных злаков составляет 0,32-1,35%. В ячменях, исследованных Лачзингером [29], их содержалось 6,2-6,7%.
В пяти сортах ячменя, исследованных Мальцевым и И Семеновой содержание гумми-веществ в расчете на сухое вещество колебалось от 1,42 до 1,95%. Шустер и Нарцисс установили, что количество гумми-веществ в ячмене и овсе зависит от сорта, погодных условий и условий произрастания. Ячмень и овес, выращенные при жаркой сухой погоде, содержат больше гумми-веществ. Выход экстракта ниже из ячменей, богатых гумми-веществами. Гумми-вещества труднорастворимых высокобелковых ячменей медленнее разрушаются при проращивании зерна. Большое влияние на этот процесс оказывает влажность ячменя, который необходимо замачивать более длительное время и до влажности 46%.
Наибольшим изменениям в гумми-веществах подвержен β-глюкан, количество которого может быть от 0,968 до 1,506 мг на 100г ячменя, количество пентозанов изменяется значительно меньше- от 0,145 до 0,176 мг 100г ячменя. Корреляция между содержанием гумми-веществ и пивоваренными качествами ячменя, как правило, не наблюдается, хотя имеются сведения о том, что процесс солодоращения происходит лучше у ячменя с невысоким содержанием гумми-веществ.
По данным Огурцовой, Лифшиц др. [10], в ячмене содержится 6,2-8,4%, а в солоде-5,8-7,8% гемицеллюлоз. При этом общее количество гемицеллюлоз в ячмене составляет в среднем 6,4%, а в эндосперме - 5,11% к сухому веществу. Количество гемицеллюлоз в оболочках ячменя и солода практически одинаково.
Поляковым и др. в ячмене найдено от 0,4 до 1,0% нерастворимого β-глюкана.
По данным Приса, в злаках содержатся следующие количества β-глюкана и арабиноксилана и представлены в таблице 6:
Таблица 6 – Сравнительная характеристика содержания β-глюкана и арабиноксилана (%) в различных зерновых культурах
| Злаки | β-глюкан | Арабиноксилан |
| Ячмень | 0,80 | 0,29 |
| Овес | 0,67 | 0,21 |
| Рис | 0,04 | 0,64 |
| Пшеница | 0,06 | 0,35 |
| Рожь | 0,18 | 0,65 |
В шести сортах ржи, произрастающих в России, содержание гумми-веществ, по данным Кошевой и др., колеблется от 4,4 до 7,4%, а гемицеллюлоз от 8,4 до 14,4%. Относительная вязкость 0,5%-ных растворов гумми-веществ в зависимости от сорта ржи составляет 1,654-2,149, а растворов гемицеллюлоз - 1,846-2,728. При кислотном гидролизе гумми-вещества и гемицеллюлозы образуют глюкозу, арабинозу и ксилозу, при этом в гумми-веществах превалирует содержание глюкозы (36-70%), а в гемицеллюлозах-пентоз (68-89%).
К некрахмальным полисахаридам, содержащимся в ячмене и овсе, относятся также целлюлоза и пектиновые вещества. В ячменном зерне содержится 3,7-7,0% целлюлозы [4], которая составляет основу оболочки ячменя и овса, фильтрующего остатка слоя дробины. Целлюлоза построена из глюкозных остатков, связанных друг с другом β-1,4-гликозидной связью. Она весьма устойчива к действию ферментов.
В результате ферментативного (частичного) гидролиза целлюлозы образуется смесь олигосахаридов, трисахаридов и тетрасахаридов, остальные 50% составляет целлобиоза. При полном гидролизе минеральными кислотами целлюлоза расщепляется до глюкозы.
Ксилан - полисахарид, содержащий преимущественно ксилозу (D-ксилопиранозу). Маннан – полисахарид, содержащий преимущественно маннозу. Галактаны содержат очень мало галактозы. Пектиновые вещества в ячмене содержатся в форме нерастворимого протопектина, который входит в состав клеточных стенок, являясь цементирующим материалом, и в форме растворимого пектина. Растворимый пектин это полисахарид, состоящий из соединенных между собой остатков галактуровой кислоты, часть карбоксильных групп которых связана с метиловым спиртом. При полном гидролизе пектина образуется α-галактуроновая кислота и метиловый спирт.
Количество пектиновых веществ в зерне ячменя и овса зависит от сорта и условий произрастания и колеблется от 1,2 до 6,5%, а количество растворимой формы пектина - от 0,6 до 1,7% на сухое вещество зерна. Высокое содержание пектиновых веществ ухудшает солодовые качества ячменя. По данным Дроздовой и Мальцева [5], количество пектиновых веществ в готовом солоде снижается на 75%. Пектиновые вещества способствуют пенообразованию, осаждают тяжелые металлы, но в то же время, входя в состав коллоидной мути пива, снижают его стойкость. При разрушении пектиновых веществ под действием ферментов солода и ферментных препаратов микробиального происхождения снижается вязкость сусла, улучшается осахаривание крахмала.
Ферментативное расщепление этих веществ в значительной степени зависит от их химического состава и физического строения, от структуры клетки, а иногда и от макроструктуры. В клеточных стенках, содержащих лигнин, эти вещества, как правило, взаимосвязаны. Так, например, у целлюлозы аморфные фракции под воздействием ферментов быстрее расщепляются, чем кристаллические. У кристаллических ксиланов были выявлены большие различия, тогда как лихенин, хотя он хорошо диспергирует, ведет себя аналогично целлюлозе. В одеревеневших субстратах лигнин может физически связывать часть сахаридов.
В связи с вышеизложенным можно сделать вывод о перспективгости промышленного биокатализа как способа интенсификации технологических процессов переработки целого зерна овса и ячменя и получения биомодифицированных продуктов с заданными функционально технологическими свойствами.
Дата добавления: 2016-09-28; просмотров: 3996;
