По химической структуре (окончание)
| 3. | Этиленимины: | имифос, тиотепа (тиофосфамид, ТиоТЭФ), фотретамин, бензотеф, фторбензотеф |
| 4. | Производные нитрозомочевины: | карамустин, ломустин, нимустин, гидроксиуреа, нитрозометилмочевина, фотемустин (мюстофоран) |
| 5. | Другие алкилирующие средства: | эстрамустин (эстрацит), дакарбазин, темозоломид. |
Толчком к применению алкилирующих соединений для лечения онкологических больных послужил тот факт, что у боевого отравляющего вещества (БОВ) иприта была обнаружена способность сильно подавлять лейкопоэз. Но из-за высокой токсичности применение его в медицинской практике было невозможно. Для синтеза хлорэтиламинов, получивших широкое распространение в терапии опухолевых заболеваний, был получен предварительно гораздо менее токсичный азотистый иприт:
| СН2 СН2Cl | СН2 СН2Cl | |
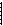
| 
| |
 S S
|  N-CH2CH2Cl (R) N-CH2CH2Cl (R)
| |
| СН2 СН2Cl | СН2 СН2Cl | |
| иприт | азотистый иприт | |
| [бис-(b-хлорэтил)-сульфид] | (трихлорэтиламин) | |
В 1943 г. у азотистого иприта была установлена способность вызывать лейкопению и подавлять опухолевый рост.
Таким образом, все хлорэтиламины являются производными азотистого иприта, различающимися значением R. Первым препаратом этой группы был эмбихин.
| СН2 СН2Cl |

|
 N-CH3 · HCl N-CH3 · HCl
|
| СН2 СН2Cl |
эмбихин
[метил-бис-(b-хлорэтил)-амина гидрохлорид]
В России применялся менее токсичный препарат новэмбихин.
Существующая в настоящее время точка зрения относительно механизма действия алкилирующих средств представлена в таблице 3.
В растворах и биологических жидкостях дихдорэтиламины отщепляют ионы Cl-. Из хлорэтилового остатка образуется электрофильный карбониевый ион, который преобразуется в этиленимоний. Последний образует функционально активный карбониевый ион, алкилирующий (ингибирующий) клеточные структуры (нуклеофильные структуры ДНК, аминогруппы и фосфатные группы РНК, аминокислоты, полипептиды, возможно, ферменты) в опухолевых клетках. Однако, эти соединения атакуют и нормальные быстро пролиферирующие клетки. Но опухолевые клетки более энергично ассимилируют из крови вещества, необходимые для синтеза нуклеиновых кислот. Поэтому для повышения избирательности действия антибластомных средств на опухолевые клетки был осуществлен синтез производных азотистого иприта, содержащих при атоме азота остатки или молекулы природных метаболитов. Примером таких соединений являются допан (к атому азота присоединено пиримидиновое основание 4-метилурацил) и сарколизин (остаток аминокислоты фенилаланина), близкие им – лофенал, пафенцил.
В дальнейшем способность образовывать алкилирующие радикалы была обнаружена и у других соединений (см. классификацию).
Таблица 3.
Дата добавления: 2016-05-05; просмотров: 821;
