Мікрокристалоскопічна реакція на кальцій
Розведена H2SO4 та розчини сульфату утворюють із катіонами Са2+ голчасті кристали гіпсу, CaSO4 ×2 Н2О.
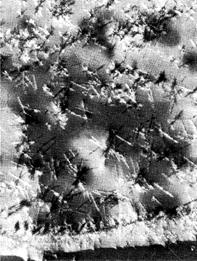
На предметне скло нанесіть краплю розчину Ca(NO3)2, краплю розведеного розчину Н2SO4, трохи упарте, поки з’явиться облямівка по краях краплі. Кристали, що утворились − оберемки невеликих голок − розгляньте під мiкроскопом (фото 1, збільшення у 17 разів, окуляр 7х).
Якщо концентрація с(Н2SО4) ³ 3 моль/л, то суміш не випаровують, а лише підсушують. Утворюються кристали у формі окремих білих голок (фото 2, збільшення у 17 разів, окуляр 7х).
| 
|
| Фото 1. | Фото 2. |
2.3.4. Утворення родизонату кальцію.На фільтрувальний папір нанесіть краплю розчину Ca(NO3)2, краплю попередньо розведеного розчину NaOH (розводячи розчин із c(NaOH) = 6 моль/л, до його краплі додайте 3 краплі дистильованої води) й краплю розчину родизонату.
Якого кольору утворюється осад? Чи можна використовувати цю реакцію, щоб виявити кальцій у присутності барію?
2.3.5. Осадження СаC2O4(s). До 2-3 крапель розчину Са(NO3)2 додайте 1-2 краплі розчину оксалату амонію. Осад розділити на 2 частини. До 1-ї додайте 2 краплі розчину з c(HNO3) = 3 моль/л, до 2-ї − з с(НАс) = 6 моль/л при нагріванні. Що при цьому відбувається? Запишіть рівняння реакцій. Чи можна дією (NH4)2C2O4 виявити Са (ІІ) у присутності Sr (ІІ) та Ва (ІІ)?
2.3.6. Реакція Са (ІІ) із гексаціанофератом (ІІ).У 3 окремих гнізда чорної крапельної пластинки вмістіть: у 1-е краплю розчину Са(NO3)2, у 2-е − розчин Sr(NО3)2, у 3-є − розчин ВаСl2. До кожного гнізда додайте по краплі розчинив з c(NH4Cl) = 4 моль/л та з с(К4Fe(СN)6) = 0,3 моль/л. У якому випадку утворився осад i якого кольору?
Запишіть рівняння реакції утворення Ca(NH4)2Fe(CN)6(s). Чи можна її використовувати, щоб виявити кальцій у присутності стронцію та барію?
2.3.7. Забарвлення полум'я від кальцію.Скляну паличку опустіть у розчин Ca(NO3)2 і внесіть у полум'я газового пальника. Солі кальцію забарвлюють безбарвне полум'я у цегляно-червоний колір.
Таблиця 7
Дата добавления: 2016-08-07; просмотров: 983;
