Применение окислительно-восстановительных реакций в аналитической химии
Окислительно-восстановительные реакции широко используются в качественном и количественном анализе.
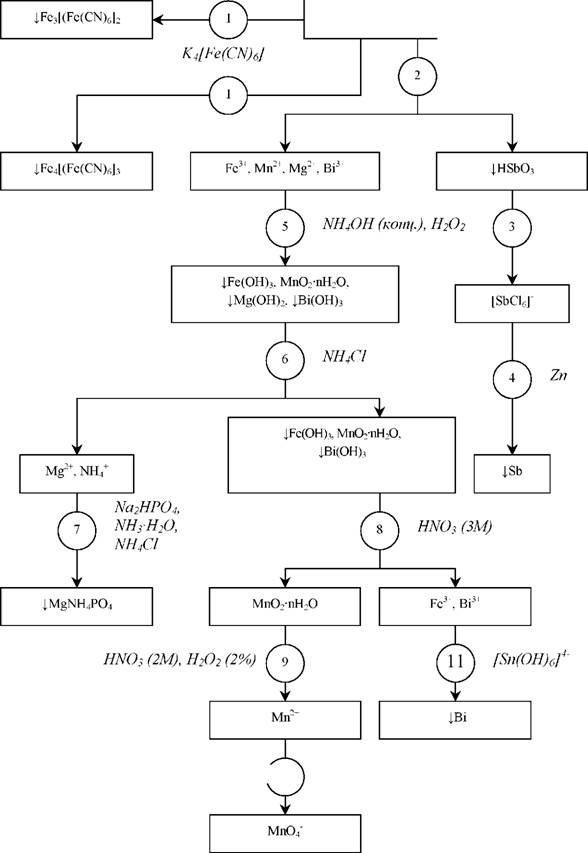
В качественном анализе окислительно-восстановительные реакции используются для:
- переведения соединений из низших степеней окисления в высшие и наоборот;
- переведения малорастворимых соединений в раствор;
- обнаружения ионов;
- удаления ионов.
6.Растворимость. Произведение растворимости. Факторы, влияющие на растворимость труднорастворимых электролитов.
В насыщенном растворе труднорастворимого сильного электролита произведение концентрации его ионов в степенях стехиометрических коэффициентов при данной температуре есть величина постоянная, называемая произведением растворимости (ПР).
Произведение растворимости характеризует растворимость труднорастворимого электролита при данной температуре. Из двух однотипных солей, например, CaSO4 с ПР = 2,5∙10–5 и BaSO4 с ПР = 1,1∙10–10, большей растворимостью обладает та соль, у которой ПР больше.
Концентрация каждого иона в насыщенном растворе электролита может быть изменена, но при этом изменяется и концентрация другого иона так, что произведение концентраций сохраняет прежнюю величину. Поэтому, если в насыщенный раствор электролита ввести некоторое количество одного из ионов, входящих в состав электролита, то концентрация другого иона должна уменьшиться и часть растворенного электролита выпадет в осадок, то есть растворимость электролита понижается от введения в раствор одноименных ионов. Произведение растворимости (ПР, Ksp) — произведение концентраций ионов малорастворимого электролита в его насыщенном растворе при постоянных температуре и давлении. Произведение растворимости — величина постоянная.
7.. Условия образования и растворения осадков. Дробное осаждение и разделение.
ДРОБНОЕ ОСАЖДЕНИЕ— способ разделения смсси веществ, близких по химич. свойствам и растворимости. Д. о. состоит в последовательном переводе компонентов смеси в осадок отдельны.ми порциями (фракция.ми). При добавлении осадителя к смеси двух солей в растворе в первую очередь осаждается компонент, образуюищй наименее растворяемое соединение. Затем, когда большая часть его будет в осадке и отношение концентраций иопов компонентов достиг-иет значеиия, равного отношению произведений растворимости образующихся соединений, в осадок начнет переходить также и второй компонент, причем каждая последую1цая фракция осадка будет богаче вторым и беднее первым компонентом. Возможность полного разделения смеси двух веществ зависит от соотношений первоначальных концентраций их в растворе, а также от значений произведений растворимости соответствующих соединений.
8.. Реакции осаждения и их применения в фармацевтическом анализе. Гетерогенные процессы
ПРОИЗВЕДЕНИЕ РАСТВОРИМОСТИ — константа равновесия гетерогенной реакции растворения (или обратной реакции осаждения) малорастворимой соли в определенном растворителе. Процессы образования и растворения осадков имеют большое практическое значение для различных отраслей науки и промышленности. Константа равновесия реакции растворения, называемая произведением растворимости ПР , является произведением концентраций соответствующих ионов в насыщенном растворе.
Представительность пробы; взаимосвязь с объектом и методом анализа. Факторы, обусловливающие размер и способ отбора представительной пробы. Отбор проб гомогенного и гетерогенного состава. Способы получения средней пробы твердых, жидких и газообразных веществ; устройства и приемы, используемые при этом; первичная обработка и хранение проб; дозирующие устройства.
Основные способы перевода пробы в форму, необходимую для конкретного вида анализа: растворение в различных средах; спекание, сплавление, разложение под действием высоких температур, давления, высокочастотного разряда; комбинирование различных приемов; особенности разложения органических соединений. Способы устранения и учета загрязнений и потерь компонентов при пробоподготовке.
Особенности пробоподготовки твёрдых, жидких и мягких лекарственных форм в фармацевтическом анализе.
9.Методы качественного анализа неорганических и органических веществ
Качественный анализ, совокупность химических, физико-химических и физических методов обнаружения и идентификации элементов, радикалов, ионов и соединений, входящих в состав анализируемоговещества или смеси веществ. Качественный анализ — один из основных разделов аналитической химии. Важнейшие характеристики методов качественного анализа: 1) специфичность (селективность), т. е. возможность обнаружения искомого элемента в присутствии другого; 2) чувствительность, определяемая наименьшим количеством элемента, которое может быть обнаружено данным методом в капле раствора(0,01–0,03 мл); Качественный анализ неорганических соединений в водных растворах основан на ионных реакциях; в соответствии с этим он разделяется на анализ катионов и анализ анионов. Наиболее часто катионы делят на 5 групп по растворимости их сернистых солей. Анионы обычно классифицируют по различнойрастворимости бариевых или серебряных солей. Если в анализируемом веществе определяют ионы, которые могут быть обнаружены селективными реагентами, то анализ ведут дробным методом
Наряду с классическими химическими методами в качественном анализе широко используют физические и физико-химические (так называемые инструментальные) методы, основанные на изучении оптических, электрических, магнитных, тепловых, каталитических, адсорбционных и др. свойств анализируемых веществ. Эти методы обладают рядом преимуществ перед химическими, т.к. позволяют во многих случаях исключить операцию предварительного химического разделения анализируемой пробы на составные части, а также непрерывно и автоматически регистрировать результаты анализа. Кроме того, при использовании физических и физико-химических методов для определения малых количеств примесей требуется значительно меньшее количество анализируемой пробы.
Качественный анализ органических соединений проводят методами элементного анализа и функционального анализа, а также путем определения основных физико-химических свойств анализируемых веществ.
Типы аналитических реакций и реагентов:
Дата добавления: 2016-06-24; просмотров: 7864;
