Нарушения сердечного ритма и проводимости (с указанием формы). 10 страница
Таким образом, тщательный анализ основных характеристик болевого синдрома и других анамнестических данных в большинстве случаев позволяет выделить среди больных ИБС пациентов с нестабильным течением заболевания.
 Запомните
Основными клиническими критериями НС являются: 1. Быстро меняющийся характер, интенсивность и частота приступов стенокардии напряжения, длительно существующей у больного (при прогрессирующей стенокардии), или недавно выявленной (при ВВС прогрессирующего течения). 2. Появление стенокардии покоя (если ранее ее не было), особенно тяжелых, спонтанно возникающих ангинозных приступов, продолжающихся более 15–20 мин. 3. Быстрое снижение толерантности к физической нагрузке и изменение функционального класса стенокардии. 4. Снижение эффективности обычной для данного больного антиангинальной терапии. 5. Появление частых ночных ангинозных приступов (в том числе вазоспастической стенокардии Принцметала). 6. Появление ранней постинфарктной стенокардии (2–14 суток от начала ИМ). Запомните
Основными клиническими критериями НС являются: 1. Быстро меняющийся характер, интенсивность и частота приступов стенокардии напряжения, длительно существующей у больного (при прогрессирующей стенокардии), или недавно выявленной (при ВВС прогрессирующего течения). 2. Появление стенокардии покоя (если ранее ее не было), особенно тяжелых, спонтанно возникающих ангинозных приступов, продолжающихся более 15–20 мин. 3. Быстрое снижение толерантности к физической нагрузке и изменение функционального класса стенокардии. 4. Снижение эффективности обычной для данного больного антиангинальной терапии. 5. Появление частых ночных ангинозных приступов (в том числе вазоспастической стенокардии Принцметала). 6. Появление ранней постинфарктной стенокардии (2–14 суток от начала ИМ).
| ||
| 6.3.2. Классификация нестабильной стенокардии | ||

| ||
С целью оценки прогностической значимости симптомов НС и выделения группы лиц с особенно неблагоприятным течением заболевания E. Braunwald в 1989 г. была предложена классификация НС, модифицированная в 2000 г. (C.W. Hamm, E. Braunwald), в которой НС делится на классы и формы в зависимости от тяжести клинической картины заболевания и условий возникновения острого коронарного синдрома (табл. 6.2).
Таблица 6.2.
Классификация нестабильной стенокардии (C.W. Hamm, E. Braunwald, 2000)
| Классы НС | Формы НС | ||
| А — развивается в присутствии экстракардиальных факторов, которые усиливают ишемию миокарда Вторичная НС | В — развивается без экстракардиальных факторов Первичная НС | С — возникает в пределах 2-х недель после ИМ Постинфарктная стенокардия | |
| I — Первое появление тяжелой стенокардии или прогрессирующая стенокардия напряжения (без стенокардии покоя) | IА | IВ | IС |
| II — Стенокардия покоя в предшествующий месяц, но не в ближайшие 48 ч (стенокардия покоя, подострая) | IIА | IIВ | IIС |
| III — Стенокардия покоя в предшествующие 48 ч (стенокардия покоя, острая) | IIIА | IIIВ IIIВ — тропонин – IIIВ — тропонин + | IIIС |
В основу этой классификации положены характер и сроки появления болевого синдрома. Наиболее серьезным в прогностическом отношении является III класс НС, при котором стенокардия покоя наблюдалась в течение последних 2-х суток перед обращением к врачу. Именно у этой категории больных НС риск развития ИМ или внезапной сердечной смерти является наиболее высоким.
Важным представляется также выделение различных форм заболевания в зависимости от условий возникновения острого коронарного синдрома. Наиболее серьезный прогноз следует ожидать у больных с так называемой первичной НС III класса, особенно у пациентов с положительными маркерами некроза миокарда (тропонин-положительные).
Приведенная классификация E. Braunwald в настоящее время широко используется в научных исследованиях, однако в клинической практике более удобной представляется оценка кратковременного риска тех или иных осложнений НС на основании следующих клинических критериев, представленных в табл. 6.3.
Таблица 6.3.
Клинические критерии кратковременного риска у больных нестабильной стенокардией (по E. Braunwald, в модификации)
| Группа высокого риска* | Группа промежуточного риска** | Группа низкого риска*** |
| Стенокардия покоя более 20 мин | Стенокардия покоя в момент осмотра купирована, но сохраняется возможность ее возобновления | Увеличение частоты и продолжительности стенокардии |
| Отек легких | Стенокардия, сопровождающаяся динамическими изменениями зубца Т | Снижение порога возникновения стенокардии |
| Появление или усиление шума митральной регургитации | Ночная стенокардия | Появление стенокардии в течение последних 2-х недель — 2-х месяцев |
| Стенокардия покоя с транзиторными смещениями сегмента RS–T не менее 1 мм | Появление в течение 2-х последних недель стенокардии напряжения III или IV ФК | Отсутствие изменений на ЭКГ |
| Стенокардия, сопровождающаяся появлением патологического III тона сердца | Наличие патологических зубцов Q или депрессии сегмента RS–T более 1 мм в нескольких отведениях | |
| Появление влажных хрипов в легких | Возраст более 65 лет | |
| Стенокардия, сопровождающаяся артериальной гипотензией | ||
| Повышенный уровень тропонинов в крови (или других маркеров некроза миокарда) |
Примечание:
* — высокий риск диагностируется при наличии хотя бы одного из нижеперечисленных критериев; ** — принадлежность к группе промежуточного риска диагностируется при отсутствии критериев высокого риска и наличии хотя бы одного из нижеперечисленных критериев;
*** — принадлежность к группе низкого риска диагностируется при отсутствии критериев высокого и промежуточного риска и наличии хотя бы одного из нижеперечисленных критериев.
Оценка кратковременного риска НС крайне необходима для выбора оптимального метода лечения больных.
| 6.3.3. Диагностика |

|
Все больные с НС должны быть госпитализированы в блоки интенсивной терапии кардиологических отделений стационаров. При этом следует помнить, что чем меньше времени прошло от начала дестабилизации состояния больного, тем выше риск развития ИМ или внезапной сердечной смерти и тем больше показана срочная госпитализация. Особенно быстро этот вопрос должен решаться при таких вариантах НС, как ВВС прогрессирующего течения, спонтанная (вариантная) стенокардия Принцметала и тяжелые и длительные приступы стенокардии покоя.
Следует также подчеркнуть, что правилом для врача должна явиться обязательная госпитализация в специализированный стационар всех больных ВВС, если симптомы болезни возникли менее 1 месяца назад. Это связано, во-первых, со сложностью прогнозирования дальнейшего развития симптомов болезни даже у больных с относительно стабильным течением ВВС и, во-вторых, с необходимостью более детального обследования этих пациентов с целью уточнения диагноза, морфологической основы и патогенетических механизмов коронарной недостаточности и проведения дифференциальной диагностики с некоронарогенными кардиалгиями.
Диагностический поиск в блоке кардиореанимации и затем в кардиологическом отделении преследует обычно следующие цели.
1.Подтверждение диагноза НС и ее клинического варианта и проведение дифференциального диагноза с острым ИМ.
2. Уточнение преобладающих патогенетических механизмов, лежащих в основе обострения коронарной недостаточности у данного больного.
3.Оценка характера и степени повреждения миокарда ЛЖ.
4. Выделение среди больных НС лиц с высоким риском развития острого ИМ и/или внезапной сердечной смерти.
Для решения этих задач необходимо оценить:
- динамику болевого синдрома на фоне проведения интенсивной антиангинальной терапии;
- динамику ЭКГ, особенно во время спонтанных приступов стенокардии;
- результаты суточного мониторирования ЭКГ по Холтеру;
- динамику уровня кардиоспецифических ферментов (КФК, МВ КФК, АсАт, ЛДГ, ЛДГ1), а также концентрации миоглобина и тропонинов I и Т;
- данные ЭхоКГ;
- состояние системы гемостаза;
- результаты, полученные при коронароангиографии.
Электрокардиография
Исследование ЭКГ12в межприступном периоде у многих больных с синдромом НС имеет ограниченное значение, особенно у больных с ВВС и спонтанной стенокардией Принцметала. Лишь при глубокой и распространенной ишемии с очагами повреждения миокарда и иногда микронекрозами кардиомиоцитов на ЭКГ в течение 1–4 дней могут регистрироваться преходящие изменения конечной части желудочкового комплекса.
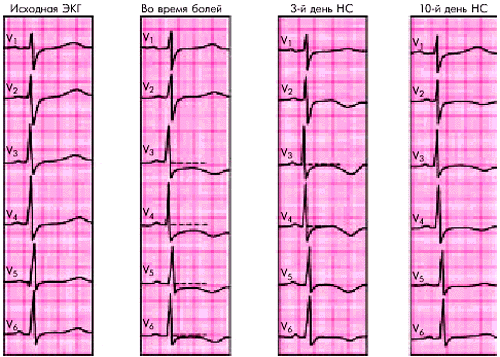
Чаще наблюдается депрессия сегмента RS–T (более 1 мм) горизонтального или косонисходящего типа, которая в большинстве случаев сочетается с соответствующими измененями зубцов Т (рис. 6.10) — их сглаженностью или формированием отрицательных равносторонних и остроконечных (“коронарных”) зубцов Т (больше 1 мм). В других случаях отрицательная динамика Т является единственным, хотя и неспецифическим, электрокардиографическим подтверждением развившейся ишемии миокарда.
Сохранение этих изменений в течение нескольких дней после начала дестабилизации ИБС указывает на более глубокое, чем при стабильной стенокардии, ишемическое повреждение миокарда ЛЖ.
Следует подчеркнуть, что такая же отрицательная динамика ЭКГ может выявляться и в случаях прогрессирования безболевой ишемии миокарда, т.е. у пациентов, у которых отсутствует болевой синдром. Следовательно, любая более или менее стойкая отрицательная динамика ЭКГ у больного ИБС, даже если она не сопровождается болевыми ангинозными приступами, требует углубленного обследования на предмет наличия или отсутствия других признаков дестабилизации заболевания.
|
| Рис. 6.10. Динамика ЭКГ (грудные отведения) у больного с нестабильной стенокардией |
 Запомните
1. Для большинства больных НС характерна отрицательная динамика ЭКГ в виде депрессии сегмента RS–T (больше 1 мм) и изменений зубца Т, сохраняющихся в течение нескольких дней от начала дестабилизации ИБС. 2. Описанные динамические изменения ЭКГ не являются строго специфичными для НС и могут выявляться на фоне приема некоторых лекарственных средств (например, дигоксина) или нарушений электролитного обмена. 3. Отсутствие отрицательной динамики ЭКГ не исключает диагноз нестабильной стенокардии. Запомните
1. Для большинства больных НС характерна отрицательная динамика ЭКГ в виде депрессии сегмента RS–T (больше 1 мм) и изменений зубца Т, сохраняющихся в течение нескольких дней от начала дестабилизации ИБС. 2. Описанные динамические изменения ЭКГ не являются строго специфичными для НС и могут выявляться на фоне приема некоторых лекарственных средств (например, дигоксина) или нарушений электролитного обмена. 3. Отсутствие отрицательной динамики ЭКГ не исключает диагноз нестабильной стенокардии.
|
Подъем сегмента RS–T указывает на трансмуральную ишемию миокарда, развившуюся вследствие окклюзии КА. Стойкий подъем сегмента RS–T характерен для развивающегося ИМ (ИМ “в ходу”). Преходящий подъем сегмента RS–T может быть выявлен во время приступа вазоспастической стенокардии Принцметала.
Длительное мониторирование ЭКГ по Холтеру является наиболее информативным методом изучения электрической активности сердечной мышцы у больных НС. Холтеровское мониторирование ЭКГ позволяет выявить:
- ишемические изменения ЭКГ во время спонтанных приступов стенокардии;
- частоту и продолжительность эпизодов болевой и безболевой ишемии;
- преходящие нарушения ритма и проводимости.
У большинства больных с синдромом НС при суточном мониторировании выявляются транзиторные ишемические изменения сегмента RS–T, в том числе эпизоды безболевой ишемии. Чаще наблюдается смещение сегмента RS–Т ниже изоэлектрической линии (на 1,0 мм и более), что свидетельствует о возникновении субэндокардиальной ишемии миокарда. У больных с нестабильным течением спонтанной (вариантной) формы стенокардии во время ангинозного приступа, сопровождающегося, как известно, динамической окклюзией КА (выраженным спазмом), можно обнаружить подъем сегмента RS–Т выше изолинии, указывающий на наличие преходящей трансмуральной ишемии миокарда.
Характерно, что в группе больных с НС существенно чаще, чем у больных со стабильным течением заболевания, обнаруживаются суточные колебания сегмента RS–T и преходящие желудочковые аритмии высоких градаций. Особенно неблагоприятным признаком является безболевая ишемия миокарда, не сопровождающаяся возникновением приступа стенокардии. Наличие безболевой ишемии миокарда существенно повышает риск внезапной сердечной смерти и острого ИМ. Прогноз остается неблагоприятным даже в тех случаях, когда под влиянием антиангинальной терапии уменьшается количество спонтанных болевых приступов стенокардии, но число эпизодов безболевой ишемии сохраняется прежним.
 Запомните
1. Чем больше частота возникновения у больных НС транзиторных ишемических изменений сегмента RS–T и их продолжительность, тем выше риск развития ИМ и внезапной сердечной смерти. 2. Особенно неблагоприятным признаком у больных НС является наличие безболевой ишемии миокарда, не сопровождающейся приступами стенокардии. Запомните
1. Чем больше частота возникновения у больных НС транзиторных ишемических изменений сегмента RS–T и их продолжительность, тем выше риск развития ИМ и внезапной сердечной смерти. 2. Особенно неблагоприятным признаком у больных НС является наличие безболевой ишемии миокарда, не сопровождающейся приступами стенокардии.
|
Функциональные нагрузочные тесты. У больных НС с низким риском ИМ и внезапной смерти непосредственно перед выпиской из стационара и не раньше чем через 7–10 дней после приступа ангинозной боли, проводят стресс-тесты (с физической нагрузкой или фармакологические) с целью объективной оценки степени риска заболевания. Главным условием их проведения является отсутствие повторных эпизодов болевой или безболевой (по данным ЭКГ или холтеровского мониторирования) ишемии миокарда в покое. Низкая толерантность к нагрузке и выраженные ишемические изменения ЭКГ во время проведения теста служат показанием для осуществления коронароангиографии и решения вопроса о целесообразности реваскуляризации (см. ниже).
Лабораторные тесты
Биохимический анализ кровиу больных НС дает возможность:
- оценить активность кардиоспецифических ферментов и других маркеров некроза с целью дифференциальной диагностики НС и острого ИМ;
- оценить выраженность и характер нарушений липидного, углеводного и других видов обмена.
Активность кардиоспецифических ферментов (КФК, МВ КФК, АсАТ, ЛДГ, ЛДГ1) при НС в большинстве случаев не отличается от нормы. Лишь изредка при тяжелом течении заболевания на фоне длительной и необратимой ишемии миокарда может произойти некротизация отдельных кардиомиоцитов. В этих случаях наблюдается небольшое повышение активности указанных ферментов, но не более чем на 40% от верхней границы нормы.
В то же время следует иметь в виду, что такое же повышение активности КФК, ЛДГ, МВ КФК и других ферментов может быть и при отсутствии некротизации сердечной мышцы (при различных заболеваниях внутренних органов, повреждении скелетных мышц, после кардиоверсии и т.д.). В этих случаях диагноз уточняется при проведении сцинтиграфии с 99mТс (технецием пирофосфатом) и при тщательном анализе всей клинической картины заболевания.
Определение современных маркеров некроза (тропонины I и Т) имеет важное значение для выделения группы больных НС с высоким риском ИМ и внезапной смерти. В настоящее время уровень тропонинов в сыворотке крови считается наиболее специфическим и чувствительным лабораторным тестом для диагностики некроза кардиомиоцитов и дифференциальной диагностики НС и острого ИМ. На рис. 6.11 видно, что у больных с НС и высоким риском развития ИМ или внезапной смерти нередко наблюдается небольшое повышение уровня тропонинов, что свидетельствует о наличии у этих пациентов микронекрозов в сердечной мышце и плохом прогнозе заболевания. Повышение уровня тропонинов при классическом ИМ существенно отличается от результатов, полученных у больных НС: амплитуда и продолжительность повышения тропонинов оказываются значительно более выраженными.
| Рис. 6.11. Изменение уровня тропонинов при нестабильной стенокардии (кривая красного цвета) и инфаркте миокарда. Для сравнения приведена кривая повышения уровня МВ КФК у больного острым инфарктом миокарда | 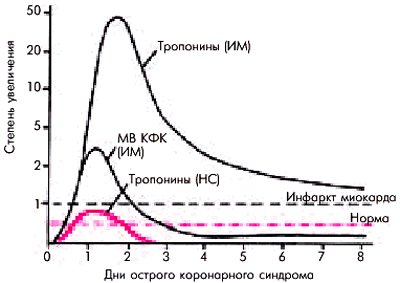
|
Нарушения углеводного и инсулинового обмена могут значительно ухудшать ближайший и отдаленный прогноз НС, так как существенно повышают риск возникновения ИМ и внезапной сердечной смерти. Так же, как при стабильной стенокардии напряжения, гиперлипидемия выявляется у значительной части больных НС. Имеется определенная зависимость между уровнем общего ХС, ХС ЛНП и количеством пораженных КА, толерантностью к физической нагрузке и глобальной систолической функцией ЛЖ (Е.П. Кохан с соавт., 2000).
Нарушения в системе гемостаза, закономерно выявляющиеся у больных НС, играют важную роль как в дестабилизации ИБС (в формировании “осложненной” атеросклеротической бляшки), так и в определении исходов НС. Поэтому у каждого больного с НС целесообразно по возможности более тщательно изучить состояние всех трех звеньев этой системы: 1) сосудисто-тромбоцитарного гемостаза; 2) системы коагуляционного гемостаза; 3) системы фибринолиза. С этой целью необходимо определение следующих показателей:
- активированное время рекальцификации (АВР);
- активированное частичное тромбопластиновое время (АЧТВ);
- фибриноген плазмы;
- фибринолитическая активность крови;
- свободный гепарин крови;
- адгезивность и агрегация тромбоцитов, агрегация эритроцитов;
- протромбиновый индекс;
- антитромбин III;
- аутокоагуляционный тест;
- время свертывания цельной крови;
- тромбиновое время;
- показатели вязкости крови;
- тромбоэластограммы.
Базисные методы определения состояния системы свертывания крови позволяют оценить следующие признаки гиперкоагуляции у больных НС.
1. Укорочение времени свертывания цельной крови (меньше 5 мин).
2. Укорочение времени рекальцификации плазмы (менее 60–120 с при использовании кальция хлорида и менее 50–70 с — при использовании каолина).
3. Уменьшение активированного частичного тромбопластинового времени (АЧТВ) — кефалин-каолиновое время меньше 35–50 с.
4. Увеличение протромбинового индекса более 100% (или уменьшение протромбинового времени).
5. Изменение основных показателей тромбоэластограммы: укорочение времени реакции (R) и времени коагуляции (К) и увеличение максимальной амплитуды (Мa) тромбоэластограммы (рис. 6.12).
6. Дефицит антитромбина III — важнейшего физиологического антикоагулянта.
7. Повышение адгезии и агрегации тромбоцитов.
8. Увеличение концентрации фибриногена (более 2–4 г/л).
9. Появление в плазме растворенных фибрин-мономерных комплексов с фибриногеном (РФМК).
10. Повышение продуктов деградации фибрина (ПДФ) — более 0,015 г/л.
Увеличение последних двух показателей — признак усиливающегося свертывания крови, сопровождающегося активацией фибринолитической системы (см. ниже).
В реальной клинической практике бывает достаточно определения времени АЧТВ, которое служит в качестве контрольного теста при лечении больных антитромбиновыми препаратами.
| Рис. 6.12. Тромбоэластограмма в норме (а); при гиперкоагуляции (б) и гипокоагуляции (в). Схема | 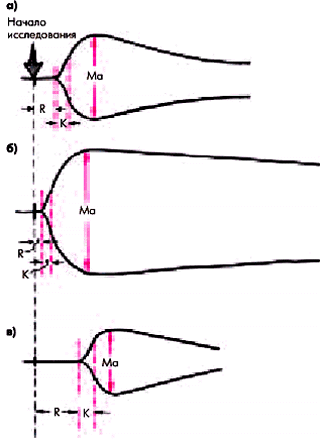
|
Эхокардиография
Эхокардиографическое исследование у больных НС дает возможность количественно оценить степень систолической и диастолической дисфункции ЛЖ, а также выявить признаки нарушения локальной сократимости, обусловленные как острым ишемическим повреждением кардиомиоцитов, так и наличием у некоторых больных НС постинфарктного кардиосклероза.
Нарушения глобальной систолической функции ЛЖ оцениваются по величине ФВ, степени укорочения переднезаднего размера ЛЖ в систолу (%DS) и другим показателям (КДО, КСО, МО, СИ, размеры ЛП). Прогностическое значение имеет снижение ФВ меньше 40%, которое выявляется более чем у половины больных НС, чаще у пациентов с длительным анамнезом ИБС и больных, перенесших в прошлом ИМ. В то же время даже у относительно молодых пациентов с ВВС примерно в 1/4–1/3 случаев также можно обнаружить снижение систолической функции ЛЖ, обусловленное ишемическим повреждением миокарда. Под влиянием лечения, направленного на восстановление перфузии миокарда, происходит уменьшение признаков систолической дисфункции ЛЖ, что подтверждает ишемический генез снижения сократимости ЛЖ.
Выявление у больных НС локальных нарушений сократимости ЛЖ с помощью двухмерной ЭхоКГ имеет особое диагностическое и прогностическое значение. Как известно, асинергия ЛЖ у больных ИБС может быть обусловлена 4 основными причинами: 1) острым ИМ; 2) постинфарктным кардиосклерозом; 3) кратковременной преходящей болевой или безболевой ишемией миокарда и 4) постоянно действующей ишемией жизнеспособного миокарда (гибернирующий миокард), а также существованием так называемого “оглушенного” миокарда.
При остром трансмуральном ИМ с зубцом Q или постинфарктном кардиосклерозе эхокардиографические признаки локальных нарушений сократимости ЛЖ (чаще акинезия или дискинезия) сохраняются длительное время, как правило, в течение всей жизни больного и соответствуют электрокардиографическим маркерам острого или перенесенного ИМ (патологический зубец Q или комплекс QS).
Участки гипокинезии ЛЖ, обнаруживаемые у больных с кратковременной преходящей ишемией миокарда, вызванной очередным приступом стабильной стенокардии или индуцированной функциональным нагрузочным тестом (велоэргометрия, тредмил-тест, фармакологические пробы), как правило, через несколько минут после прекращения нагрузки или купирования приступа стенокардии не выявляются. На этом основана диагностика ИБС с помощью метода стресс-эхокардиографии.
Более чем у половины больных с НС гипокинезия ЛЖ может сохраняться от одного до нескольких дней после купирования болевого приступа, свидетельствуя о более серьезных нарушениях коронарного кровообращения и более глубоком ишемическом повреждении миокарда. Это является важным диагностическим признаком НС, отличающим эту форму ИБС от приступов стабильной стенокардии.
Причиной таких локальных нарушений сократимости ЛЖ, сохраняющихся у больных НС в течение нескольких дней от начала дестабилизации болезни, могут являться дистрофические изменения и даже некрозы кардиомиоцитов в ограниченных участках сердечной мышцы, расположенных в бассейне нарушенного коронарного кровообращения.
Кроме того, следует иметь в виду еще два возможных механизма снижения локальной сократимости ЛЖ, которые особенно часто наблюдаются у больных НС.
1. Феномен гибернирующего (“спящего”) миокарда, находящегося в условиях хронического снижения коронарной перфузии.
2. Феномен “оглушения”, выявляющийся после восстановления исходной перфузии тканей (реперфузии).
Оба феномена были описаны в главе 5. Напомним, что феномен гибернации миокарда (hybernatio, “спячка”) заключается в нарушении локальной сократимости ЛЖ, возникающем при выраженном и продолжительном снижении его перфузии и не сопровождающемся иными признаками ишемии. Феномен гибернации является своеобразной формой клеточного анабиоза, обеспечивающего выживаемость кардиомиоцитов в условиях дефицита кислорода. Важно помнить, что гибернирующий миокард реагирует на введение катехоламинов: например, под влиянием малых доз добутамина временно восстанавливается сократимость миокарда, что доказывает его жизнеспособность. Феномен “оглушенного” миокарда (stunning) — это преходящее постишемическое нарушение локальной сократимости ЛЖ, возникающее после восстановления исходного коронарного кровообращения (реперфузии) и прекращения действия ишемии. Оба феномена очень характерны для больных с “обострением” ИБС, в том числе для пациентов с НС, хотя встречаются и при стабильном течении заболевания.
 Запомните
1. Примерно у половины больных НС обнаруживаются эхокардиографические признаки снижения глобальной систолической функции ЛЖ, в частности, уменьшение ФВ ниже 40%. 2. Нарушения локальной сократимости ЛЖ у больных НС, как правило, сохраняются в течение нескольких дней после ангинозных приступов, свидетельствуя о наличии более значительных нарушений коронарного кровотока и метаболизма кардиомиоцитов. 3. Основной причиной относительно продолжительного снижения локальной сократимости ЛЖ у больных НС являются: Запомните
1. Примерно у половины больных НС обнаруживаются эхокардиографические признаки снижения глобальной систолической функции ЛЖ, в частности, уменьшение ФВ ниже 40%. 2. Нарушения локальной сократимости ЛЖ у больных НС, как правило, сохраняются в течение нескольких дней после ангинозных приступов, свидетельствуя о наличии более значительных нарушений коронарного кровотока и метаболизма кардиомиоцитов. 3. Основной причиной относительно продолжительного снижения локальной сократимости ЛЖ у больных НС являются:
|
Добавим, что нарушения локальной сократимости в области заднедиафрагмальной стенки ЛЖ свидетельствуют, как правило, о стенозировании (органическом или динамическом) правой коронарной артерии, а соответствующие нарушения переднеперегородочной и верхушечной локализации — об ограничении коронарного кровотока в бассейне ЛКА.
Если у больных НС, несмотря на интенсивную антиангинальную и антитромбоцитарную терапию, нарастают симптомы коронарной недостаточности и сохраняется высокий риск возникновения ИМ и ВCС, должен быть решен вопрос о целесообразности хирургической реваскуляризации зон ишемии. В этих случаях больной должен быть переведен в специализированные кардиохирургические центры, где проводится КАГ и уточняется характер поражения КА, локализация и распространенность патологического процесса, а также состояние коллатерального кровообращения, после чего решается вопрос о выборе способа реваскуляризации.
Сцинтиграфия миокарда
Сцинтиграфия миокарда с 201Т1, зарегистрированная в покое (без нагрузки), позволяет выявить у части больных НС дефекты накопления радиопрепарата в зонах нарушенной перфузии миокарда и оценить их локализацию и распространенность. Чем меньше времени прошло с момента ангинозного приступа, тем больше шансов обнаружить эти дефекты. Если перфузия миокарда полностью восстановлена, “холодные” зоны локального снижения радиоактивности на сцинтиграммах больше не выявляются. В отличие от этого при остром ИМ или постинфарктном кардиосклерозе “холодные” зоны резкого снижения или отсутствия радиоактивности обнаруживаются в течение длительного времени.
Таким образом, у части больных НС сцинтиграфия миокарда с 201Т1 позволяет визуализировать зоны локального снижения перфузии миокарда, определить их распространенность и локализацию.
Коронароангиография (КАГ)
Проведение КАГ у больных НС позволяет уточнить локализацию, распространенность и характер поражения коронарного русла, а также оценить выраженность коллатерального кровообращения. Эти данные необходимы, прежде всего, для решения вопроса о целесообразности проведения чрескожной коронарной ангиопластики и особенно показаны у больных НС с высоким риском возникновения острого ИМ и внезапной сердечной смерти:
- больным с повторными эпизодами ишемии миокарда (рецидивы боли или отрицательная динамика сегмента RS–T);
- больным с повышенным содержанием в сыворотке крови тропонинов или МВ КФК;
- пациентам с нестабильной гемодинамикой (артериальная гипотензия или прогрессирующая сердечная недостаточность);
- больным с угрожающими нарушениями ритма (повторные эпизоды ЖТ или ФЖ);
- пациентам с ранней постинфарктной стенокардией.
Сужение КА обнаруживают примерно у 85–90% больных НС, из них примерно в 40% случаев на КАГ, зарегистрированных в первые сутки заболевания, можно обнаружить тромбы в КА. Только у 10–15% больных по данным КАГ сужение крупных венечных сосудов является гемодинамически незначимым или артерии остаются интактными, несмотря на наличие у этих пациентов типичных клинических, электрокардиографических и сцинтиграфических признаков локального нарушения перфузии миокарда, характерного для ИБС. В этих последних случаях речь идет, как правило, о динамическом стенозе или о метаболическом синдроме (“синдроме Х”), в основе которого лежат серьезные нарушения микроциркуляторного сосудистого русла, обусловленные повреждением эндотелия мелких венечных сосудов и их склонностью к спазму и образованию микротромбов.
Почти у 2/3 больных НС выявляется гемодинамически значимый стеноз КА (сужение более 75% просвета КА), а еще у 1/4 — полная окклюзия одной из 3-х КА, в том числе у больных, перенесших в прошлом ИМ.
Дата добавления: 2016-04-22; просмотров: 652;
