Нарушения сердечного ритма и проводимости (с указанием формы). 12 страница
В то же время применение этих препаратов сопровождается в 1,5–2 раза большей частотой развития малых и больших кровотечений. Этот факт, наряду с остающимися нерешенными проблемами дозировки прямых антитромбинов и продолжительности их применения при острых коронарных синдромах, а также высокая стоимость этих ЛС пока не позволяют рекомендовать их для широкого применения в клинике при лечении больных НС. По-видимому, прямые ингибиторы тромбина целесообразно применять для лечения больных с тромбоцитопенией, вызванной гепарином (рекомендации комитета экспертов ВНОК РФ, 2001).
Коронарная реваскуляризация
При отсутствии эффекта от медикаментозной терапии и сохранении признаков рецидивирующей ишемии миокарда показано проведение коронарной реваскуляризации: чрескожной транслюминальной коронарной ангиопластики (ЧТКА) или аорто-коронарного шунтирования (АКШ). Основными показаниями к проведению экстренной коронарной реваскуляризации являются признаки, характеризующие высокий риск развития ИМ и летального исхода:
1. Повторные эпизоды ишемии миокарда (рецидивы боли или/и отрицательная динамика сегмента RS–T).
2.Повышение содержания в сыворотке крови тропонинов или МВ КФК.
3. Нестабильность гемодинамики (артериальная гипотензия или прогрессирующая сердечная недостаточность).
4. Угрожающие нарушения ритма (повторные эпизоды ЖТ или ФЖ).
5. Ранняя постинфарктная стенокардия.
Чрескожная транслюминальная коронарная ангиопластика. Выбор конкретного метода коронарной реваскуляризации определяется характером, степенью и распространенностью поражения КА, которые выявляются при проведении КАГ (см. выше). При поражении одной КА в большинстве случаев проводят ЧТКА, в том числе с установлением стента, что способствует механической стабилизации поврежденной атеросклеротической бляшки и меньшей частоте рестенозов после баллонной дилатации сосуда.
Результаты баллонной ангиопластики, проведенной у больных НС по экстренным показаниям, несколько хуже, чем на фоне стабильного течения ИБС (см. главу 5). Это связано с тем, что механическое растяжение (сдавление) поврежденной атеросклеротической бляшки увеличивает разрывы фиброзной оболочки и, соответственно, ее тромбогенность. Частота развития ИМ во время инвазивной процедуры экстренной баллонной ангиопластики составляет около 5%, т.е. несколько меньше, чем при применении консервативной терапии (около 10%). Смертность, связанная с самим инвазивным вмешательством, сравнительно низка.
С целью предупреждения рестенозов после ЧТКА целесообразно еще до начала процедуры баллонной ангиопластики начать применение блокаторов гликопротеиновых IIb/IIIа рецепторов тромбоцитов или тиклопидина. Лечение этими ЛС продолжают в течение еще 12–24 ч после инвазивного вмешательства. В последующем рекомендуется прием в течение месяца аспирина в сочетании с клопидогрелем или тиклопидином.
Аорто-коронарное шунтирование проводят чаще при трехсосудистом поражении КА, при стенозе ствола ЛКА, а также при однососудистом сужении, если при КАГ выявляется выраженная извитость или изогнутость венечных сосудов, что не позволяет безопасно провести коронарную ангиопластику.
Летальность во время экстренной операции АКШ у больных НС в последние годы снизилась и составляет около 4–8%, а риск развития ИМ — около 10%. У больных с более тяжелым течением заболевания или ранней постинфарктной стенокардией риск возникновения ИМ более высокий. Существенной проблемой коронарной реваскуляризации остается высокая частота рестенозов КА: при проведении ангиопластики она достигает 40%, а при АКШ — 5–10%.
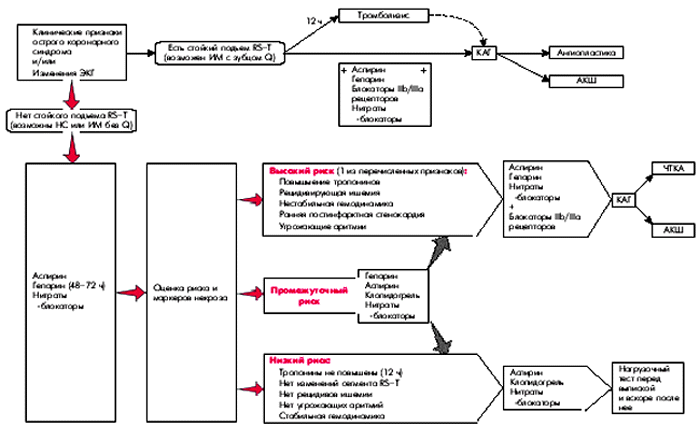
На рис. 6.17 представлена наиболее общая схема ведения больных с острым коронарным синдромом, в том числе пациентов с НС.
|
| Рис. 6.17. Тактика лечения больных с острым коронарным синдромом (Рекомендации комитета экспертов ВНОК, 2001 в модификации) |
Ведение больных после выписки из стационара
После выписки из стационара всем больным, перенесшим эпизоды НС, показано активное воздействие на ФР атеросклероза: курение, ожирение, АГ, гиперлипидемии и т.д. (см. главы 4 и 5). Особое значение придается в настоящее время применению гиполипидемической терапии ингибиторами ГМГ-КоА редуктазы (статинами), которые существенно снижают смертность и частоту осложнений у больных с высоким и средним уровнями ХС ЛНП. Согласно рекомендациям комитета экспертов ВНОК (2001 г.), такую терапию следует начинать еще в стационаре, ориентируясь на уровни липидов в пробах крови, взятых при поступлении.
В обязательном порядке (при отсутствии противопоказаний) должно быть предусмотрено применение:
- β-адреноблокаторов;
- антитромбоцитарных препаратов;
- гиполипидемических средств;
- нитратов.
У больных с клиническими или эхокардиографическими признаками дисфункции ЛЖ показано также длительное применение ингибиторов АПФ.
| 6.3.5. Прогноз |

|
Ближайший прогноз НС оценивается большинством авторов как неблагоприятный: у 10–20% больных НС в течение трех месяцев развивается острый ИМ или новые эпизоды НС, причем летальные исходы составляют 4–10%.
Основными признаками прогностически неблагоприятного варианта течения НС являются:
- сохранение или прогрессирование болевого синдрома и неэффективность антиангинальной терапии;
- приступы стенокардии покоя длительностью более 20 мин;
- косвенные признаки, указывающие на сохранение наклонности к спазму КА (ночные приступы стенокардии Принцметала, положительная проба с эргометрином и др.);
- частые и длительные эпизоды смещения сегмента RS–T при суточном мониторировании ЭКГ, в том числе сохранение эпизодов безболевой ишемии;
- выявление при холтеровском мониторировании ЭКГ преходящих желудочковых аритмий высоких градаций;
- выраженное снижение толерантности больных НС к нагрузкам;
- анамнестические указания на перенесенный в прошлом ИМ или операцию реваскуляризации.
| 6.4. Инфаркт миокарда |

|
Инфаркт миокарда (ИМ) — это ишемический некроз сердечной мышцы, развивающийся в результате острой недостаточности коронарного кровообращения.
ИМ является одной из самых распространенных причин смертности и инвалидизации населения, как в нашей стране, так и за рубежом. В Российской федерации ежегодно ИМ развивается у 0,2–0,6% мужчин в возрасте от 40 до 59 лет (Н.А. Мазур). У мужчин старшей возрастной группы (60–64 г) заболеваемость ИМ еще выше и достигает 1,7% в год. Женщины заболевают ИМ в 2,5–5 раз реже мужчин, особенно в молодом и среднем возрасте, что связывают обычно с более поздним (примерно на 10 лет) развитием у них атеросклероза. После наступления менопаузы (в возрасте старше 55–60 лет) разница в заболеваемости мужчин и женщин существенно уменьшается.
В последние годы отмечается рост заболеваемости ИМ, особенно среди лиц молодого и среднего возраста. Несмотря на повсеместное снижение госпитальной летальности от ИМ, общая смертность от этого заболевания до сих пор остается высокой, достигая 30–50% от общего числа заболевших. Причем большая часть летальных исходов наступает на догоспитальном этапе.
| 6.4.1. Классификация |

|
Современная классификация ИМ предусматривает его деление:
- по величине и глубине поражения сердечной мышцы;
- по характеру течения заболевания;
- по локализации ИМ;
- по стадии заболевания;
- по наличию осложнений ИМ.
1. По величине и глубине поражения сердечной мышцы различают трансмуральный и нетрансмуральный ИМ.
При трансмуральном ИМ (инфаркте миокарда с зубцом Q) очаг некроза захватывает либо всю толщу сердечной мышцы от субэндокардиальных до субэпикардиальных слоев миокарда (рис. 6.18, а), либо большую его часть (рис. 6.18, б), что находит свое отражение на поверхностной ЭКГ в виде формирования патологического зубца Q или комплекса QS в нескольких электрокардиографических отведениях. Отсюда и синоним трансмурального ИМ — “инфаркт миокарда с зубцом Q”. Как правило, такое повреждение сердечной мышцы достаточно обширно и очаг некроза распространяется на 2 и больше сегментов ЛЖ (крупноочаговый ИМ).
| Рис. 6.18. Трансмуральные (с зубцом Q) и нетрансмуральные (без зубца Q) инфаркты миокарда (схема). а, б — трансмуральные ИМ; в —субэндокардиальный (нетрансмуральный) ИМ; г — интрамуральный (нетрансмуральный) ИМ | 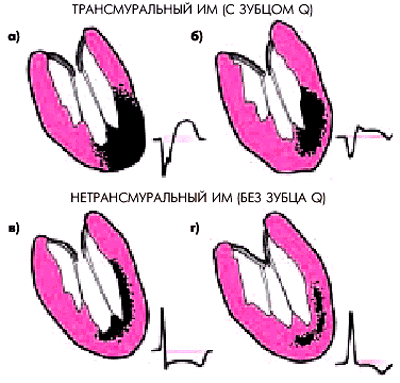
|
При нетрансмуральном ИМ (инфаркте миокарда без зубца Q) очаг некроза захватывает только субэндокардиальные или интрамуральные отделы ЛЖ (рис. 6.18, в, г) и не сопровождается патологическими изменениями комплекса QRS (“инфаркт миокарда без зубца Q”). В течение длительного времени в отечественной литературе для обозначения ИМ без зубца Q использовался термин “мелкоочаговый ИМ”. Действительно, в большинстве случаев ИМ без зубца Q существенно меньше по протяженности, чем трансмуральный инфаркт, хотя нередко встречаются случаи обширного субэндокардиального ИМ, распространяющегося на несколько сегментов ЛЖ, но затрагивающего только субэндокардиальные слои миокарда.
2. По характеру течения заболевания различают первичный, повторный и рецидивирующий ИМ.
Первичный ИМ диагностируется при отсутствии анамнестических и инструментальных признаков перенесенного в прошлом ИМ.
Повторный ИМ диагностируется в тех случаях, когда у больного, у которого имеются документированные сведения о перенесенном в прошлом ИМ, появляются достоверные признаки нового очага некроза, чаще формирующегося в бассейне других КА в сроки, превышающие 28 дней с момента возникновения предыдущего инфаркта.
При рецидивирующем ИМ клинико-лабораторные и инструментальные признаки формирования новых очагов некроза появляются в сроки от 72 ч (3 суток) до 28 дней после развития ИМ, т.е. до окончания основных процессов его рубцевания.
3. По локализации ИМвыделяют:
- переднесептальный (переднеперегородочный);
- передневерхушечный;
- переднебоковой;
- переднебазальный (высокий передний);
- распространенный передний (септальный, верхушечный и боковой);
- заднедиафрагмальный (нижний);
- заднебоковой;
- заднебазальный;
- распространенный задний;
- ИМ правого желудочка.
ИМ чаще локализуется в ЛЖ, поражая его переднюю, заднюю, боковую стенки или/и межжелудочковую перегородку (МЖП), что зависит от местоположения критического стеноза или окклюзии той или иной КА. Нарушение кровообращения по ПМЖВ ЛКА может привести к развитию ИМ переднеперегородочной области, верхушки и гораздо реже — заднедиафрагмальной (нижней) стенки ЛЖ. Прекращение кровотока по ОВ ЛКА сопровождается возникновением переднебазального, бокового или заднебазального ИМ (при окклюзии дистальных отделов ОВ ЛКА). При нарушении кровообращения в бассейне ПКА может развиться заднедиафрагмальный (при поражении проксимальных отделов ПКА) или заднебазальный ИМ (при окклюзии дистальных отделов ПКА). Изолированный инфаркт правого желудочка встречается сравнительно редко. Часто имеется сочетание ИМ различной локализации.
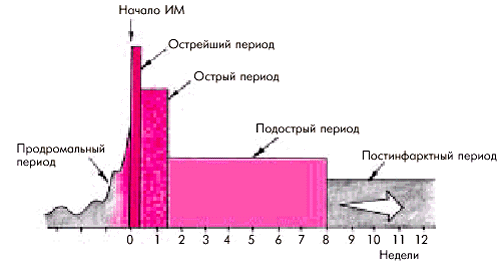
4. По стадии течения заболеванияразличают (рис. 6.19):
- острейший период — до 2 ч от начала ИМ;
- острый период — до 10 дней от начала ИМ;
- подострый период — с 10 дня до конца 4–8 недели;
- постинфарктный период — обычно после 4–8 недели.
|
| Рис. 6.19. Деление инфаркта миокарда на стадии. Объяснение в тексте |
Иногда выделяют так называемый продромальный период (“предынфарктное состояние”), который в известной степени соответствует понятию нестабильной стенокардии, осложнившейся развитием ИМ. Этот период можно выделить только ретроспективно, после состоявшегося ИМ, поскольку при возникновении клинической картины НС, хотя и возрастает риск развития острого ИМ или внезапной смерти, все же никогда нельзя с уверенностью сказать, завершится ли острый коронарный синдром развитием ИМ или нет.
5. К числу наиболее распространенных осложнений ИМ относятся:
- острая левожелудочковая недостаточность (отек легких);
- кардиогенный шок;
- желудочковые и наджелудочковые нарушения ритма;
- нарушения проводимости (СА-блокады, АВ-блокады, блокады ножек пучка Гиса);
- острая аневризма ЛЖ;
- внешние и внутренние разрывы миокарда, тампонада сердца;
- асептический перикардит (эпистенокардитический);
- тромбоэмболии.
| 6.4.2. Этиология и патогенез |

|
Основной причиной развития ИМ является атеросклероз КА (95%). Следует также иметь в виду, что довольно редко (не более чем у 5% больных) ИМ может развиться в результате эмболии КА (инфекционный эндокардит, внутрижелудочковые тромбы), врожденных дефектов развития венечных сосудов и других поражений КА (коронарииты при системной красной волчанке, ревматизме, ревматоидном артрите) и т.д. Однако в этих случаях ИМ расценивается не как клиническая форма ИБС, а как осложнение одного из перечисленных заболеваний (см. главу 5).
В большинстве случаев прекращение или резкое ограничение коронарного кровотока наступает в результате тромбоза КА, который обычно развивается в области “осложненной” атеросклеротической бляшки, истонченная капсула которой оказывается поврежденной (надрыв, изъязвление, обнажение липидного ядра бляшки). Это способствует активации тромбоцитарных и плазменных факторов свертывания крови тканевым тромбопластином и коллагеном.
Вначале образуется тромбоцитарный “белый” пристеночный тромб. Одновременно в этой области выделяется ряд биологически активных веществ, обладающих мощным вазоконстрикторным действием (эндотелин, серотонин, тромбин, антитромбин А2). В результате возникает выраженный спазм стенозированной КА, еще больше ограничивающий кровоток по венечной артерии. Кроме того, мелкие тромбоцитарные агрегаты могут эмболизировать венечные сосуды на микроциркуляторном уровне, что еще больше ограничивает коронарный кровоток.
Постепенно размеры пристеночного тромба увеличиваются и, если не происходит его спонтанного лизиса в результате естественной активации собственной фибринолитической системы или не проводится тромболитическая терапия, тромб полностью окклюзирует просвет сосуда и развивается трансмуральный ИМ (инфаркт с зубцом Q).
В тех случаях, когда по разным причинам полной окклюзии КА не происходит или возникает спонтанный лизис тромба, может развиться субэндокардиальный или интрамуральный ИМ (инфаркт без зубца Q). Последний может развиться и при полной окклюзии КА, если хорошо выражены коллатерали.
Важно помнить, что в большинстве случаев (около 75%) процесс формирования тотального тромба, полностью перекрывающего просвет крупной КА, может занимать от 2-х дней до 2–3 недель. В этот период клиническая картина прогрессирующего ухудшения коронарного кровотока в целом соответствует симптоматике нестабильной стенокардии (предынфарктный синдром).
Гораздо реже (примерно у 1/4 больных ИМ) процесс формирования тотального, полностью окклюзирующего тромба, протекает молниеносно. В этих случаях в клинической картине заболевания отсутствует симптоматика продромального периода.
Быстрому формированию очага некроза в сердечной мышце могут способствовать еще 3 дополнительных фактора:
- выраженный спазм КА;
- слабое развитие коллатеральных сосудов;
- выраженное увеличение потребности миокарда в кислороде в результате физического или психоэмоционального напряжения, подъема АД и других причин.
Все три фактора ведут к увеличению скорости формирования очага некроза и его объема. Наоборот, в условиях хорошо развитого коллатерального кровообращения даже полная, но постепенная, окклюзия КА в отдельных случаях может не сопровождаться развитием ИМ.
В научной литературе до сих пор обсуждается вопрос о том, возможно ли развитие ИМ за счет длительного и выраженного спазма венечной артерии или нарушения кровообращения на микроциркуляторном уровне. Не исключено, что эти механизмы могут лежать в основе некоторых случаев не-Q-инфаркта, особенно при наличии у больных значительного органического сужения венечного сосуда. Тем не менее этот вопрос требует дальнейшего изучения.
 Запомните
1. Острый инфаркт миокарда в большинстве случаев развивается в результате образования в области “осложненной” атеросклеротической бляшки тромба, полностью или частично ограничивающего коронарный кровоток. Выраженный спазм КА, слабое развитие коллатералей и увеличение потребности миокарда в кислороде на фоне нагрузки являются дополнительными факторами, усугубляющими коронарную недостаточность и ведущими к увеличению объема очага некроза и скорости его формирования. 2. При полной окклюзии КА (органической и динамической), сохраняющейся в течение длительного времени, и слабом развитии коллатералей формируется трансмуральный ИМ (инфаркт с зубцом Q). 3. При наличии пристеночного тромба, частично ограничивающего коронарный кровоток, и/или развитой сети коллатералей развивается нетрансмуральный ИМ (инфаркт без зубца Q). Запомните
1. Острый инфаркт миокарда в большинстве случаев развивается в результате образования в области “осложненной” атеросклеротической бляшки тромба, полностью или частично ограничивающего коронарный кровоток. Выраженный спазм КА, слабое развитие коллатералей и увеличение потребности миокарда в кислороде на фоне нагрузки являются дополнительными факторами, усугубляющими коронарную недостаточность и ведущими к увеличению объема очага некроза и скорости его формирования. 2. При полной окклюзии КА (органической и динамической), сохраняющейся в течение длительного времени, и слабом развитии коллатералей формируется трансмуральный ИМ (инфаркт с зубцом Q). 3. При наличии пристеночного тромба, частично ограничивающего коронарный кровоток, и/или развитой сети коллатералей развивается нетрансмуральный ИМ (инфаркт без зубца Q).
|
Нарушения метаболизма сердечной мышцы
Возникновение ишемии сердечной мышцы приводит к глубоким нарушениям в метаболизме кардиомиоцитов и клеток проводящей системы сердца. В результате прекращения или значительного ограничения коронарного кровотока развивается гипоксия, которая нарушает синтез АТФ в митохондриях. При этом сократительная функция кардиомиоцитов быстро снижается.
Значительное ограничение поступления с коронарным кровотоком жирных кислот и глюкозы, являющихся основным энергетическим субстратом клеток, активизирует анаэробный гликолиз (распад гликогена). Причем гликоген метаболизируется лишь до лактата, который в условиях дефицита кислорода дальше не окисляется (см. рис. 5.49). Концентрация лактата и других недоокисленных продуктов в сердечной мышце и крови коронарного синуса возрастает, и в миокарде происходит сдвиг рН в кислую сторону (ацидоз), который способствует еще большему снижению электрической активности и сократимости миокарда.
Дефицит АТФ приводит к раскрытию калиевых каналов клетки, ионы К+ выходят во внеклеточную среду, снижая тем самым трансмембранный потенциал покоя и возбудимость кардиомиоцитов. Одновременно уменьшается скорость нарастания ТМПД, общая его продолжительность (рис. 6.20), а также скорость проведения электрического импульса. Характерно, что степень этих нарушений в отдельных участках ишемизированного миокарда различна. Поэтому при ишемии создаются условия для возникновения выраженной негомогенности электрофизиологических свойств сердечной мышцы, лежащей в основе многих нарушений сердечного ритма.
В результате ишемии нарушается также обратный транспорт ионов Са2+ в саркоплазматический ретикулум и внеклеточную среду. Kонцентрация Са2+ в клетке возрастает, и развивается так называемая “ишемическая контрактура” кардиомиоцитов, ведущая к нарушению процесса диастолического расслабления
Значительное угнетение функции К+-Nа+–насоса, возникающее в результате дефицита АТФ, сопровождается также повышением концентрации ионов Nа+ в клетке и, соответственно, ее отеком.
 Запомните
Ишемия миокарда приводит к многочисленным расстройствам метаболизма и функции клеток сердца, основными из которых являются: Запомните
Ишемия миокарда приводит к многочисленным расстройствам метаболизма и функции клеток сердца, основными из которых являются:
|
| Рис. 6.20. Изменение трансмембранного потенциала действия (ТМПД) в зоне ишемического повреждения. Обьяснения в тексте. | 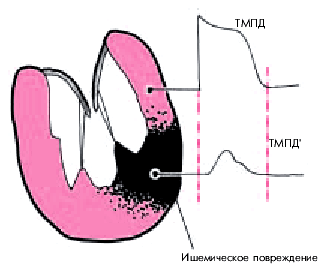
|
Морфологические данные
Самые ранние морфологические изменения в сердечной мышце при развивающемся ИМ можно выявить только при использовании электронной микроскопии. Уже через 15–20 мин после коронарной окклюзии обнаруживают набухание митохондрий и истощение гликогена. Через 60 мин после прекращения коронарного кровообращения выявляется необратимое ишемическое повреждение клетки в виде распада хроматина ядер и выраженной контрактуры саркомеров.
При использовании световой микроскопии первые изменения в очаге ИМ обнаруживаются только через 12–18 ч от начала инфаркта. Наблюдается расширение капилляров, отек мышечных волокон. Через 24 ч выявляется фрагментация мышечных волокон и инфильтрация полиморфно-ядерными лейкоцитами.
Макроскопически картина ИМ начинает выявляться только через 18–24 ч от начала заболевания. Очаг некроза выглядит бледным и отечным, а через 48 ч зона некроза приобретает серый оттенок и становится дряблой.
При неосложненном течении процесс формирования рубца завершается примерно через 6 недель от начала ИМ.
Последствия инфаркта миокарда
В результате возникновения ИМ происходит нарушение диастолической и систолической функций ЛЖ, а также начинается сложный процесс его ремоделирования. Одновременно наблюдаются значительные изменения функционального состояния других органов и систем.
Диастолическая дисфункция ЛЖ является одним из первых проявлений ишемии и развивающегося ИМ. Диастолическая дисфункция обусловлена повышением ригидности (снижением податливости) сердечной мышцы во время диастолы.
Начальные стадии диастолической дисфункции характеризуются снижением скорости диастолического расслабления и объема раннего диастолического наполнения (в фазу быстрого наполнения желудочка). При этом увеличивается объем кровотока во время систолы левого предсердия. Значительная часть диастолического наполнения ЛЖ осуществляется только в конце диастолы, во время систолы ЛП.
Дальнейшее ухудшение диастолической функции ЛЖ приводит к росту КДД в ЛЖ, давления наполнения и среднего давления в ЛП и венах малого круга кровообращения, что существенно повышает риск возникновения застоя крови в легких.
Систолическая дисфункция ЛЖ проявляет себя 1) в нарушении региональной сократимости ЛЖ и 2) в появлении признаков глобальной систолической дисфункции ЛЖ.
Нарушения локальной сократимости ЛЖ при ИМ развиваются очень рано. Вначале они напоминают таковые, обнаруживаемые у больных стабильной стенокардией во время проведения нагрузочных тестов или у пациентов НС после ангинозного приступа (см. выше). Однако уже через сутки от начала ИМ гипокинезия некротизирующегося участка сердечной мышцы, отражающая функцию гибернирующего (“спящего” в условиях выраженной ишемии) миокарда, сменяется ее акинезией — отсутствием во время систолы сокращения некротизированного участка сердечной мышцы. Наиболее серьезным нарушением локальной сократимости является дискинезия — парадоксальное выбухание участка некроза в момент систолы.
Наконец, в области неповрежденной сердечной мышцы нередко наблюдается локальная гиперкинезия — некоторое увеличение сократимости интактных участков ЛЖ, которая носит компенсаторный характер.
Снижение глобальной систолической функции ЛЖ при ИМ заключается
- в уменьшении ФВ, УО, СИ, МО, АД;
- в повышении КДД и КДО ЛЖ;
- в появлении клинических признаков левожелудочковой недостаточности и застоя крови в малом круге кровообращения;
- в появлении признаков системных расстройств периферического кровообращения, в том числе на микроциркуляторном уровне.
Насосная функция ЛЖ при ИМ определяется многими факторами, в первую очередь, распространенностью очага некроза.
 Запомните
Между выраженностью снижения глобальной систолической функции ЛЖ и величиной очага некроза существует прямая зависимость (С. Rаskley): 1. При величине некроза, превышающей 10% массы миокарда ЛЖ, наблюдается снижение ФВ. 2. При вовлечении в некротический процесс более 15% массы ЛЖ к этим изменениям присоединяется повышение КДД и КДО ЛЖ. 3. Если область некроза превышает 40% от общей массы миокарда ЛЖ, развивается кардиогенный шок (см. ниже). Запомните
Между выраженностью снижения глобальной систолической функции ЛЖ и величиной очага некроза существует прямая зависимость (С. Rаskley): 1. При величине некроза, превышающей 10% массы миокарда ЛЖ, наблюдается снижение ФВ. 2. При вовлечении в некротический процесс более 15% массы ЛЖ к этим изменениям присоединяется повышение КДД и КДО ЛЖ. 3. Если область некроза превышает 40% от общей массы миокарда ЛЖ, развивается кардиогенный шок (см. ниже).
|
Понятно, что в каждом конкретном случае заболевания такая зависимость может существенно нарушаться, поскольку еще большее ухудшение гемодинамики может быть связано с наличием острой аневризмы ЛЖ, появлением митральной регургитации при инфаркте сосочковых мышц или перфорацией МЖП, выраженной гипертрофии миокарда, наличием диастолической дисфункции сердечной мышцы, уровнем АД, а также состоянием соседних с инфарктом участков миокарда, не вовлеченных в процесс инфарцирования (величиной их кровоснабжения, наличием в этой зоне рубцов после перенесенного в прошлом ИМ) и т.п.
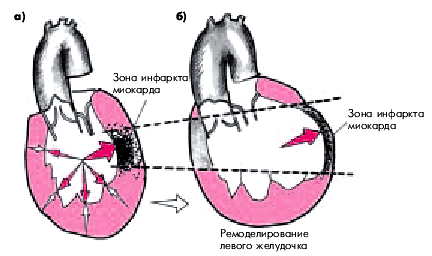
Ремоделирование ЛЖ при ИМ — это совокупность изменений структуры и функции ЛЖ, обусловленных формированием в сердечной мышце ИМ. Наиболее существенные изменения происходят при трансмуральном ИМ. Формирующийся в стенке ЛЖ обширный очаг некроза испытывает на себе высокое внутрижелудочковое давление, создаваемое интактным миокардом желудочка во время систолы (рис. 6.21, а). Поскольку этот участок некроза не участвует в сокращении и не оказывает сопротивления внутрижелудочковому давлению, он довольно быстро начинает растягиваться и истончаться. В результате площадь инфаркта, а также общие размеры ЛЖ, увеличиваются (рис. 6.21, б).
Поскольку часть сердечной мышцы выпадает из сокращения, а полость ЛЖ становится расширенной, неповрежденные участки миокарда испытывают избыточную нагрузку, что приводит вначале к их гиперфункции, а затем и гипертрофии. Одновременно еще больше увеличивается КДО ЛЖ, что поначалу, согласно механизму Старлинга, позволяет поддерживать сердечный выброс на должном уровне.
|
| Рис. 8.21. Ремоделирование левого желудочка при трансмуральном инфаркте миокарда. а - влияние ситолического внутрижелудочного давления на некротизированный участок сердечной мышцы (2-е сутки ИМ); б - увеличение площади инфаркта, истончение стенки в области некроза и дилатация ЛЖ |
 Запомните
Ремоделирование ЛЖ при остром ИМ заключается в формировании следующих структурных изменений: Запомните
Ремоделирование ЛЖ при остром ИМ заключается в формировании следующих структурных изменений:
|
Ремоделирование ЛЖ больше выражено у больных с обширным передним трансмуральным ИМ. В этих случаях ремоделирование начинается уже через 24 ч от начала инфаркта и продолжается в течение длительного времени (недели и месяцы). В конечном счете ремоделирование усугубляет нарушения систолической и диастолической функций желудочка и способствует возникновению левожелудочковой СН.
На выраженность процесса ремоделирования влияют несколько факторов.
1. Размеры ИМ (чем больше площадь инфаркта, тем более выраженными оказываются структурные изменения в ЛЖ).
2. Размер периинфарктной зоны (области ишемизированного или гибернирующего миокарда, непосредственно граничащей с зоной некроза).
3. Механические свойства зоны некроза (в последующем — рубцовой зоны).
4. Величина постнагрузки, в том числе уровень АД, ОПСС, размеры полости ЛЖ и др.
5. Величина преднагрузки (объем венозного возврата крови к сердцу).
6. Гиперактивация САС.
7. Гиперактивация РААС, в том числе тканевых РАС.
8. Гиперпродукция эндотелина и других вазоконстрикторных субстанций.
Дата добавления: 2016-04-22; просмотров: 569;
