ОВТВ, образующие метгемоглобин
Как уже указывалось, железо, входящее в структуру гемоглобина – двухвалентно, не зависимо от того, связан пигмент крови с кислородом (HbO) или нет (Hb). Более того, только находясь в двухвалентном состоянии Fe+2 обладает необходимым для осуществления транспортных функций сродством к кислороду.
В нормальных условиях спонтанно и под влиянием различных патогенных факторов, в том числе химической природы, двухвалентное железо гемоглобина окисляется, переходя в трёхвалентную форму. Образуется так называемый метгемоглобин (MetHb). Метгемоглобин не участвует в переносе кислорода от легких к тканям, поэтому значительное повышение его содержания в крови представляет опасность. Эволюционно сформировались механизмы обратного превращения метгемоглобина в гемоглобин. Благодаря этим механизмам у здорового человека уровень метгемоглобина в крови не превышает 0,5 - 2%. Существуют два основных пути, защиты железа гемоглобина от окисления.
Первый связан с “обезвреживанием” проникающих в эритроциты ксенобиотиков-окислителей до момента их действия на гемоглобин. Так, в присутствии энзима глутатионпероксидазы (ГПО) восстановленный глутатион взаимодействует с молекулами-окислителями, попавшими в клетки крови, предотвращая их метгемоглобинобразующее действие. Несостоятельность этого механизма (снижение активности глутатионпероксидазы, содержания восстановленного глутатиона в эритроцитах), может привести к умеренной метгемоглобинемии и появлению в крови телец Гейнца (продукты денатурации гемоглобина).
Второй механизм обеспечивает восстановление уже образовавшегося в крови метгемоглобина при участии двух ферментативных систем: НАДН-зависимой и НАДФН-зависимой метгемоглобинредуктаз. В одной из них донорами электронов (восстанавливающие агенты) являются продукты анаэробного этапа метаболизма глюкозы (НАДН), в другой - гексозомонофосфатного превращения (НАДФН) (рис. 27):
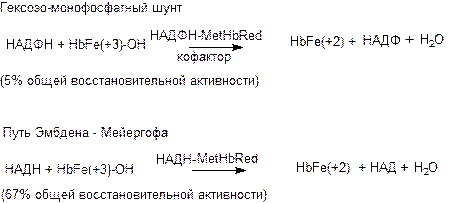
Рисунок 27. Механизмы восстановления метгемоглобина
В количественном отношении более значимым является механизм, связанный с гликолизом. Однако в процессе гексозомонофосфатного превращения под влиянием гексозо-6-фосфатдегидрогеназы (Г-6ф-ДГ) образуется восстановленный никатинамидадениндинуклеотд фосфат (НАДФН), который не только участвует в превращении метгемоглобина в гемоглобин в присутствии НАДФН-метгемоглобинредуктазы, но и в восстановлении окисленного глутатиона при участии НАДФН-зависимой глутатионредуктазы. Поэтому значение этого пути “защиты” гемоглобина также велико. По этой причине лица с врожденной недостаточностью Г-6Ф-ДГ весьма чувствительны даже к относительно невысоким дозам целого ряда токсикантов.
Основной причиной массивного образования метгемоглобина в крови до уровня, порой угрожающего жизни человека, является действие на организм химических веществ, так называемых метгемоглобинообразователей(оксидов азота, органических и неорганических нитро- и аминосоединений, фенолов, хлоратов, сульфонов и т.д.). Наряду с MetHb при интоксикациях подобными веществами в крови нередко появляется и другой продукт повреждения гемоглобина - сульфгемоглобин. В отличие от MetHb, который легко восстанавливается в организме за счет редуктазных ферментных систем обратно до гемоглобина, сульфгемоглобин представляет собой необратимый дериват Hb. Он никогда не встречается в нормальной крови и также не способен обратимо присоединять кислород, хотя и содержит двухвалентное железо.
Наиболее токсичные метгемоглобинообразователи относятся к одной из следующих групп:
1. Соли азотистой кислоты (нитрит натрия)
2. Алифатические нитриты (амилнитрит, изопропилнитрит, бутилнитрит)
3. Ароматические амины (анилин, аминофенол)
4. Ароматические нитраты (динитробензол, хлорнитробензол)
5. Производные гидроксиламина (фенилгидроксиламин)
6. Производные гидразина (фенилгидразин).
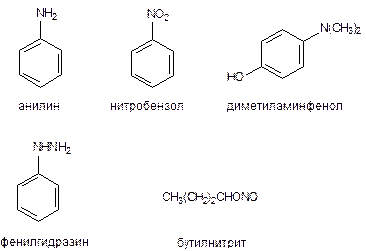
Некоторые из указанных веществ могут представлять интерес для военной медицины либо как возможные диверсионные агенты (нитрит натрия), либо как промышленные агенты весьма опасные в плане образования зон химического заражения при авариях и катастрофах (анилин, динитробензол).
Попав в организм, мегемоглобинообразователи либо непосредственно активируют процессы, приводящие к окислению железа гемоглобина, либо первоначально метаболизируют с образованием реактивных продуктов, которые обладают этим свойством. Тяжесть развивающейся при этом патологии определяется дозой и скоростью поступления токсиканта в организм, а затем в эритроциты, их окислительно-восстановительным потенциалом, скоростью элиминации. Если действующим агентом является не исходное вещество, а продукт его метаболизма, то глубина патологического процесса зависти также от интенсивности процесса биоактивации ксенобиотика в организме. Поэтому у различных экспериментальных животных при введении им веществ, подвергающихся биоактивации, скорость образования метгемоглобина, как правило, существенно различается (табл. 28).
Таблица 28.
Дата добавления: 2016-04-14; просмотров: 777;
