Механизм токсического действия. Оксид углерода in vitro активно взаимодействует с многочисленными гем-содержащими протеидами (гемоглобин
Оксид углерода in vitro активно взаимодействует с многочисленными гем-содержащими протеидами (гемоглобин, миоглобин, цитохромы и т.д.) при условии, что железо, входящее в структуру порфиринового кольца их простетической группы, находится в двухвалентном состоянии. Связь двухвалентного железа с СО - обратима. С трехвалентным железом вещество не взаимодействует.
Оксид углерода, проникший в кровь, вступает во взаимодействие с гемоглобином (Hb) эритроцитов, образуя карбоксигемоглобин (HbCO), не способный к транспорту кислорода. Развивается гемический тип гипоксии. Оксид углерода способен взаимодействовать как с восстановленной (Hb), так и с окисленной (HbO) формой гемоглобина, поскольку в обеих формах железо двухвалентно.
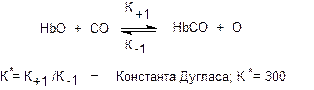
Степень сродства токсиканта к гемоглобину может быть охарактеризована константой равновесия реакции взаимодействия (константа Дугласа). Установлено, что у человека, хотя скорость присоединения CO к гемоглобину в 10 раз ниже скорости присоединения кислорода, скорость диссоциации карбоксигемоглобина приблизительно в 3600 раз меньше соответствующей скорости для оксигемоглобина. Поэтому относительное сродство Hb к CO примерно в 300 раз выше, чем к кислороду. Величина константы Дугласа у животных разных видов различна (у лошади – 240, канарейки – 100, кролика – 40). В состоянии равновесия СО, в концентрации 1 объемная часть на 1000 объемных частей воздуха, превращает 50% гемоглобина крови человека в карбоксигемоглобин. Как правило, в реальных условиях, концентрация 0,1% СО во вдыхаемом воздухе обусловливает образование около 10% карбоксигемоглобина в крови.
Количество карбоксигемоглобина, образовавшегося в крови в начале воздействия яда, может быть рассчитано по формуле Лилиенталя (1946):
% НbСО = (рСО t МОД) 0,05 , где
pСО – парциональное давление СО во вдыхаемом воздухе;
t – время экспозиции в минутах;
МОД – минутный объем дыхания в литрах.
Поскольку карбоксигемоглобин не в состоянии переносить кислород от легких к тканям существует тесная корреляция между его уровнем в крови и выраженностью клинической картины отравления. Экспозиция 0,5% СО в течение часа при умеренной физической активности сопровождается образованием 20% карбоксигемоглобина, при этом пострадавший начинает испытывать неприятные ощущения, предъявляет жалобы на головную боль. Интоксикация средней степени тяжести развивается при содержании крабоксигемоглобина 30 - 50%, тяжелая - около 60% и выше. Смертельные исходы при отравлении СО в эксперименте на животных наблюдаются при уровне HbСО в крови - 60-70%. Вместе с тем механическое удаление 70% гемоглобина или ингаляция воздуха с пониженным парциальным давлением О2 (и снижение тем самым содержания HbО до уровня 30%) к смерти экспериментальных животных не приводят. Это наблюдение косвенно указывает на наличие дополнительных механизмов токсического действия СО. По существующим представлениям они состоят в следующем.
Во-первых, оксид углерода не только выключает из транспорта О2 часть гемоглобина, но также нарушает явление гем-гем взаимодействия, затрудняя тем самым процесс диссоциации HbО в крови отравленного и передачу транспортируемого кислорода тканям (Л.А. Тиунов, В.В. Кустов, 1969). Эффект еще более усиливается по мере развития интоксикации и понижения парциального давления СО2 в крови и тканях (эффект Бора).
Во-вторых, СО взаимодействует не только с гемоглобином, но также с целым рядом различных цитохромов (цитохромом “а”, цитохромом “С”, цитохромом Р-450 и т.д.), угнетая тем самым биоэнергетические процессы в тканях (развивается гистотоксический тип гипоксии - см. ниже). Поскольку валентность железа тканевых цитохромов переменна, они становятся уязвимыми для действия токсиканта при переходе в состояние Fe+2. Это состояние наиболее вероятно в условиях снижения парциального давления кислорода в тканях (при гипоксии). Так, установлено, что экспериментальные животные, находящиеся под воздействием газовой смеси 3 атм. кислорода и 1 атм. оксида углерода, не погибают, хотя при этих условиях практически весь Hb превращается в HbCO. Тем не менее, тканевые цитохромы резистентны к действию СО (железо находится преимущественно в трехвалентной форме), а растворенного в плазме крови кислорода оказывается достаточно, чтобы удовлетворить потребность в нем тканей. При изменении соотношения газовой смеси 3 атм. кислорода и 2 атм. оксида углерода животные погибают, несмотря на то, что количество растворенного в плазме крови кислорода остается таким же, как в первом опыте. Развитие интоксикации в этом случае можно объяснить угнетением системы цитохромов – нарушением тканевого дыхания.
Наконец, СО активно взаимодействует с миоглобином (сродство в 14 - 50 раз выше, чем к кислороду), пероксидазой, медь-содержащими ферментами (тирозиназа) тканей. Миоглобин (мышечный пигмент - аналог гемоглобина, состоящий из одной молекулы глобина, связанной с гемом) в организме выполняет функцию депо кислорода, а также значительно ускоряет диффузию кислорода в мышечной ткани. Взаимодействие оксида углерода с миоглобином приводит к образованию карбоксимиоглобина. Нарушается обеспечение работающих мышц кислородом. Этим отчасти объясняют развитие у отравленных выраженной мышечной слабости.
Определение карбоксигемоглобина в крови
Для уточнения диагноза отравления оксидом углерода – производится определение HbCO в крови различными физико-химическими и химическими методами.
Существуют довольно простые экспресс-методы определения содержания HbCO в крови: проба с разведением, проба с кипячением, проба со щелочью, проба с медным купоросом, проба с формалином. Принцип методов основан на большей устойчивости HbCO (сохраняет розовую окраску в растворе), в сравнении с HbO к денатурирующим воздействиям. Их чувствительность находится в пределах 25-40% HbCO.
Количественное определение содержания HbCO в крови производят спектрометрическими, фотометрическими, колориметрическими и газоаналитическими методами. Наиболее чувствительны фотометрический и спектрофотометрический методы, позволяющие определять HbCO в крови, начиная с 0,5-1%.
При необходимости направления проб в лабораторию для определения наличия HbCO необходимо исключить контакт содержимого пробирок с воздухом, например, путем наслаивания вазелинового масла.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
- использование индивидуальных технических средств защиты (средства защиты органов дыхания; при применении карбонилов металлов - средства защиты органов дыхания и кожи) в зоне химического заражения;
Специальные профилактические медицинские мероприятия:
- применение антидота перед входом в зону пожара;
- проведение санитарной обработки пораженных карбонилами металлов на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
- своевременное выявление пораженных;
- применение антидотов и средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само-взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим.
- подготовка и проведение эвакуации
Дата добавления: 2016-04-14; просмотров: 894;
