ХІМІЧНІ ВЛАСТИВОСТІ. Хімічні властивості алкінів зумовлені наявністю в їх молекулі потрійного С≡С зв’язку, тому для них
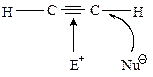
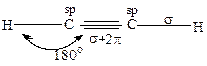 Хімічні властивості алкінів зумовлені наявністю в їх молекулі потрійного С≡С зв’язку, тому для них, як і для алкенів, характерні реакції приєднання. Однак, слід зауважити, що π-електронна густина потрійного зв’язку в ацетилені важче поляризується, ніж подвійного в етилені, оскільки електронегативність атома вуглецю в sp-гібридному стані вища, ніж у sp2-стані. Внаслідок цього, π-електрони потрійного зв’язку сильніше утримуються атомами вуглецю, більшу стягнуті в середину молекули і є менше рухливі ніж π-електрони зв’язку С=С. Крім того, довжина потрійного С≡С-зв’язку менша від довжини подвійного С=С зв’язку. В результаті, алкіни проявляють меншу реакційну здатність у реакціях електрофільного приєднання (АЕ) у порівнянні з алкенами.
Хімічні властивості алкінів зумовлені наявністю в їх молекулі потрійного С≡С зв’язку, тому для них, як і для алкенів, характерні реакції приєднання. Однак, слід зауважити, що π-електронна густина потрійного зв’язку в ацетилені важче поляризується, ніж подвійного в етилені, оскільки електронегативність атома вуглецю в sp-гібридному стані вища, ніж у sp2-стані. Внаслідок цього, π-електрони потрійного зв’язку сильніше утримуються атомами вуглецю, більшу стягнуті в середину молекули і є менше рухливі ніж π-електрони зв’язку С=С. Крім того, довжина потрійного С≡С-зв’язку менша від довжини подвійного С=С зв’язку. В результаті, алкіни проявляють меншу реакційну здатність у реакціях електрофільного приєднання (АЕ) у порівнянні з алкенами.
Однак, з боку атомів водню існує деякий дефіцит електронної густини, яка зміщена до центру потрійного зв’язку. Тому алкіни можуть вступати в реакції нуклеофільного приєднання (АN). Причому нуклеофіл атакує молекулу ацетилена з «торця».
У молекулі ацетилену зв’язок С¾Н, утворений sp-гібридною орбіталлю атома С. Відомо, що електронегативність гібридної орбіталі зростає зі збільшенням у ній частки s-орбіталі: sp3 – 2,5; sp2 – 2,75; sp – 3,2 (за шкалою Л.Полінга, див. табл. . на стор. ).
Тому в цьому ж ряду зростає і полярніть зв’язку С¾Н, що веде до протонізації атомів водню.
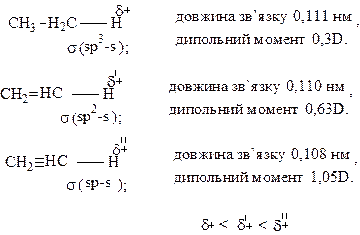
Отже, атоми водню в ацетилені протонізовані значно більше, ніж в етилені або в етані, про що свідчать значення констант іонізації цих сполук: рК (ацетилен) = 25; рК (етилен) = 44. Для порівняння рК (Н2О) = 15,7. Отже ацетилен проявляє кислотні властивості, хоч є слабшою кислотою, ніж вода.
Дата добавления: 2016-02-11; просмотров: 996;
