Созревание висцеральных функций.
Эндокринная система.Во время внутриутробного развития организм постоянно находится под влиянием гормонов, даже в то время, когда они им еще не вырабатываются. Так, например, материнские стероидные гормоны в разной степени проходят через плаценту и воздействуют на плод. Некоторые гормоны продуцирует плацента. Вырабатываемые плацентой гормоны обуславливают развитие приспособительных изменений и в организме беременной женщины: стимулируется пролиферация в молочных железах, трансформируется эндометрий, тормозится сократительная деятельность беременной матки (хорионический гонадотронин, хорионический лактосомато-гронин, прогестерон, в поздние сроки беременности — эстрогены).
Большинство собственных гормонов плода начинает синтезироваться уже на 2-3 месяце внутриутробного развития, причем, к моменту рождения их концентрация в крови плода резко увеличивается и существенно превышает соответствующий уровень у взрослого человека. После рождения содержание гормонов падает, но это не лишает новорожденного важного механизма регуляции, поскольку в молоке кормящей матери содержится большое количество компонентов, компенсирующих дефицит выработки гормонов организмом ребенка и определяющих его развитие. Таким образом, материнское молоко, кроме питательной, ферментативной и иммунологической ценности, играет еще и роль поставщика гормонов. Особенно велика в нем концентрация пролактина. В случае его дефицита (например, при искусственном вскармливании) возникают отдаленные эндокринные нарушения — гиперпролатинемический гипогонадизм, нарушается обмен дофамина; более половины женщин, получавших в раннем детстве искусственное вскармливание, страдают бесплодием.
Роль гормонов в молоке матери состоит, во- первых, в том, что в условиях незавершенности развития нейроэндокринных механизмов младенца они повышают его адаптационные возможности в новых условиях существования. Во-вторых, эти гормоны необходимы для нормального созревания механизмов мозга. Так, например, дефицит пролактина в материнском молоке нарушает развитие до-фаминергической системы мозга ребенка.
В перинатальный и ранний постнатальный периоды высока потребность развивающегося мозга в анаболических и тиреоидных гормонах, ибо в это время осуществляется синтез белков нервной
ткани и идет процесс ее миелинизации. Помимо гуморальной связи мать — дитя существует и рефлекторный канал связи: акт сосания вызывает у матери усиление секреции пролактина и окситоцина, в результате чего, продуцируется больше молока. Однако, увеличение синтеза и секреции гормонов (первые посредники) еще не означает повышения их влияния на клеточную мембрану органов — мишеней ребенка, т.к. необходимо еще и достаточное созревание на мембранах механизма, обеспечивающего образование второго посредника (цАМФ), который многократно усиливает действие гормона на ткань.
Гипоталамо- гипофизарная система.Специфическое действие ад-ренокортикотропного гормона (АКТГ) на надпочечники начинается только на 7-м месяце внутриутробного периода, когда увеличивается скорость образования в надпочечниках гидрокортизона и тестостерона. У новорожденного функционируют все звенья гипоталамо-гипофизарно-надпочечниковой системы. Уже с первых часов после рождения дети на стрессорные раздражения реагируют повышением содержания кортикостероидов в крови и моче.
У новорожденных гормон роста, или соматотропный гормон (СТГ), участвует в реакциях иммунологической защиты (существует прямая зависимость между концентрацией СТГ в крови и количеством лимфоцитов). Но главное — СТГ стимулирует рост эпифизар-ных хрящей. Эта функция реализуется при нормальной деятельности щитовидной и поджелудочной желез, а также половых гормонов.
Плод растет намного быстрее, чем ребенок, но это зависит не столько от СТГ, сколько от плацентарных гормонов, поступления питательных веществ от матери и генетической программы развития. Плоды- ан-энцефалы, у которых отсутствует гипофиз, также растут с нормальной скоростью. Врожденная или приобретенная недостаточность гипофиза приводит, однако, к замедлению роста детей и гипофизарной карликовости; повышенная продукция СТГ у детей, наоборот — к высокому росту.
В отличие от других гормонов секреция тиреотропного гормона (ТТГ) сразу после рождения резко усиливается. Это способствует адаптации новорожденного к новым условиям, которые являются для него экстремальными.
Пролактин (ПРЛ) особенно увеличивается у девочек в пубертатный период; с установлением менструальных циклов концентрация ПРЛ в крови изменяется циклически: максимума она достигает за день до овуляции, минимума — перед или во время менструации. У мальчиков-подростков ПРЛ в наибольшей степени стимулирует рост предстательной железы и семенных пузырьков.
Гонадотропины-фолликулостимулирующий и лютеинизирующий гормоны (ФСГ и ЛГ) — усиливают выработку половых гормонов в надпочечниках и половых железах. Уже во внутриутробном периоде формируется прочная связь между гонадотропной функцией гипофиза, гормонами половых желез и гипоталамусом. В пубертатном периоде происходит закономерное увеличение секреции гонадотро-пинов. У девочек это вызывает рост и развитие яичников и появ-
160
ление цикличной секреции ФСГ и ЛГ. Однако, концентрация этих гормонов выходит на взрослый уровень лишь к 18 годам.
Содержание гормона нейрогипофиза вазопрессина, или антидиуретического гормона (АДГ), к моменту рождения ребенка увеличивается, в первые сутки после рождения резко снижается, затем повышается, достигая максимума у годовалых детей. Однако, новорожденные при любом водном режиме выводят гипотоничную мочу. Одна из причин — нечувствительность почек к АДГ в этот возрастной период.
Второй гормон нейрогипофиза — окситоцин у детей выполняет лишь антидиуретическую функцию, а матка и молочные железы реагируют на него после завершения пубертатного периода (когда матка подвергается длительному предварительному воздействию эстрогенов и прогестерона, а молочные железы — воздействию про-лактина).
Надпочечники принимают участие в адаптационных реакциях организма с первых дней жизни ребенка. Нарушения функции коры надпочечников у детей не только снижают адаптацию к стрессу, но вызывают и другие последствия: у девочек развиваются вторичные половые признаки, свойственные мужскому типу, ослабевает умственное и физическое развитие.
На ранних стадиях развития плода мозговое вещество надпочечников вырабатывает исключительно норадреналин, но доля адреналина постепенно увеличивается. Функция катехоламинов, секретиру-емых плодом во время родов, в основном, заключается в предупреждении у него гипогликемии путем стимуляции гликогенолиза. Мозговой слой надпочечников, как и корковый, способен реагировать на стресс с первых дней жизни ребенка. С возрастом секреция катехоламинов нарастает (табл. 18.2), увеличивается активность всей симпатоадреналовой системы. Реакция симпатоадреналовой системы на стресс у детей и подростков более выражена, чем у взрослых.
Таблица 18.2Содержание катехоламинов в моче (в мкг/сут) в различные возрастные периоды у здоровых детей
| Возраст | Адреналин | Норадреналин | |||
| — 15 дней | 0.06 - | 0.2 | 0.9 | - 3.63 | |
| - 2 мес. | 0.2 - | 0.68 | 1.68 | - 3.8 | |
| - 5 мес. | 0.4 - | 1.0 | 2.9 | - 7.9 | |
| - 12 мес. | 0.5 - | 1.1 | 3.4 | - 9.0 | |
| — 3 года | 0.7 - | 1.7 | 4.0 | - 12.0 | |
| — 10 лет | 1.7 - | 3.7 | 6.0 | - 16.0 | |
| - 16 лет | 1.7 - | 4.1 | 7.5 | - 18.1 |
Функции половых желез.Между 5 и 7 месяцами внутриутробного развития андрогены оказывают решающее влияние на реализацию генетически запрограммированного пола плода: при наличии андро-генов гипоталамус дифференцируется по мужскому типу; при их
161
отсутствии — по женскому типу. Андрогены способствуют росту и развитию мужских половых органов.
Андрогены и гонадотропные гормоны стимулируют созревание сперматогенного эпителия и процесс сперматогенеза. Если фоллику-лостимулирующий гормон активирует сперматогенез, то лютеинизи-рующий гормон — продукцию андрогенов. Зрелые сперматозоиды появляются в 10-15 лет, их представительство становится доминирующим в 16-18 лет, когда концентрация тестостерона выходит на взрослый уровень.
Андрогены, действуя по анаболическому типу, способствуют увеличению массы мышц, содержанию в костях протеина, а также обеспечивают подростковый спурт длины тела и продолжающееся ее увеличение у юношей. Однако, влияние андрогенов на рост скелета неоднозначно. Скорость роста зависит от исходных величин длины тела, концентрации андрогенов и их взаимодействия с другими половыми гормонам. После первоначального ускоряющего влияния андрогенов, в зрелом возрасте (в среднем после 21 года) они вызывают торможение роста скелета.
Андрогены стимулируют эритропоэз, а эстрогены подавляют его. Под контролем андрогенов активизируется рост гортани мальчиков, и в связи с удлинением голосовых связок, голос становится ниже. Мужской тип оволосения также формируется под влиянием андрогенов: в волосяных фолликулах происходит превращение тестостерона в дегидротестостерон — андроген, который, помимо всего прочего, вызывает оволосение лица по мужскому типу и рост предстательной железы.
Развитие яичников и половых органов у плодов, развивающихся по женскому типу, происходит под воздействием гонадотропинов матери, эстрогенов плаценты и надпочечников. Эстрогены вызывают ускоренное развитие скелета в плодовом периоде, когда девочки могут опережать по длине тела мальчиков.
Под влиянием ФСГ гипофиза в препубертатном периоде происходит постепенное созревание фолликулов яичников. В раннем пубертате, однако, ни один фолликул не созревает до овуляции — все они подвергаются атрезии (рассасыванию эпителия фолликула и его рубцеванию). У девочек, как и у мальчиков, пульсирующая секреция рилизинг-фактора лютеинизирущего гормона появляется в начале пубертатного периода только по ночам. Когда же рилизинг-фактор выделяется и днем (примерно в 14- 15 лет), начинает типичная для зрелых женщин секреция фолликулостимулирующего и лютеинизи-рующего гормонов, устанавливается двухфазный менструальный цикл, закачивающийся овуляцией и образованием желтого тела. В фазу созревания доминантного фолликула вплоть до овуляции преобладает активность эстрогенов, а в фазу желтого тела — прогестерона.
Женские половые гормоны способствуют росту матки, влагалища, малых половых губ, молочных желез и установлению характерного для женщин телосложения.
Отмечены положительные корреляции между уровнем полового созревания и электрической активностью мозга, — на ЭЭГ нарас-
162


 тает активность а2-волн и снижается активность 0- ритма. Эти изменения наиболее выражены у девочек. Прирост циркулирующих половых гормонов, особенно эстрогенов (наряду с тиреоидными гормонам), ускоряет у подростков миелинизацию волокон мозолистого тела, влияет на созревание трансколозальных связей, что улучшает взаимодействие левого и правого полушарий мозга. Недостаточная выработка половых гормонов подростков ослабляет диффе-ренцировку клеток в гипоталамусе и всей центральной нервной системе.
тает активность а2-волн и снижается активность 0- ритма. Эти изменения наиболее выражены у девочек. Прирост циркулирующих половых гормонов, особенно эстрогенов (наряду с тиреоидными гормонам), ускоряет у подростков миелинизацию волокон мозолистого тела, влияет на созревание трансколозальных связей, что улучшает взаимодействие левого и правого полушарий мозга. Недостаточная выработка половых гормонов подростков ослабляет диффе-ренцировку клеток в гипоталамусе и всей центральной нервной системе.
Предопределяющие половое созревание гормональные сдвиги в организме мальчиков и девочек инициируются гипоталамусом (рис. 18.1). В детстве, из-за высокой чувствительности гипоталамуса к половым гормонам, их небольшое количество по механизму отрицательной обратной связи способно подавить выработку рили-зинг-гормонов и, соответственно — гонадотропных гормонов. В пубертатном периоде гипоталамус становится менее чувствительным к половым гормонам, для его стимуляции необходима их более высокая концентрация. Усиливается выработка как рилизинг-гормонов, так и гонадотропных гормонов, отмечается рост гонад, повышается уровень эстрогенов, андрогенов и прогестерона. У взрослых людей чувствительность гипоталамуса к половым гормонам становится еще ниже. Таким образом, половое созревание обусловлено ступенчатым созреванием — сначала гипоталамуса, затем — гипофиза и, наконец, половых желез.
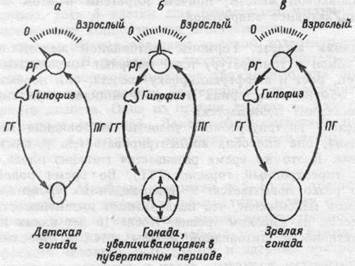
Рис. 18.1.Регуляция половых стероидных гормонов в разные возрастные периоды.
Вверху на шкапах показано увеличение пороговой концентрации стероидных гормонов: а — в детстве, б — в пубертатном периоде, в — у взрослого человека. РГ — рилизинг-гормоны, ГГ — гонадотропные гормоны, ПГ — половые гормоны.
 163
163




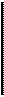 Секреторная функция половых желез стимулируется адекватными для детей и подростков умеренными физическими нагрузками. Интенсивные нагрузки в пубертатном периоде могут привести к усилению андрогенной функции как у мальчиков, так и у девочек. В результате у девочек-подростков появляются признаки маскулинизации. Вместе с тем чрезмерные нагрузки приводят к угнетению продукции половых гормонов и задержке полового созревания.
Секреторная функция половых желез стимулируется адекватными для детей и подростков умеренными физическими нагрузками. Интенсивные нагрузки в пубертатном периоде могут привести к усилению андрогенной функции как у мальчиков, так и у девочек. В результате у девочек-подростков появляются признаки маскулинизации. Вместе с тем чрезмерные нагрузки приводят к угнетению продукции половых гормонов и задержке полового созревания.
Вилочковая железа (тимус).Гормоны, вырабатываемые вилочко-вой железой (главный из них, тимозин), имеют большое значение как для дифференцировки Т-клеток, так и для пролиферации и созревания клеток самой железы. Установлено, что уже у 7,5-недельного эмбриона проявляются различные функции Т-клеток, а к 12 неделе внутриутробного развития железа напоминает зрелый орган и вскоре становится центральным органом иммуногенеза. Т-клетки действуют, главным образом, на кислотоустойчивые бактерии, вирусы кори, ветряной оспы и грибы. Хелперные Т-клетки необходимы для инициации ответа на антиген; супрессорные Т-клетки играют гомеостатическую роль, удерживая иммунный ответ в необходимых пределах.
У детей активность железы проявляется в полной мере, поскольку ребенку приходится сталкиваться с огромным количеством новых для него антигенов. До периода половой зрелости повышенная активность тимуса обусловлена действием тироксина. Андрогенные и эстрогенные гормоны вызывают быструю и резко выраженную атрофию вилочковой железы, причем эстрогены в этом отношении значительно активнее андрогенов.
Щитовидная железа.Гормоны щитовидной железы повышают основной обмен и температуру тела, ускоряют миелинизацию нервных волокон, рост и дифференцировку скелета; они необходимы для ускорения обмена холестерина и других липидов (при гипотиреозе уровень последних повышается).
К 12 неделе внутриутробного развития щитовидная железа уже сформирована, она способна концентрировать йод и синтезировать йодтирозины. В это же время развивается гипофиз плода, вырабатывающий тиреотропный гормон (ТТГ). Во время родов выброс последнего резко повышается. У новорожденных уровень тиреоид-ных гормонов максимален, что поддерживает интенсивность обменных процессов на высоком уровне. После 10 лет каких-либо различий в активности щитовидной железы детей и взрослых не отмечается.
В период полового созревания в связи с выраженной васкуляри-зацией щитовидной железы имеет место значительное увеличение ее объема, особенно у девочек. При этом возникает состояние гипер-тиреоза, сопровождающееся усилением энергетических процессов, повышенной возбудимостью, увеличением частоты сердцебиений. В этот период особенно проявляется стимулирующее влияние на щитовидную железу эстрогенов и тормозящее — прогестерона.
164


 Околощитовидные железы.У новорожденных в первые 2 дня жизни происходит снижение уровня кальция в плазме. Околощитовидные железы плода до рождения проявляют минимальную активность. Гомеостаз кальция обеспечивается гиперфункцией околощитовидных желез матери, высвобождением кальция из костей у матери и усилением его реабсорбиии почечными канальцами. (На гомеостаз кальция влияют также гормон роста, тироксин, кальцито-нин, кортизол). Избыток ионов кальция транспортируется через плаценту от матери к плоду. Когда же после рождения переход кальция от матери к плоду прекращается, возникает состояние ги-покальциемии новорожденного. Снижение содержания ионов кальция во внеклеточной жидкости ведет к резкому усилению возбудимости нервно-мышечной системы и тетании, что иногда отмечается у новорожденных.
Околощитовидные железы.У новорожденных в первые 2 дня жизни происходит снижение уровня кальция в плазме. Околощитовидные железы плода до рождения проявляют минимальную активность. Гомеостаз кальция обеспечивается гиперфункцией околощитовидных желез матери, высвобождением кальция из костей у матери и усилением его реабсорбиии почечными канальцами. (На гомеостаз кальция влияют также гормон роста, тироксин, кальцито-нин, кортизол). Избыток ионов кальция транспортируется через плаценту от матери к плоду. Когда же после рождения переход кальция от матери к плоду прекращается, возникает состояние ги-покальциемии новорожденного. Снижение содержания ионов кальция во внеклеточной жидкости ведет к резкому усилению возбудимости нервно-мышечной системы и тетании, что иногда отмечается у новорожденных.
На обмен кальция в организме детей значительное влияние оказывает также витамин Д, который вместе с паратгормоном усиливает всасывание кальция из кишечника.
Поджелудочная железа.У плода В-клетки, продуцирующие инсулин, появляются раньше, чем а-клетки, продуцирующие глюкоген. В этот период отногенеза оба гормона не связаны с регуляцией глюкозы. В отличие от взрослого организма инсулин плода в большей мере влияет на повышение транспорта аминокислот через клеточные мембраны. Повышенная концентрация аминокислот в крови вызывает быстрое увеличение секреции инсулина. В течение первых недель постнатальной жизни развивается инсулиновый ответ на гипергликемию, хотя В- клетки еще продолжают частично реагировать на повышение концентрации аминокислот.
Дети и юноши обычно обладают высокой толерантностью к сахарным нагрузкам. В последние десятилетия значительно возросло число детей и подростков, имеющих врожденную или приобретенную недостаточность островков Лангерганса, что приводит к развитию сахарного диабета. Одна из причин диабета — избыточное потребление детьми сладостей. Длительное избыточное потребление сахара истощает В- клетки и приводит к уменьшению продукции инсулина.
Система крови.Мембрана плаценты в 5-10 раз толще мембраны альвеолы легких, что затрудняет обмен газов между плодом и матерью. Кроме того, в начальные этапы внутриутробного развития содержание эритроцитов и гемоглобина у плода намного меньше, чем у взрослого человека, встречаются и ядерные эритроциты. Однако, в процессе развития у плода создаются механизмы, препятствующие возникновению чрезмерной гипоксии: при уменьшении объема каждого эритроцита содержание гемоглобина в нем, как и число эритроцитов, значительно увеличиваются и превышают таковые у взрослого человека (рис. 18.2); гипоксия оказывает стимулирующее действие на образование эритропоэтинов; оксигемоглобин плода имеет более высокую степень диссоциации, чем оксигемогло-
165
 | |
 |
|
Рис.18.2. Концентрация гемоглобина (точечная линия), число эритроцитов (сплошная линия) и средний объем эритроцита (пунктирная линия) у плода на разных стадиях беременности.




 бин взрослого человека; увеличивается масса циркулирующей крови; возрастает уровень гепарина, обладающего, помимо прочего, анти-гипоксическим действием.
бин взрослого человека; увеличивается масса циркулирующей крови; возрастает уровень гепарина, обладающего, помимо прочего, анти-гипоксическим действием.
При рождении до 35% крови ребенка находится в плаценте. Если при рождении плаценту держат над ребенком, к нему переливается много плацентарной крови, в результате чего концентрация гемоглобина и число эритроцитов увеличивается.
|
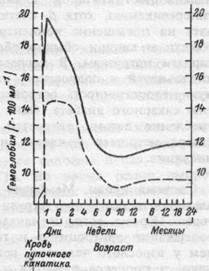
| Рис.18.3. Концентрация гемоглобина (НЬ) у ребенка в первые два года жизни. Сплошная линия — средний уровень, пунктирная — нижний предел нормы. |
Первый этап новорожденности характеризуется большой кислородной емкостью крови (на 10-15% большем, чем у взрослого человека). Со 2-3 дня жизни количество эритроцитов в единице объема крови начинает снижаться. Это происходит в результате гипероксии, которая проявляется у ребенка после рождения. Кровь с относительно повышенным содержанием кислорода, протекая через почки, перестает оказывать стимулирующее влияние на их эритропо-этическую ткань, и, соответственно, концентрация эритроцитов и гемоглобина уменьшается (рис. 18.3). Наиболее низкий уровень эритроцитов наблюдается у ребенка в возрасте 2- 3 месяцев. Затем число эритроцитов и количество гемоглобина увеличивается, причем у мальчи-
166

 ков этот процесс продолжается и в подростковом возрасте, а у девочек-подростков прирост эритроцитов и гемоглобина прекращается. Увеличение числа эритроцитов у мальчиков связывают с секрецией тестостерона. С ним соотносят и высокую активность карбоангидразы, которая способствует транспорту газов между кровью и тканью. Некоторое снижение кроветворения у девочек обусловлено тормозным влиянием эстрогенов. В пубертатном возрасте отношение общего гемоглобина к массе тела у мальчиков выше, чем у девочек.
ков этот процесс продолжается и в подростковом возрасте, а у девочек-подростков прирост эритроцитов и гемоглобина прекращается. Увеличение числа эритроцитов у мальчиков связывают с секрецией тестостерона. С ним соотносят и высокую активность карбоангидразы, которая способствует транспорту газов между кровью и тканью. Некоторое снижение кроветворения у девочек обусловлено тормозным влиянием эстрогенов. В пубертатном возрасте отношение общего гемоглобина к массе тела у мальчиков выше, чем у девочек.
В целом, число эритроцитов тесно коррелирует с уровнем полового созревания, скоростью роста ребенка и интенсивностью метаболизма. Транспорт кислорода кровью с возрастом становится все более эффективным, его утилизация улучшается. Способность крови к переносу кислорода в наибольшей степени выражена в пубертатном периоде. К моменту полового созревания кроветворение протекает, как и у взрослых, в костном мозге грудины, ребер, тел позвонков, костей черепа и таза.
Кривые диссоциации оксигемоглобина у детей и взрослых отличаются: у первых, в основном, отмечается меньшая насыщаемость крови кислородом и низкая величина рН плазмы. Происходящие с возрастом изменения в содержании эритроцитов и гемоглобина направлены на обеспечение возросшего потребления кислорода на единицу массы тела, особенно у мальчиков (девочки с той же мышечной массой потребляют меньше кислорода). Объем крови, начиная с детского возраста, и, особенно, в подростковом возрасте, также больше у мальчиков.
Лейкоциты появляются в конце 3-го месяца внутриутробного развития, а на последней неделе беременности их концентрация у плода превышает таковую у взрослого человека. Она становится еще выше, достигая своего максимума в первый же день после рождения (физиологический лейкоцитоз). Это результат быстрой мобилизации нейтрофилов из запасных пулов костного мозга ребенка в ответ на стресс при рождении. В этих условиях среди поступающих в систему циркуляции лейкоцитов многие оказываются незрелыми. На фоне физиологического лейкоцитоза отмечается перераспределение содержания нейтрофилов и лимфоцитов. Число нейтрофилов прогрессивно уменьшается, а лимфоцитов — увеличивается. В возрасте 5-6 дней имеет место так называемый первый перекрест относительного содержания нейтрофилов и лимфоцитов в периферической крови. Состояние лейкоцитоза могут вызывать и внешние антигенные стимулы, с которыми сталкивается новорожденный (реактивный лейкоцитоз).
С возрастом общее число лейкоцитов прогрессивно снижается и достигает взрослого уровня в 16 годам.
В процессе возрастного развития через несколько критических этапов проходит иммунная система. Первый этап наблюдается сразу после рождения, когда организм внезапно встречается с огромным количеством антигенов. В это время велика роль супрессорных Т- клеток, которые предупреждают развитие гипериммунных реакций; активность Т-киллеров, т.е. клеток, способствующих уничто-
167


 жению микроорганизмов, низкая; ограничен синтез у-интерферона; хемотаксис и фагоцитоз ослаблены. В крови много Т-лимфоцитов, однако имеются признаки функциональной незрелости Т- и В-лимфоцитов. В этот период гуморальный иммунитет обеспечивается почти полностью материнскими антителами. Вместе с тем, сопротивляемость организма по отношению к различным микробам и вирусам низкая.
жению микроорганизмов, низкая; ограничен синтез у-интерферона; хемотаксис и фагоцитоз ослаблены. В крови много Т-лимфоцитов, однако имеются признаки функциональной незрелости Т- и В-лимфоцитов. В этот период гуморальный иммунитет обеспечивается почти полностью материнскими антителами. Вместе с тем, сопротивляемость организма по отношению к различным микробам и вирусам низкая.
Через 3-6 месяцев развивается второй критический период становления иммунной системы. Обусловленный передачей антител с молоком матери, пассивный гуморальный иммунитет ослабляется в связи с катаболизмом материнского гамма-глобулина. И хотя концентрация лимфоцитов в это время достигает своего максимума, лимфоциты еще незрелы. Большинство антигенов вызывает первичный иммунный ответ, не оставляющий иммунологической памяти.
Когда ребенок начинает ходить, возрастают его контакты с внешним миром и увеличиваются антигенные нагрузки (третий критический период приходится на конец первого и второй год жизни). Однако, синтез некоторых антител субкласса g2 — g4 ограничен, в результате чего полисахаридные антигены, например, пневмококка вообще не индуцируют гуморального иммунитета. И все же иммунная система по ряду показателей становится более зрелой. Так, дети старше двух лет имеют то же процентное содержание Т-лимфоцитов, что и взрослые.
Примерно в 5 лет происходит так называемый второй перекрест в содержании нейтрофилов и лимфоцитов (количество первых повышается, а вторых — снижается). В это время развивается четвертый критический период созревания иммунной системы.
Следующий критический период связан с пубертатным скачком роста, который сопровождается относительным уменьшением массы лимфоидных органов. И хотя половые гормоны стимулируют гуморальное звено иммунитета, они подавляют клеточное звено. Вредные привычки, стресс могут в еще большей степени ослабить иммунную систему подростков. Химические загрязнители биосферы вызывают в раннем отногенезе нарушение развития Т-лимфоцитов и вилочковой железы.
В процессе возрастного развития количество кровяных пластинок, постепенно увеличиваясь, выходит на взрослый уровень к подростковому возрасту.
Скорость оседания эритроцитов от детского к подростковому возрасту замедляется, особенно у мальчиков, а способность эритроцитов к агглютинации повышается. Однако, активность агглютининов и агглютиногенов увеличивается с разной скоростью. Так, максимальная активность агглютиногена А достигается в 3 года, а агглютинина а — к 7 и даже 10 годам; именно с этого возраста ярко проявляются реакции несовместимости крови при ее переливании. Прогрессивно нарастает также активность ферментов плазмы. Это относится к липазе, амилазе, холинэстеразе, карбоангидразе. Еще в грудном возрасте содержание глобулинов уменьшается, а альбуми-
168

 нов — нарастает. Вместе с тем, ряд компонентов минерального состава плазмы (Na+, K+, Ca++, Mg++) остается относительно стабильным.
нов — нарастает. Вместе с тем, ряд компонентов минерального состава плазмы (Na+, K+, Ca++, Mg++) остается относительно стабильным.
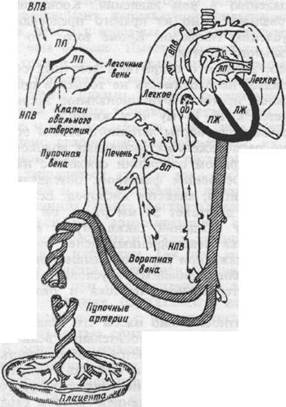
Система кровообращения.Кровообращение плода имеет несколько особенностей. Одна из них состоит в том, что функцию легкого выполняет плацента. Оксигенированная кровь поступает из плаценты в организм плода по пупочной вене. Примерно 50% крови проходит через печень, а оттуда по характерному для плода венозному протоку попадает в нижнюю полую вену. Остальная кровь пупочной вены (с большим насыщением кислорода) поступает непосредственно в нижнюю полую вену (рис. 18.4). Из последней разделенная crista dividens часть крови через присущее плоду овальное окно направляется в левое предсердие. Кровь из верхней полой вены попадает в правое предсердие, правый желудочек и легочный ствол. У плода в отсутствие дыхания легочные артериолы создают большое сопротивление кровотоку. В результате кровь из легочного ствола поступает через широкий артериальный (боталлов) проток в аорту, где в этот период кровяное давление ниже, чем в легочном стволе.

 Рис.18.4. Схема
Рис.18.4. Схема
 кровообращения плода.
кровообращения плода.
Верхний конец нижней попой вены сообщается непосредственно с левым предсердием через овальное отверстие (см.вставку) и с правым предсердием. ПП и ПЖ — правые предсердие и желудочек; ЛП и ЛЖ — левые предсердие и желудочек; ВПВ — верхняя полая вена: НПВ — нижняя полая вена; АП — артериальный проток; ВП — венозный проток; ОО — овальное отверстие.
 169
169



 Эффективный сердечный выброс плода представляет собой сумму левожелудочкового выброса и минутного объема крови, протекающего через артериальный проток, и достигает 220 мл/(кг.мин). Около 65% этой крови возвращается к плаценте, а остальные 35% крови перфузируют органы и ткани новорожденного.
Эффективный сердечный выброс плода представляет собой сумму левожелудочкового выброса и минутного объема крови, протекающего через артериальный проток, и достигает 220 мл/(кг.мин). Около 65% этой крови возвращается к плаценте, а остальные 35% крови перфузируют органы и ткани новорожденного.
Что касается особенности регуляции кровообращения плода, то для первой половины беременности характерно доминирование гуморальных, а не нейрональных адренергических механизмов. По мере созревания плода нарастает и симпатическая, и парасимпатическая регуляция. Например, атропин, введенный женщине на разных этапах беременности, вследствие блокады им холинергических волокон способствует прогрессивному нарастанию сердечного ритма у плода. Это значит, что в процессе созревания холлинергическая регуляция сердца усиливается.
С момента первого вдоха сопротивление в сосудах легких снижается в 7 раз и приток крови к левому предсердию улучшается. В результате повышается давление в левом предсердии и переход крови через овальное отверстие затруднен. Функциональное закрытие овального окна происходит обычно к 3- месячному возрасту, однако у 25% взрослых при катетеризации сердца зонд можно провести через закрывающие его ткани. В ответ на гипоксию новорожденного сосуды легких суживаются, что приводит к снижению притока крови к левому предсердию и падению в нем давления. Кровь вновь начинает переходит через овальное окно из правого предсердия в левое, что приводит к углублению гипоксии. Кроме того, это вызывает незаращение артериального протока.
В норме у новорожденного, в связи с открытием легочных сосудов и началом дыхания, отпадает необходимость не только в овальном окне, но и в артериальном протоке. Функциональное закрытие последнего обычно завершается к 10- 15-му часу жизни.
Артериальный проток отличается от аорты легочного ствола большим количеством циркулярно расположенных мышечных волокон. У плода поддержание протока в открытом состоянии связано с наличием в крови простагландинов. Основным фактором, обуславливающим его закрытие у новорожденного, является кислород. Если РО2 крови, проходящей через проток, достигает 50 мм рт.ст., он суживается. Возраст плода к моменту рождения также играет важную роль: стенки артериального протока недоношенных менее чувствительны к воздействию кислорода даже при развитом мышечном слое. Следовательно, у недоношенных или родившихся в условиях гипоксии детей риск незаращения артериального протока и овального кона возрастает.
Масса сердца новорожденного относительно массы его тела почти вдвое больше, чем у взрослого человека. Относительная величина МОК имеет ту же закономерность, что объясняется необходимостью компенсировать высокий энергетический обмен ребенка, будущую частоту дыхания и сердечных сокращений. Снижение с возрастом относительной величины МОК обусловлено урежением частоты сердцебиений, повышением общего периферического сопротивления со-
170


 судов в большом круге кровообращения и снижением центрального венозного давления.
судов в большом круге кровообращения и снижением центрального венозного давления.
На функциональном состоянии системы кровообращения новорожденных сказываются и особенности его телосложения. Относительные размеры головы (по отношению к размерам туловища) в 4 раза превышают таковые у взрослого человека, а относительная длина нижних конечностей вдвое меньше, чем у взрослых. Это приводит к тому, что доля МОК в сосудах системы нисходящей аорты у новорожденных равна 40%, в то время, как у взрослых — 75%. Вследствие этого констрикция сосудов системы нисходящей аорты у новорожденного не вызывает столь выраженной прессорной реакции, как у взрослого человека.
Реакция сердечно-сосудистой системы новорожденного на орто-статическую пробу (быстрое изменение положения тела с горизонтального на вертикальное) отличается от реакции взрослого человека. Если у взрослого переход в вертикальное положение сопровождается скоплением крови в нижних конечностях и некоторым уменьшением венозного возврата, то у новорожденного венозный возврат может даже повыситься, т.к. короткие нижние конечности не позволяют центробежным силам, действующим в направлении голова-ноги, существенно снизить центральное венозное давление, а отток крови от головы относительно больших размеров вызывает даже повышение этого давления и венозного возврата.
Коэффициент капиллярной фильтрации у новорожденных вдвое выше, чем и у взрослых. У недоношенных новорожденных он может быть еше больше. Имеется несколько причин высокой капиллярной фильтрации у новорожденных: дилатация артериол, высокая плотность капилляров, высокое венозное давление, относительно большой объем плазмы, низкое содержание в ней протеина, а также высокий уровень тканевого метаболизма. Центральное венозное давление у новорожденного выше, чем у взрослого человека, что обусловлено слабой растяжимостью вен, их узким просветом, большим объемом плазмы, высокой частотой сердцебиений (сердце не успевает заполняться кровью так, как при более редкой частоте сердцебиений и, соответственно, продолжительной диастоле).
На ранних этапах постнатального онтогенеза сердце продолжает оставаться под доминирующим влиянием симпатических нервов. Однако, парасимпатические влияния в процессе развития ребенка постепенно нарастают. Так, при введении атропина новорожденному ребенку частота сердцебиений повышается на 15%, в то время, как у взрослых при соответствующих дозировках она возрастает на 80%. Слабые влияния блуждающего нерва на сердце новорожденного связаны не только с незрелостью центральной регуляции, но и с нестабильностью синтеза ацетилхолина в пресинаптических бляшках.
В основе отмечающихся с возрастом урежений ЧСС лежит усиление влияний парасимпатических волокон, стимуляция механоре-цепторов сосудов нарастающим уровнем АД, повышающейся активностью скелетной мускулатуры, приводящей к усилению влияний блуждающего нерва. Так, частота сердцебиений ребенка 7- 8 месяцев
171


 составляет около 120 уд/мин вместо 140- 150 уд/мин у новорожденного, что объясняется формированием в данный период позы сидения. Влияние блуждающего нерва на сердце еще более выражено вследствие реализации позы стояния в 9-12 месяцев.
составляет около 120 уд/мин вместо 140- 150 уд/мин у новорожденного, что объясняется формированием в данный период позы сидения. Влияние блуждающего нерва на сердце еще более выражено вследствие реализации позы стояния в 9-12 месяцев.
В процессе возрастного развития увеличивается толщина стенки крупных эластических артерий, утолщаются стенки сосудов мышечного типа. В результате, повышается жесткость сосудов и увеличивается скорость распространения пульсовой волны.
У новорожденных детей ренинангиотензивная система является более важным механизмом регуляции АД, чем барорецепторный рефлекс. Относительно роли хеморецепторов сосудов существует две точки зрения: более распространенная состоит в том, что они в неонатальном периоде имеют такую же возбудимость, как и у взрослого человека; другая заключается в том, что хеморецепторы, чувствительные к напряжению углекислоты в крови, созревают постепенно.
Возрастающая констрикция артериол лежит в основе характерной тенденции онтогенетического развития — постепенного повышения артериального давления от рождения до юношеского возраста. Детерминантами АД в возрастном аспекте являются также особенности генотипа, феномен акцелерации, уровень полового созревания. Наиболее значимыми детерминантами АД у детей и подростков являются длина и масса тела. При одном и том же календарном возрасте артериальное давление будет выше у индивидуумов с большей длиной и массой тела. Норма АД в эти периоды онтогенеза сугубо индивидуальна и часто не совпадает с общепринятыми нормативами.
Имеющееся у детей низкое сопротивление сосудов кровотоку, слабо выраженные реакции их тонуса на внешние стимулы не способствует поддержанию гомеостаза. В частности, даже при небольшом охлаждении теплоотдача резко возрастает в связи с тем, что кожные сосуды остаются дилатированными. Быстрое совершенствование сосудодвигательных реакций на внешние стимулы начинается с 6-летнего возраста. Их развитие можно ускорить закаливающими процедурами. Сосудодвигательные реакции из неэкономичных генерализованных в этом возрасте становятся более локальными; в раннем же возрасте активность определенной группы мышц начинает вовлекать в рабочую гиперемию и сосуды многих неработающих мышц.
С 7-8 лет у детей отмечается предстартовая реакция системы кровообращения: еще до начала мышечной работы учащаются сердцебиения и повышается артериальное давление. Это свидетельствует о появлении в системе кровообращения условно- рефлекторных реакций, которые в процессе дальнейшего онтогенетического развития становятся более выраженными. Вместе с тем, организм ребенка даже в условиях систематической физической тренировки не приобретает той экономизации функций сердечно-сосудистой системы, которая характерна для взрослых.
Выраженные изменения кровообращения происходят в подростковом периоде, являющимся одним из критических этапов развития.
172



 Масса сердца и размеры его камер увеличиваются быстрее, чем диаметр кровеносных сосудов. Просвет сосудов относительно размеров сердца в этом возрасте невелик еще и потому, что в результате скачкообразного увеличения длины тела сосуды вытягиваются. Рост миокарда у подростков опережает рост клапанов, что приводит к транзиторной недостаточности клапанов. Ее усиливает асинхронность работы сосочковых мышц миокарда. Указанные особенности развития сердца и сосудов у подростков сказываются на характере потока крови и способствуют появлению функциональных шумов сердца. В связи с феноменом акцелерации у многих подростков темпы развития сердца отстают от характеристик физического развития (длина и масса тела, окружность грудной клетки). При этом, несмотря на высокие показатели физического развития, адаптивные реакции сердечно-сосудистой системы могут быть неадекватны мощности физической нагрузки.
Масса сердца и размеры его камер увеличиваются быстрее, чем диаметр кровеносных сосудов. Просвет сосудов относительно размеров сердца в этом возрасте невелик еще и потому, что в результате скачкообразного увеличения длины тела сосуды вытягиваются. Рост миокарда у подростков опережает рост клапанов, что приводит к транзиторной недостаточности клапанов. Ее усиливает асинхронность работы сосочковых мышц миокарда. Указанные особенности развития сердца и сосудов у подростков сказываются на характере потока крови и способствуют появлению функциональных шумов сердца. В связи с феноменом акцелерации у многих подростков темпы развития сердца отстают от характеристик физического развития (длина и масса тела, окружность грудной клетки). При этом, несмотря на высокие показатели физического развития, адаптивные реакции сердечно-сосудистой системы могут быть неадекватны мощности физической нагрузки.
В пубертатный период усиливается андренергическая регуляция системы кровообращения. Важную роль в регуляции сердца и сосудов осуществляет также и эндокринная система. Например, правильному развитию сердца способствуют гонадотропная функция гипофиза и уровень половых гормонов в крови (гипофизэктомия у экспериментальных животных приводит к уменьшению массы сердца по отношению к массе тела). В подростковом периоде усиливаются половые различия сердечно-сосудистой системы — миокарду мальчиков-подростков свойственны большие функциональные возможности, чем у девочек. У девочек в связи с менструальным циклом происходит предменструальный подъем систолического АД и снижение частоты сердцебиений. Величина АД у девочек выходит на взрослый уровень раньше, чем у мальчиков (примерно через 3,5 года после появления первых менструаций).
В период подросткового спурта длины тела может наблюдаться преходящее увеличение частоты сердцебиений. Ее взрослый уровень устанавливается в конце подросткового периода; у девушек частота сердцебиений на 10% выше, чем у юношей. Более медленный темп сердечных сокращений у последних связывают с большими размерами сердца и большей силой сердечных сокращений, а также более выраженной парасимпатической регуляцией сердца.
Адаптивные перестройки сердечно-сосудистой системы, связанные с мышечной нагрузкой, совершенствуются у подростков преимущественно за счет прироста частоты сердцебиений, ударный объем крови меняется при этом незначительно.
Несмотря на то, что к юношескому возрасту повышается роль мышечного насоса и удлиняются фазы сердечного цикла, особенно диастолы, и тем самым создаются благоприятные условия для заполнения сердца кровью и реализации механизма Старлинга, относительная величина МОК снижается. Ее уменьшение обусловлено урежением частоты сердцебиений, повышением общего периферического сопротивления артериальных сосудов (из-за разрастания мышечного слоя в артериолах и запаздывания по отношению к размерам сердца увеличения диаметра артериальных сосудов), умень-
173

 шением относительного количества циркулирующей крови и относительной массы сердца. В целом, величина прироста МОК не поспевает за приростом массы тела.
шением относительного количества циркулирующей крови и относительной массы сердца. В целом, величина прироста МОК не поспевает за приростом массы тела.
Развитие внешнего дыхания.Основным органом внешнего дыхания плода является плацента. Через нее плод получает кислород из крови матери, а ей отдает углекислоту. С 11 недели у плода начинаются сокращения диафрагмы межреберных мышц; их частота увеличивается при гипоксии, гиперкапнии и ацидозе. Эти движения ускоряют развитие легких; они также активизируют кровообращение, усиливая приток крови к сердцу.
Первый полноценный вдох происходит сразу после рождения. Его предпосылками являются следующие факторы. Во-первых, прохождение плода по родовым путям сопровождается резкой активизацией механорецепторов кожи, афферентные импульсы от которых поступают в ретикулярную формацию. Источниками афферентных импульсов являются также проприо- и вестибулорецепторы. К этому добавляется импульсация со стороны терморецепторов кожи, улавливающих перепад температур при рождении, а также от органов слуха и зрения. Когда этого оказывается недостаточно для включения полноценного глубокого дыхания, сенсорный поток усиливают искусственно: новорожденного на несколько секунд опускают в ванночку с теплой водой, пошлепывают.
Во-вторых, первому вдоху способствует устранение причины торможения дыхательного центра ребенка. Задержку дыхания может вызвать "рефлекс ныряльщика", обусловленный раздражением амни-отической жидкостью рецепторов полости носа (область крыльев носа). Для исключения этих тормозных влияний тотчас после рождения ребенка удаляется слизь с его личика, обеспечивается отток жидкости из полости носа.
Ведущим механизмом первого вдоха является "химический". Отслоение плаценты во время родов и перевязка пуповины приводят к уменьшению в крови новорожденного содержания кислорода и накоплению углекислоты. От начала родов к их концу насыщение крови плода кислородом снижается с 20 до 17 мм.рт.ст., а содержание СО2 повышается с 44 до 51 мм рт.ст. Хеморецепторы дуги аорты, бифуркации сонной артерии и легочного ствола, с которых усиливается афферентация к дыхательному центру, еще не созрели в полной мере; чувствительность центральных хеморецепторов к гипоксии, гиперкании и ацидозу в этот период невелика. Вместе с тем, указанного механизма оказывается достаточно для возникновения первого вдоха.
У плода грудная клетка растет быстро, а легкие — медленно, в результате давление в плевральной полости постепенно снижается, и к моменту родов возможен значительный градиент давления между атмосферным воздухом и плевральной полостью.
Помимо описанного "рефлекса ныряльщика", для реализации первого вдоха существуют и другие препятствия. Одно из них — наличие амниотической жидкости в легких и воздухоносных путях,
174




 вязкость которой в 36 раз выше, чем воздуха. Большая часть жидкости после рождения ребенка переходит в начинающие открываться капилляры легких, другая часть жидкость через рот выходит наружу во время рождения, третья — заглатывается и даже выполняет определенную пищеварительную функцию. Всасывание жидкости в легкие происходит в течение нескольких часов и обусловлено более высоким онкотическим давлением крови. Часть амниотической жидкости всасывается в лимфатические сосуды легких.
вязкость которой в 36 раз выше, чем воздуха. Большая часть жидкости после рождения ребенка переходит в начинающие открываться капилляры легких, другая часть жидкость через рот выходит наружу во время рождения, третья — заглатывается и даже выполняет определенную пищеварительную функцию. Всасывание жидкости в легкие происходит в течение нескольких часов и обусловлено более высоким онкотическим давлением крови. Часть амниотической жидкости всасывается в лимфатические сосуды легких.
Низкая растяжимость легких, равно как и низкая возбудимость дыхательного центра у новорожденного, также является препятствием для вдоха. Устойчивость новорожденного к асфиксии связана с преобладанием у него анаэробных процессов над аэробными. Мозг новорожденного характеризуется низким метаболизмом, его относительная устойчивость к гипоксии связана также с достаточными запасами гликогена для получения энергии анаэробным путем и более медленным, чем у взрослых, падением артериального давления в ответ на асфиксию. Итак, у новорожденного имеются факторы, направленные как на стимуляцию дыхания, так и на сдерживание его, однако обычно доминируют первые.
К концу внутриутробного периода развития альвеолы уже дифференцированы и легкие потенциально способны увеличивать свой объем на вдохе. Однако, недостаток или отсутствие сурфактанта приводит к слипанию альвеол, образованию нефизиологических ателектазов и даже неонатальной смерти ребенка.
У новорожденного реципрокная деятельность дыхательного центра осуществляется, главным образом, за сет рефлекса Геринга- Брейера (у взрослого человека его роль выражена меньше): дыхательный центр новорожденного имеет высокую чувствительность к импульсам, идущим от рецепторов растяжения легких (в частности, гладких мышц бронхиол). Недостаточную зрелость дыхательного центра и компенсирует повышенная активность рефлекса Геринга- Брейера. К нервному контролю дыхания присоединяются и эндокринные факторы: например, гормоны щитовидной железы повышают чувствительность дыхательного центра к приходящим стимулам.
С возрастом морфофункциональные показатели внешнего дыхания существенно изменяются (табл. 18.3): дыхательная поверхность легких резко возрастает, частота дыхания снижается, увеличивается дыхательный объем, относительные величины альвеолярной вентиляции и потребления кислорода уменьшаются. Частота дыхания устойчиво снижается к 18-20 годам, но в наибольшей степени — в первые два года. Абсолютная величина минутного объема дыхания (МОД) с возрастом увеличивается, однако МОД, отнесенный к массе тела или его поверхности, уменьшается, что обусловлено снижением интенсивности обмена веществ. Высокая интенсивность легочной вентиляции у детей компенсирует более низкую, чем у взрослых, утилизацию кислорода. Так, у детей младшего школьного возраста 1 л кислорода извлекается, в среднем, из 30 л вдыхаемого воздуха, а у взрослого человека — из 26 л. Облегчающаяся в процессе онтогенетического развития утилизация кислорода связана с уменьше-

 Таблица 18.3Сравнительная характеристика параметров дыхательной системы у новорожденного и взрослого человека
Таблица 18.3Сравнительная характеристика параметров дыхательной системы у новорожденного и взрослого человека
| Показатели | Единицы измерения | Новорожденные | Взрослые |
| Площадь поверхности тела | м2 | 0,21 | 1.9 |
| Масса тела | КГ | ||
| Вес легких | Г | ||
| Диаметр трахеи | мм | ||
| Диаметр бронхиолей | мм | 0,1 | 0,2 |
| Число разветвленных дыхательных путей | п-106 | 1,5 | |
| Диаметр альвеол | мкм | 50-100 | 200-300 |
| Число альвеол | п-106 | ||
| Площадь поверхности альвеол | м2 | ||
| Жизненная емкость легких | МЛ-КГ-1 | ||
| Остаточная емкость | мл- кг-1 | ||
| Мертвое пространство | мл-кг-1 | 2,2 | 2,2 |
| Дыхательный объем | мл-кг-1 | ||
| Частота дыхания в покое | дых-мин-1 | ||
| Альвеолярная вентиляция | мл-кг-1 • мин' | 100-150 | |
| Потребление Ог в покое | мл-кг-1 -мин'1 | ||
| Относительный МОД | л-мин-1 -кг-1 |
 нием в более старших возрастных группах относительного количества плазмы крови и межтканевой жидкости, которые являются препятствием для газообмена. Для детей характерна слабая растяжимость легких: у новорожденных она в 40 раз меньше, чем у взрослых людей. Поэтому дыхательные мышцы — главным образом, ин-спираторные — затрачивают на вентиляцию легких много энергии. Достижение дефинитивного (зрелого) уровня развития респираторной системы происходит к 16-17 годам.
нием в более старших возрастных группах относительного количества плазмы крови и межтканевой жидкости, которые являются препятствием для газообмена. Для детей характерна слабая растяжимость легких: у новорожденных она в 40 раз меньше, чем у взрослых людей. Поэтому дыхательные мышцы — главным образом, ин-спираторные — затрачивают на вентиляцию легких много энергии. Достижение дефинитивного (зрелого) уровня развития респираторной системы происходит к 16-17 годам.
Пищеварение.Глюкоза, аминокислоты и жирные кислоты легко проникают в организм плода через плаценту. Большое количество глюкозы депонируется в виде гликогена в печени и скелетных мышцах. К моменту рождения печень плода содержит в 2- 3 раза больше гликогена, чем печень взрослого человека. 90% накопленного гликогена расходуется на энергетическое обеспечение в первые 2-3 часа после рождения, когда прекращается плацентарное кровоснабжение. Недоношенные дети имеют недостаточные запасы глюкозы.
Концентрация глюкозы в крови ребенка тотчас после рождения выше, чем у плода. Это связано с повышенной активностью нервной системы и высокой концентрацией циркулирующих катехолами-нов, вызывающих гликогенолиз. В связи с тем, что запасы глюкозы исчерпываются в организме ребенка уже в первые часы жизни,
176

 источником его энергоснабжения и периоде новорожденности становятся жиры.
источником его энергоснабжения и периоде новорожденности становятся жиры.
У детей раннего возраста преобладает мембранное и внутриклеточное пищеварение; последнее осуществляется по механизму пино-цитоза. У грудных детей, помимо мембранного, внутриклеточного и полостного пищеварения, имеет место и аутолитический тип пищеварения, который за счет ферментов, содержащихся в женском молоке (особенно молозиве), компенсирует недостаточность полостного пищеварения.
На протяжении первого года жизни женское молоко, имеющее в своем составе оптимальное количество веществ, необходимых для развития ребенка, является основным продуктом питания. Углеводы молока, главным образом, представлены молочным сахаром (лактозой). В женском молоке содержится Д-лактоза. Поскольку в полости рта и желудке молоко находится очень короткое время, оно не подвергается там сколько-нибудь существенным изменениям. Гидролиз лактозы происходит преимущественно в области щеточной каймы кишечного эпителия. В-лактоза женского молока более медленно, чем а-лактоза коровьего молока, подвергается гидролизу в тонком кишечнике и частично поступает в толстый кишечник, где происходит ее дальнейшее расщепление бактериальной флорой. Это способствует поддержанию нормального биоценоза кишечника.
После введения ребенку прикорма, содержащего большое количество крахмала, возрастает роль амилазной активности слюнных желез и поджелудочной железы.
Переваривание белков осуществляется при участии многих ферментов желудка, поджелудочной железы и тонкого кишечника. Особенностью переваривания и усвоения белков у новорожденных является большая роль внутриклеточного звена пищеварения. В первые два месяца жизни ребенка пепсиноген переходит в пепсин не под влиянием соляной кислоты, которая еще не вырабатывается, а под влиянием молочной кислоты. У грудных детей кислотность желудочного сока ниже, чем у взрослых (рН, соответственно, равно 3-4 ед. и 1-2 ед.), что обеспечивает оптимум действия пепсина. Однако, в этот возрастной период наибольшей активностью обладает химозин желудочного сока, осуществляющий створаживание молока, образуя его мелкие хлопья, что облегчает гидролиз казеина (легко расщепляющегося белка). В отличие от женского молока для казеиногена коровьего молока характеры крупные сгустки, что затрудняет его дальнейшее переваривание. В результате, у детей первых недель жизни усвоение белков женского молока составляет 90-95%, а белков коровьего молока — 60-70%. Более высокой абсорбции белков женского молока способствуют содержащиеся в нем протео-литические ферменты (пепсин и трипсин).
Относительно слабая переваривающая сила желудочного сока у новорожденного биологически целесообразна с той точки зрения, что материнские глобулины, находящиеся в молоке, не расщепляются в желудке ребенка, и, всасываясь в кишечнике в нативном виде, в какой-то мере обеспечивают иммунитет ребенка.
177





 У детей первого года жизни жиры женского молока, благодаря наличию липазы в слюне, желудочном соке и самом молоке, начинают расщепляться в желудке. Гидролиз жира может происходить и в отсутствие желчных солей. Жиры с длинной углеродной цепью расщепляются под влиянием панкреатической липазы в присутствии желчных кислот. Следовательно, незрелость внешнесекреторной функции печени оказывает существенное влияние на степень абсорбции жира. Новорожденный ребенок способен абсорбировать 85-90% жира женского молока. Однако, жиры коровьего молока усваиваются в этом периоде в значительно меньшем количестве. В связи с этим, для приготовления адаптированных молочных смесей используется добавка жиров растительного происхождения, которые легче подвергаются гидролизу и усвоению, чем жиры коровьего молока.
У детей первого года жизни жиры женского молока, благодаря наличию липазы в слюне, желудочном соке и самом молоке, начинают расщепляться в желудке. Гидролиз жира может происходить и в отсутствие желчных солей. Жиры с длинной углеродной цепью расщепляются под влиянием панкреатической липазы в присутствии желчных кислот. Следовательно, незрелость внешнесекреторной функции печени оказывает существенное влияние на степень абсорбции жира. Новорожденный ребенок способен абсорбировать 85-90% жира женского молока. Однако, жиры коровьего молока усваиваются в этом периоде в значительно меньшем количестве. В связи с этим, для приготовления адаптированных молочных смесей используется добавка жиров растительного происхождения, которые легче подвергаются гидролизу и усвоению, чем жиры коровьего молока.
Нейрогуморальная регуляция желудка проявляется в конце первого месяца жизни ребенка, когда гистамин у новорожденного начинает оказывать стимулирующее влияние на желудочную секрецию. Моторная функция желудка слабо выражена; кардиальный сфинктер имеет низкий тонус, в результате чего содержимое желудка нередко забрасывается в пищевод и срыгивается; из-за слабости пилоричес-кого сфинктера отмечается ускоренный переход пищевых масс из желудка в 12-перстную кишку.
В первые месяцы жизни ребенка внешнесекреторная функция поджелудочной железы быстро нарастает (особенно при искусственном вскармливании), обеспечивая гидролиз легкоусвояемых пищевых веществ молока. Так, объем панкреатической секреции к концу 1-го года жизни увеличивается в 10 раз. Увеличивается и ферментативная активность панкреатического сока: первой повышается активность протеиназ, а к 9 годам становится максимальной амило- и липо-литическая активность.
Пищеварительная функция печени развивается медленно; во внутриутробном периоде главная функция печени состоит в образовании белков плазмы. В течение первого полугодия постнатальной жизни ребенок получает преимущественно жировую диету (около 50% калорийности женского молока покрывается за счет жира, что сопровождается его недорасшеплением в кишечнике). Последнее объясняется ограниченной липазной активностью поджелудочной железы в этот возрастной период и недостатком желчных солей, образуемых гепатоцитами. Особенно низка активность желчеобразования у недоношенных детей. Этот дефицит при грудном вскармливании в какой-то мере компенсируется хорошим эмульгированием жира женского молока.
Дезаминизация аминокислот в печени в неонатальном периоде мало эффективна. В первые дни жизни ребенка наблюдается недоразвитие глюкоронилтрансферазной активности, что ограничивает возможности экскреции билирубина. Это является главной причиной билирубинемии новорожденных (физиологическая желтуха). У недоношенных детей активность глюкоронилтрансферазы особенно недостаточна, и, следовательно, предрасположенность к желтухе у них выражена больше.
178


 Поджелудочная железа способна к секреторной деятельности уже непосредственно после рождения. Панкреатическую секрецию может поддерживать молочная кислота, имеющаяся в желудке в раннем постнатальном периоде, когда сколько-нибудь значительные количества соляной кислоты там отсутствуют. У ребенка объем панкреатической секреции к концу 1-го года жизни увеличивается в 10 раз, а амилазы — в 25 раз. Активность протеиназ достигает максимального уровня к 3 годам; амило - и липолитическая активность выходят на зрелый уровень к 9 годам.
Поджелудочная железа способна к секреторной деятельности уже непосредственно после рождения. Панкреатическую секрецию может поддерживать молочная кислота, имеющаяся в желудке в раннем постнатальном периоде, когда сколько-нибудь значительные количества соляной кислоты там отсутствуют. У ребенка объем панкреатической секреции к концу 1-го года жизни увеличивается в 10 раз, а амилазы — в 25 раз. Активность протеиназ достигает максимального уровня к 3 годам; амило - и липолитическая активность выходят на зрелый уровень к 9 годам.
В процессе внутриутробного развития в системе пищеварения нарастает число эндокринных клеток и в них повышается содержание регуляторных пептидов (гастрина, секретина и др.). К моменту рождения в кишечнике ребенка содержатся все необходимые для пищеварения ферменты: энтерокиназа, щелочная и кислая фосфота-за, эрепсин, лактоза и другие, причем, активность сахарозы и мальтозы проявляется раньше, чем лактозы. С возрастом их содержание увеличивается. В детском возрасте выработка протеаз в кишечнике увеличивается в 40 раз, что обеспечивает более интенсивное расщепление белка.
Транспорт глюкозы через эпителий тощей кишки начинается на 20-й неделе внутриутробного развития, однако, взрослого уровня эта функция достигает через несколько лет после рождения.
Всасывание жиров у недоношенных детей ниже, чем у родившихся в срок, а у последних ниже, чем у более старших детей. Это объясняется низким уровнем синтеза и транспорта солей желчных кислот в первый год жизни.
Участие пищеварительной системы в детоксикации организма особенно важно для новорожденного ребенка, когда другие пути выведения токсических продуктов метаболизма (почки, печень, кожа) в этом возрасте еще незрелые. В этот возрастной период высока роль пищеварительного тракта и для поддержания водного и электролитного гомеостаза, поскольку почечная функция еще не установилась в полной мере.
При стрессе, особенно у недоношенных, прохождение пищи по незрелому желудочно-кишечному тракту ускоряется, что приводит к снижению всасывания воды и питательных веществ и дегидратации ребенка.
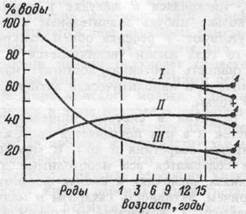
Почки и водно-солевой обмен. Ворганизме плода и ребенка общее содержание жидкости повышено. У ребенка раннего возраста внеклеточная жидкость составляет около 45% массы тела, а к зрелому возрасту она уменьшается до 18% (рис. 18.5). Такая динамика обусловлена уменьшением интерстициального пространства: внутри клеток нарастает содержание недиффундирующих протеинов и других осмотически активных субстанций, вследствие чего увеличиваются объем внутриклеточной жидкости и размеры клеток. Кроме того, у новорожденных и грудных детей из-за высокой активности альдостсрона в организме задерживаются гидрофильные ионы натрия.
179
 | ||||||
 |  | |||||
 | ||||||
|
Рис. 18.5. Возрастная характеристика распределения воды у плода и детей различною возраста.
I — общее
Дата добавления: 2016-03-27; просмотров: 937;
