Топливо Уд. теплота сгорания
МДж/кг
Дрова 8,3-15,5
Горючий сланец 8,4 – 20
Торф 8,4 – 21
Бурый уголь 10,5 – 21
Каменный уголь ок. 29,4
Антрацит 32,8- 32,6
Природный горючий газ на 1 куб.м 25,2-46,2
Нефть 42
По энергетической ценности виды топлива характеризуются следующим образом:
Топливо Энергетическая ценность
КВт ч /кг
Дрова 2,33-4,32
Горючий сланец 2,33 – 5,82
Торф 2,33 – 4,66
Бурый уголь 2,92 -5,82
Каменный уголь ок. 8,15
Антрацит 9,08 – 9,32
Природный горючий газ на 1 куб.м 6,98 – 12,82
Нефть 11,63
Различные виды топлива соизмеряются по их удельной теплоте сгорания, т.е. по количеству энергии, виделяющейся при сжигании кило-грамма топлива.
Для исчисления общих запасов топлива различные его виды мысленно заменяют так называемым условным топливом с удельной теплотой сгорания 29,4 МДж/кг. Обозначив удельную теплоту сгорания данного топлива через Q, а его количество ( в килограммах или тоннах) через Т, найдем эквивалентное ему количество Х условного топлива по одной из следующих формул:
Х=ТQ /29,4 или Х=ТQ/ 8,15,
в зависимости от того, в каких единицах (МДж/кг или кВт·ч/кг) задана Q.
Практически при соответствующих расчетах принимают:
1т каменного угля = 1 т условного топлива
1т бурого угля = 0,4 т условного топлива
1т нефти = 1,4 условного топлива
1000 м3природного газа = 1,3 т условного топлива
Несколько сложнее соизмерение топливных и нетопливных энергетических ресурсов. Мощность гидроэнергии, измеряемая в киловаттах, зависит от высоты (напора) воды и ее расхода, т.е. количество воды, протекающей в выбранном створе реки в единицу времени. Ее исчисляют следующим образом.
Вода, падая с высоты, производит работу, равную произведению ее веса на высоту падения. Масса воды пропорциональна ее объему. Обозначив через R ее расход, т.е. количество кубометров воды, падающей за секунду, а через Н – высоту падения, выраженную в метрах, можно вычислить мощность N водного потока в киловаттах по следующей формуле:
N=(1000/102) RH=9,8 RH.
В этой формуле 1000 – число килограммов в кубометре воды, а 102 – число килограммометров в секунду, равное одному киловатту мощности.
Принимая средний коэффициент полезного действия гидроустановки равным 0,80-0,85, получаем практическое выражение для потенциальной (теоретической) мощности водного потока:
N= 8RH, кВт.
Понятие условного топлива применяют не только для исчисления общих отходов топлива, но и для исчисления энергетических ресурсов любого вида. Исходной величиной при этом служит среднее количество весовых единиц условного топлива, фактически расходуемых на тепловых электростанциях для получения одного киловатт-часа электроэнергии при данном уровне энергетической техники ( в настоящее время -около 0,35 кг). При помощи этой величины определяют какому количеству условного топлива эквивалентны ресурсы нетопливных источников энергии (количество киловатт-часов электроэнергии, которые можно получить от них за год).
Запасы гидроэнергии на определенной территории представляют сумму потенциальной мощности всех водотоков, умноженную на число часов возможного ее использования за год. Это потенциальные (теоретические) гидроэнергоресурсы. Наряду с ними различают: технически возможные к использованию гидроэнергоресурсы – часть потенциальных, которая при данном уровне техники практически может быть использована; экономически эффективные гидроэнергоресурсы, использование которых при существующих условиях экономически выгодно.
При соизмерении невозобновляющихся и возобновляющихся энергетических ресурсов необходимо учитывать скорость возобновления (прирост древесины, а иногда и торфа).
В состав всех видов топлива входит горючая масса (органическая масса и горючие неорганические вещества: сера, ее соединения и т.д.) и негорючая масса (зола, влага). Чем больше в топливе золы, влаги, тем ниже его теплота сгорания. Чем выше в органической массе содержание углерода и водорода и чем ниже содержание кислорода и азота, тем больше теплота сгорания топлива.
Одним из важнейших видов жидких топлив является нефть, которая содержит в органической части 83-87% углерода и 12-14% водорода. Удельная теплота сгорания нефти колеблется в пределах 35,8-44 МДж/кг.
Природный газ содержит до 98% метана и является наиболее эффективным видом топлива. В пределах Украины имеются практически все виды топлива, в том числе нефть и газ.
2.5. Основные источники и характеристики воды
Вода занимает важное место в жизни и деятельности человека. Распространение воды: 97,57% – в мировом океане, 2,14% – в высокогорных ледниках и полярных льдах, 0,29% – в реках и озерах, в водяных парах атмосферы – около 0,001%. Примерно 7% массы земной коры составляют подземные воды.
Для бытовых и промышленных нужд применяется только пресная вода (содержание солей до 1 г/л), составляющая 3% всех запасов воды.
Расход воды на душу населения в крупных городах США и Европы составляет 600-700л в сутки, в развивающихся странах – 50 л.
В воде содержатся почти все элементы системы Менделеева. Ее обшая масса 1,4х1018т, в ней содержится 2,8 млрд. т урана. Если извлечь из нее только 0,01% содержащегося урана, то его хватит на 100 лет для выработки электроэнергии для всего человечества.
Качество воды определяется ее химическими и физическими характеристиками, такими как жесткость, общее солесодержание, прозрачность, окисляемость и др. Для питьевых нужд большое значение имеет количество токсичных примесей (мышьяк, стронций, радий, радиактивный уран), содержание микробов, запах, цвет и вкус. Для технических нужд важны показатели жесткости, содержание солей, механических примесей.
Жесткость воды характеризуется содержанием в ней солей кальция и магния. Различают жесткость воды трех видов: временную, постоянную и общую.
Временная (устранимая) жесткость характеризуется содержанием в воде бикарбонатов кальция и магния, которые легко удаляются из воды простым кипячением. Бикарбонаты переходят в нерастворимые углекислые соли и выпадают в виде плотного осадка.
Постоянная жесткость воды связана с присутствием в ней хлоридов, сульфатов, нитратов кальция и магния. Эти соли не удаляются при кипячении воды. Временная и постоянная жесткость в сумме дают общую жесткость. Вода имеет жесткость, равную единице, если в литре ее содержится 1 мг-экв ионов кальция или магния. Жесткость вызывает агресивность по отношению к бетону. При содержании 250 млг/л сульфатных ионов наступает разрушение бетонного камня.
Общее солесодержание или сухой остаток – масса вещества, оставшегося после испарения воды и высушивания полученного остатка при 105...110°С до постоянной массы. Сухой остаток выражается в миллиграммах на 1 литр воды.
Прозрачность воды определяется толщиной слоя воды, через который можно различить крест или шрифт определенного размера (без или с помощью фотоэлемента). В открытых районах Черного моря она равна 24...28 м.
Окисляемость воды определяется массой (в миллиграммах) перманганата калия, взаимодействующего с 1 л воды при кипячении в течение 10 минут.
Кислотность или щелочность воды характеризуется концентрацией водородных ионов или величиной pH = – 1g [H+, моль/л].
При pH = 6,5 – 7,5 вода считается нейтральной, при pH < 6,5 воду называют кислотной, при pH > 7,5 – щелочной.
| |
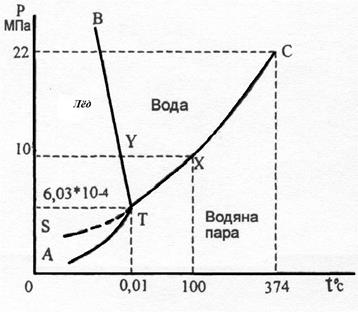
Например, при определенных значениях темпера-туры и давления, которое соответствует точкам диаг-раммы в плоскости, огра-ниченной кривыми ВТ и СТ, вода существует только в жидком состоянии, в точках ниже кривых АТ и ТС – в виде пара.
Точки на кривых соответствуют условиям, при которых две смежные фазы находятся в равновесии.
Две точки на диаграмме вызывают особый интерес. Точка Т (0,01оС и 6,03·10-4МПа) называется тройной точкой, где в равновесии находятся одновременно три фазы: пар, вода и лед. Точка С (347оС и 22,0 МПа) называется критической. При температуре свыше 374оС пар воды нельзя преобразовать в жидкость при увеличении давления. Иными словами, при температуре и давлении свыше чем в точке С, пар и жидкость воды не различаются. Между ними не существует фазовой линии.
Диаграмма состояния воды играет исключительно важную роль при проектировании и эксплуатации паровых котлов, энергетических турбин энергосистем, автоклавов и т.д.
2.6. Классификация вод
Природные воды делятся на три вида, различающиеся по наличию примесей: атмосферные, поверхностные и подземные.
Атмосферная вода– это вода дождевых и снеговых осадков, она характеризуется сравнительно небольшим содержанием примесей, главным образом растворенных газов: кислорода, углекислого газа, сероводорода, оксидов азота, кислородных соединений серы, органических веществ, которые определяют атмосферу в промышленных районах. Атмосферная вода почти не содержит растворенных солей, в частности солей кальция и магния.
Поверхностные воды – речные, озерные, морские содержат, кроме примесей, имеющихся в атмосферной воде, разнообразные вещества. В ней есть двууглекислые соли кальция, магния, натрия и калия, а также сернокислые и хлорные соли. При содержании солей менее 1 грамма на литр воды она называется пресной, более одного грамма – соленой.
Подземные воды – артезианских скважин, колодцев, ключей, гейзеров – характеризуются разнообразным содержанием солей, состав которых зависит от вида и структуры почв и горных пород, через которые просачиваются атмосферные воды и воды поверхностных водоемов, образуя подземные водоемы. Фильтрующая способность почв и горных пород обусловливает высокую прозрачность подземных вод и отсутствие в них примесей органического происхождения. Уникальным сырьем для химической промышленности являются минеральные воды, насыщенные различными солями. Так, воды насыщенные хлористым натрием, служат сырьем для производства соды, едкого натра и хлора. Из подземных рассолов получают также йодистые, бромистые соединения и другие соли.
В зависимости от назначения вода условно подразделяется на промышленную и питьевую. Питьевая вода в первую очередь освобождается от бактерий; к ней предъявляются особые требования в отношении вкуса, цвета, запаха. Промышленные воды не должны содержать примесей больше допустимой нормы, которая устанавливается в зависимости от вида производства.
Вода для прямоточных паровых котлов не должна содержать окисей углерода и кислорода, вызывающих коррозийное разрушение труб, и может содержать сухой остаток не более 0,2...0,3 мг/л. Соли в паровых котлах отлагаются на внутренних поверхностях труб в виде накипи, снижают теплопроводность их стенок, приводят к перегреву труб и преждевременному их износу. Повышенные требования в отношении чистоты предъявляются к воде в производстве полупроводников, люминофоров и некоторых других материалов.
2.7 Очистка и обезвреживание воды
Очистка воды от примесей, т.е. подготовка, включает следующие операции: осветление, обесцвечивание, обеззараживание, смягчение, дегазацию.
Осветление и обесцвечивание природной воды производится с целью удаления из нее механических примесей. Это достигается отстаиванием ее в бетонированных резервуарах большой вместимости (отстойниках) с последующим пропусканием через песчаные фильтры с зернистым фильтрующим слоем. Для осаждения коллоидных примесей в отстойники вводят коагулянты – сульфаты железа или алюминия, в результате чего вода обесцвечивается. Осадки удаляются из воды при отстаивании и фильтровании.
Обеззараживание воды – обязательный процесс очистки воды, используемой для бытовых нужд. Уничтожение болезнетворных микробов и окисление органических примесей достигается хлорированием – введением газообразного хлора, хлорной извести, гипохлорида кальция, а также озонированием и кипячением. При обработке воды хлором вода приобретает его запах, при озонировании запах отсутствует, что является достоинством данного метода. Вода обеззараживается также обработкой ионами серебра и при воздействии ультрафиолетовых лучей и ультразвуковых колебаний.
Для того, чтобы после обработки в воде не оставался избыток хлора, ее дехлорируют. При этом избыток хлора либо химически связывается, либо удаляется при пропускании воды через угольные фильтры. Умягчение и обессоливание воды – основные процессы ее подготовки. Удаление из воды всех солей (всех катионов и анионов) называется обессоливанием, только солей кальция и магния – смягчением. Полное обессоливание воды (дистиллирование) применяется сравнительно редко. Способы умягчения воды подразделяются на физические, химические и физико-химические.
К физическим способам относятся – кипячение, дистилляция и вымораживание.
Дистиллированную (полностью обессоленную) воду получают перегонкой на специальных дистилляционных установках.
Сущность химических методов умягчения заключается в связывании ионов кальция и магния при помощи реагентов в нерастворимые и легкоудаляемые осадки. В зависимости от применяемых реагентов различают способы: а) известковый – обработка гашеной известью; б) содовый – воздействуют кальцинированной содой; г) натронный – обработка едким натром; д) фосфатный – воздействуют тринатрийфосфатом.
Сущность ионообменного (физико-химического) способа состоит в удалении из воды ионов кальция и магния при помощи ионитов (ионообменных солей), способных обменивать свои ионы на ионы, содержащиеся в воде.
Современным физико-химическим методом смягчения воды является электрохимический, в частности электрокоагуляция, которая производится в электролизерах с растворимыми электродами.
Дегазация воды– удаление из нее растворенных газов – осуществляется химическим и физическим способами.
Физические способы удаления газов заключаются в аэрации или нагревании воды в вакууме.
Производственные и бытовые сточные воды обычно содержат различные органические и неорганические примеси, которые при сливе в водоемы загрязняют их. Спуск промышленных сточных вод в водоемы производится в соответствии с санитарными правилами, которыми определено предельно допустимое содержание веществ в сточных водах.
Способы очистки и обезвреживания сточных водподразделяются на механические, физико-химические, химические и биологические.
Механические способы очистки сточных вод от примесей заключаются в их отстаивании и фильтровании, в частности, через полупроницаемые мембраны под давлением.
Физико-химические методы основаны на применении флотации, экстракции и адсорбции вредных примесей, отгонки их с водяным паром. Разновидностью физико-химических методов являются термические, например, испарение воды при нагревании и сжигании органической части сухого остатка.
Химические методы очистки сточных вод основаны на использовании окислительно-восстановительных, электрохимических процессов, реакций нейтрализации и перевода вредных веществ в неактивную безвредную форму. Биологический метод заключается в разложении и окислении вредных примесей с помощью микроорганизмов. Среди встречающихся в почве микроорганизмов наиболее многочисленными являются грибы, водоросли и бактерии. Они «атакуют» содержащиеся в сточных водах органические вещества, которые представляют собой прекрасную питательную среду для микробов, и разлагают углеводы, жиры и другие соединения на двуокись углерода, воду и минеральные соли. Различают процессы биологической очистки, протекающие в естественных и искусственно созданных условиях, проводимых на специальных очистных станциях.
2.8. Воздух в технологических процессах
Наряду с природной водой воздух широко используется в различных технологических процессах.
Прежде всего, воздух расходуется в энергетических агрегатах во время сжигания органических энергоносителей (угля, газа, мазута, бензина) – тепловых электростанциях и двигателях внутреннего сгорания. Большие объемы воздуха используют в металлургии: на производство 1т стали его расходуют около 15· 103 м3на 1т меди – примерно 60 · 103м3. Воздух широко используется для транспортирования материалов (пневмотранспорт), при теплопередаче и охлаждении технологических объектов, как рабочее тепло в пневматических системах. Некоторые физические характеристики атмосферного воздуха: плотность – 1,293 кг/м3; средняя молярная масса (условно) – 29; критическая температура – 140,7 0С, критическое давление 3,72 МПа
Существенную роль в промышленности играют отдельные составные воздуха, характеристики которых приведены в табл. 2.1.
Состав воздуха и его свойства
Таблица 2.1
| Складові | Вміст, % | Густина, кг/м³ | Температура кипіння, ºС | Молекулярна маса, а.о.м. | |
| за об’ємом | за масою | ||||
| Азот (N2) | 78,15 | 75,6 | 1,25 | –195 | |
| Кисень (О2) | 20,9 | 23,1 | 1,43 | –183 | |
| Аргон (Ar) | 0,9 | 1,3 | 1,78 | –196 | |
| Діоксид вуглецю (СО2) | 0,03 | 0,04 | 1,96 | – 78 | |
| Гелій (Не) | 1∙10‾3 | 7∙10‾4 | – | – | – |
| Неон (Nе) | |||||
| Криптон (Kr) | |||||
| Ксенон (Хе) | |||||
| Озон (О3) | 1∙10‾6 | 3∙10‾6 | 2,1 | – | |
| Водень (Н2) | 5∙10‾5 | – | 0,09 | –253 | |
| Радон (Rn) | 6∙10‾18 | – | – | – |
Содержание водяного пара в воздухе колеблется от долей процента до нескольких процентов и зависит от местных условий и температуры. Определенной температуре и давлению соответсвует конкретное содержание водяного пара в воздухе. Отношение абсолютной влажности воздуха к максимально возможной, выраженной в %, называется относительной влажностью воздуха.
Зная относительную и абсолютную влажность насыщенной парами воды воздуха, можно вычислить концентрацию воды в воздухе, что иногда является необходимым в технологических процессах. Используя полученные данные и фазовую диаграмму воды (см. рис 2.6), можно предусмотреть условия конденсации водяного пара (выпадание росы) на поверхности машин, изделий, предотвращение возникновения процессов коррозии и др. При охлаждении ниже О0С вода почти полностью конденсируется в лед (иней). При температуре ниже -192 0С и давлении 760 мм водяного столба из воздуха образуется легкоподвижная голубая жидкость плотностью 960кг/м3.
Поскольку температура кипения кислорода (-183 0С) выше температуры кипения азота (-196 0С), кислород легче переходит в жидкое состояние, нежели азот, вследствие чего жидкий воздух богаче на кислород, нежели атмосферный. Жидкий воздух можно достаточно долго хранить в специальных термосах-сосудах Дьюара. Во время хранения жидкий воздух еще больше обогащается на кислород вследствие испарения азота, аргона, и др. методом ректификации - перегонкой.
Горение в чистом кислороде проходит быстрее, нежели в воздухе, и тепло не затрачивается на нагрев азота воздуха. Этот эффект используется для получения высоких температур до 3200 0С) при сжигании (ацетилена, водорода) в специальных горелках, которыми сваривают и разрезают металлы.
Кислород интенсифицирует химические процессы многих производств. В доменном процессе при обогащении кислородом дутья повышается производительность плавки, в производстве серной и азотной кислот, в процессе полимеризации этилена. Смесь сжиженного кислорода с органическим веществом (углем, древесиной) имеет сильные взрывчатые свойства и применяется в горнодобывающей технологии для взрывных работ.
В противоположность кислороду, второй компонент воздуха – молекулярный азот – химически малоактивный газ. Атмосферный азот в больших количествах применяется как исходное вещество для синтеза аммиака и некоторых соединений, а также как инертная среда.
Аргон широко применяется как инертный газ в спецметалургии, сварке, как рабочее тело в плазмотронах. Важное значение в процессах новых технологий имеют и другие инертные газы.
ОСНОВНЫЕ ПОНЯТИЯ
Природное сырье
Искусственное сырье
Минеральное и органическое сырье
Рудное сырье
Полиметаллическое сырье
Обогащение сырья
Концентрат
Хвосты обогащения
Гравитационное обогащение
Магнитная сепарация
Флотация
Качество сырья
Проба благородного метала
Карат
Топливо
Условное топливо
Жесткость воды
Кислотность или щелочность
Фазовая диаграмма воды
Тройная точка
Относительная и абсолютная влажность
Сосуд Дьюара
ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
1. Расскройте понятие “сырье”
2. По каким признакам классифицируется сырье?
ГЛАВА 3. СИСТЕМА ТЕХНОЛОГИЙ В ЭНЕРГЕТИКЕ
3.1. Основные виды и источники энергии
Энергетический потенциал планеты включает практически неистощимые источники энергии – солнце, ветер, воды рек и морей – и невосполнимые, связанные с использованием полезных ископаемых – нефти, угля, природного газа, урановых руд, горючих сланцев и торфа.
Источники энергии первой группы, за исключением гидроэнергии рек, до настоящего времени занимают незначительное место в мировом энергетическом балансе.
Энергия необходима как для проведения самого технологического процесса, так и для транспортировки сырья и готовой продукции, вспомогательных материалов. В структуре себестоимости продукции затраты на электроэнергию составляют более 30%, что свидетельствует о высокой энергоемкости некоторых видов производств, которые в 5 раз превышают достигнутые в мире с применением новейших технологий.
В промышленности применяются разнообразные виды энергии: электрическая, тепловая, ядерная, химическая и энергия света.
3.2. Система технологий тепловых электростанций
На тепловых электростанциях (ТЭС) источником энергии является органическое топливо, прежде всего уголь, а также горючие сланцы, нефтяной мазут, газ. Система технологий теплоэнергетики состоит из следующих звеньев (при работе на угле).
1. Добыча угля (подземным или открытым способом).
2. Обогащение и подготовка к сжиганию.
3. Сжигание угля и получение пара высокого давления.
4. Конверсия тепловой энергии пара последовательно в механическую энергию турбоэлектрогенератора и электрическую (в одном блоке турбоэлектрогенератора).
Основное оборудование паротурбинных ТЭС:
1. Котлоагрегат (паровой котел, пароперегреватель).
2. Турбогенератор (паровая турбина, соединенная с электрогенератором).
Тепловые электоростанции, на которых в качестве привода электрогенераторов применяют так называемые конденсационные турбины, называют конденсационными электростанциями (КЭС).
Паротурбинные электростанции, вырабатывающие и отпускающие потребителям одновременно 2 вида энергии: электирическую энергию и теплоту (получаемую в результате частичного использования отрабатываемого пара) называют теплоэлектроцентралью (ТЭЦ).
На рис. 3.1 изображена упрощенная иллюстрационная система ТЭС. Реальные агрегаты конструктивно значительно сложнее.

Рис. 3.1. Технологическая схема конденсационной ТЭС
1 – котлоагрегат, 2 – турбина, 3 – электрогенератор, 4 – конденсатор,
5 – циркуляционный насос, 6 – градирня, 7 – насос градирни,
8 – конденсационный насос 1 ступени, 9 – обессоливающая установка; 10 – конденсационный насос 2 ступени, 11 – подогреватель низкого давления;12 – деаэратор; 13 – бустерный питательный насос; 14 – питательный насос; 15 – подогреватель высокого давления.
При сжигании топлива в топке котлоагрегата 1 поступающая в него по трубам вода превращается в пар. Под высоким давлением пар подается в турбину 2, где он, воздействуя на лопасти ротора турбины, приводит его во вращающееся движение. Ротор турбины механически связан с ротором электрогенератора 3, в трехфазной статорной обмотке которого при вращении ротора образуется эдс., т.е. вырабатывается электроенергия.
Отработавший в турбине пар подается по трубопроводу в конденсатор 4, являющейся частью турбоагрегата. Конденсатор представляет собой теплообменник для осуществления перехода воды из парообразного состояния в жидкое. Конденсация пара происходит в результате попадания пара в паропровод теплообменника с более низкой температурой, чем температура насыщения пара при данном давлении. Конденсация пара сопровождается выделением теплоты,которая отводится от горячего паропровода при помощи охлажденной воды, циркулирующей с помощью циркуляционного насоса 5 через теплообменник 4 и градирню 6.
Градирня представляет собой пустотелое сооружение в форме усеченного конуса для охлаждения воды атмостферным воздухом. Насос 7 подает воду внутрь градирни, где она распыляется в виде фонтана. Охлаждение происходит в основном за счет испарения воды сквозным воздушным потоком, движущимся снизу вверх.
Превращению пара в воду, помимо охлаждения, способствует вакуум, создаваемый в паропроводе теплообменника конденсационными нососами 1 и 2 ступеней 8 и 10. Далее вода через обессоливающую установку 9, подогреватели низкого и высокого давлений 11, 15 и деаэратор 12 с помощью бустерного 13 и питательного 14 насосов направляется в котлоагрегат для повторного использования.
Деаэратор представляет собой аппарат для удаления из воды растворенных в ней кислорода и диоксида углерода, вызывающих коррозию труб и другого оборудования. По принципу действия деаэраторы бывают термические, химические и др.
Бустерный насос -это вакуумный насос, установленный между конденсационными насосами с целью приведения в соответсвие разных уровней их выпускного давления.
Таким образом, получается замкнутый пароводяной тракт: котлоагрегат – паровая турбина-конденсатор-котлоагрегат.
Повышение давления и температуры пара перед турбинами и снижение конечной температуры и давления отработанного пара увеличивает КПД конденсационной электростанции. При работе КЭС практически вся энергия, сообщенная пару при сжигании топлива, преобразуется в электрическую. Часть выработанной электроенергии расходуется на обеспечение собственных нужд электростанции (работа вспомагательного оборудования, освещение, вентиляция и пр.). Общий КПД современных КЭС достигает 35-42%. Обычно КЭС работают на местных твердых топливах, мазуте и природном газе.
Конденсационные электростанции являются основным типом мощных тепловых электростанций.
Тепловые конденсационные электростанции чаще всего называют ГРЭС, т.е. государственные районные электростанции. Это название устарело и не соотвествует действительности. Раньше, когда не было энергосистем, каждая ТЭС обеспечивала потребителей в пределах того района, где сама распологалась. В настоящее время при наличии единых энергосистем страны слово "районная" потеряло смысл.
ТЭЦ оборудуют преимущественно теплофикационными турбинами, т.е. турбинами без конденсатора. В таких турбинах давление на выходе последней ступени выше атмосферного. Отработавший в турбине пар либо отводится в теплофикационную сеть, либо направляется в специальные водонагреватели, где пар отдает тепло воде, которая идет на отопление жилищ, обеспечение коммунально-бытовых потребностей в горячей воде и технологических нужд промышленных предприятий.
Комбинированное производство электороэнергии и тепла способствует более эффективному использованию топлива по сравнению с раздельной выработкой электроэнерги на КЭС и тепла в местных котельных. Кроме того, местные котельные не всегда рационально используют отпускаемое им топливо, загрязняют атмосферу выбросами продуктов сгорания и тем самым ухудшают окружающую среду населенных пунктов. Такие города как Киев и Харьков для тепло – и электроснабжения используют по нескольку ТЭЦ.
Пример.Чтобы уяснить экологическую проблему ТЭС, следует проанализировать количественные характеристики отходов в цепи потока энергии от добычи угля до получения электроэнергии.
Но расчеты удобнее производить, задаваясь мощностью электрогенератора и по очереди переходить до предыдущей стадии конверсии.
Поэтому, если мощность достаточно большого турбогенератора составляет 1000МВт, коэффициент полезного действия конверсии механической энергии паровой турбины в электрическую – 0,95, а энергии пара в механическую – 0,37, то коэффициент конверсии химической энергии угля в тепловую энергию пара и далее в электрическую будет равнятся произведению:
η = 0,95 х 0,37 = 0,36
Если удельная теплота сгорания качественного каменного угля составляет около 28 МДж/кг, то ежесекундно нужно сжигать
1000 МДж
------------------------------------ = 100 кг
0,36 х 28 МДж х кг-1
То есть 100 кг угля, которые сжигаются за 1с,эквивалентны 1000 МДж, то есть мощности в 1000 МВт.
Рассмотрим материальные потоки при реализации конверсии химической энергии 100 кг угля в электрическую. Состав разных видов каменного угля колеблется в довольно широких пределах. Так, содержание углерда составляет 75...97%, водорода 2...15%, серы 1... 4%, азота до 1,5%. Кроме приведенных химических элементов уголь содержит много металлов и неметаллов, которые, сгорая, образуют до 6% золы и легкие соединения, многие из которых ядовиты. Исдходя из средних значений приведенных данных состава угля, выполним расчеты (на 100кг угля).
Выход диоксида углерода (СО2) и расход кислорода для полного сгорания согласно стехиометрическим уравнениям: С+О2= СО2
Молярные массы кг/моль: С=12; О2= 32; СО2= 44
Масса полученного СО2из 100 кг угля со средним содержанием 86% углерода составит:
44 х 86
СО2= ------------------------------ = 315 кг
315 кг
Количество вещества СО2= ------------------------------- = 7,15 моль
44 кг х моль -1
Масса расходуемого кислорода на сжигание 100 кг угля составляет
32 х 86
О2= ------------------------ = 229,3 кг
229,3 кг
Количество вещества О2 = ------------------------------- = 7,16 моль
32 кг х моль-1
Выход диоксида серы из 100 кг угля определим исходя из среднего содержания серы в угле 2,5% согласно уравнению: S+ O2= SO2
Молярные массы, кг/моль: S=32; O2 =32; SO2= 64
64 х 2,5 кг
Масса SO2 = ---------------------------- = 5 кг
5 кг
Количество вещества SO2 = --------------------------- = 0,08 моль
64 кг х моль-1
3,3
Выход оксидов азота в пересчете на NO2= ---------- = 0,07 моль
Расход суммарного количества вещества кислорода на окисление серы и азота определим исходя из того, что согласно уравнению на один моль SO2и NO2расходуется по одному молю О2, поэтому на получение 0,08 моль SO2и 0,07 NO2 будет израсходовано 0,08 + 0,07 = 0,15 моль О2или 0,15 х 32 = 4,8 кг. Вместе с расходами на окисление углерода 7,31, или 7,31 х 32 = 233,9 кг.
Объем воздуха (при нормальных условиях содержания О2=2,3%), который забирается из окружающей среды и выбрасывается в виде дыма в измененном химическом составе через трубу просто в небо:
VВ= 1015 : 1,29 = 775 м3( Ѕвозд= 1,29 кг/м3)
С воздухом поступает азот соответственно содержанию (76% массы) 1015 х 0,76 =771 кг. Состав дыма (без учета излишков воздуха и влаги) можно определить исходя из того, что количество израсходованного кислорода (7,3 моля) эквимолекулярно будет заменено диоксидами СО2, SO2,NO2.
Таким образом, если на входе в топку с воздухом на каждые 100 кг угля за секунду поступает 7,4 моля кислорода и 771 : 28 = 27 молей азота, т.е. 7,31 + 27 = 34,31 моля, то на выходе получим более 34,3 моля газа. Суммарное количество вещества соответственно вышеприведенным вычислениям
27 N2+7,15 СО2+0,08 SO2 + 0,01 NO2= 34,3 моля
Состав дымовых газов в объемных процентах будет соответствовать процентному соотношению молей каждого из них.
21 х 100 7,16 х 100
Так % N2 = ------------- = 79%; % СО2= ------------------ = 21%
34,3 34,3
0,08 х 100 0,07 х 100
% SO2= ------------------ = 0,24%; % NO2= -------------------- = 0,2%
34,3 34,3
Откуда % (масс): N2 = 10; СО2=29; SO2 =0,5; NO2 = 0,3
В реальном дымовом газе соотношение компонентов будет отличаться, кроме СО2, а также других оксидов азота и других газов. Вычисленные результаты относятся к сжиганию 100 кг угля соответственно мощности 1000 МВт, то есть на каждые 1000 Дж за секунду (280 кВтч). Для большей наглядности рассмотрим ситуацию, сложившуюся около мощной современной электростанции с установленной мощностью 3000 МВт.
За сутки, т.е. за 86400 с, выбросы составляют:
по СО2 3 х 315 х 8,04 х 104= 8127 х 104кг (81270 т);
по SO2 3 x 5 x 8,04 x 104= 129 x 104 кг (1290 т);
по NO2 3x 33 x 8,04 x 104= 86 x 104кг (860 т) и поглощение О2
3 х 233 х 6 х 8,04 х 104= 6027 х 104кг (60270 т)
При этом на станцию необходимо доставить угля 3 х 100 х 86400 = 24120000 кг (24120т) и вывезти шлака 3х 5,2 х 86400 = 2340000 кг (2340 т)
Под отвалы шлака и золы ( высотой до 10м) необходимо ежегодно отводить площадь до 3га. Ежесуточно такая станция вырабатывает электроэнергию 3000 х 106= 8,04 х 104= 25,8 х 103Дж, или 25,8 х 1013х 2,8 х 10 -7= 7224 х 106кВтч
Соответственно на тепловых электростанциях Украины при их нормальной загрузке выброс составляет 281,5 х 109х 1,12 = 315 х 109кг (315 млн. т), где 281,5 х 109максимальное годовое количество электроэнергии, вырабатываемой в Украине, кВт·ч.
В атмосфере оксиды серы и азота образуют с парами воды соответствующие кислоты, которые губительно действуют на растительность и фауну водоемов. Обычная дождевая вода, образующаяся при конденсации водяного пара в атмосфере, имела бы нейтральную реакцию (рН), но даже в чистом воздухе из-за наличия СО2, она приобретает значение РН-5,6...5,7.
Сегодня в промышленных регионах, где в атмосфере в значительной степени содержаться оксиды серы и азота, дождевая вода обычно имеет рН от 3 до 4. Уменьшение pН на единицу означает увеличение кислотности в 10 раз, на два – в 100 раз. Известны случаи выпадения дождей с рН около 2,5, т.е. кислотность равнялась уксусу. Озера и водоемы, содержащие воду с такой кислотностью, мертвы.
Ниже приведены уровни рН дождевой воды в сравнении с известными веществами.
| Вещество | Уровень рН |
| Лимонный сок | |
| Уксус | |
| Томатный сок | |
| Дождевая вода | 5,6 |
| Морская вода | |
3.3. Система технологий ГЭС
Движущей силой в гидроэлектростанции является поток речной воды, который приводит в действие гидротурбину, соединенную с электрогенератором.
Основное оборудование ГЭС:
1. Плотина для создания требуемого напора воды путем поднятия уровня с одной стороны и опускания – с другой.
2. Гидротурбина которая преобразует энергию падающей воды в механическую энергию вращения.
3. Гидрогенератор (электрогенератор), который механическую энергию преобразует в электрическую.
Основное энергетическое оборудование размещают в здании ГЭС:
- в машинном зале – гидроагрегаты, вспомогательное оборудование, устройства автоматического управления и контроля;
- на центральном посту управления – пульт оператора-диспетчера или автооператор ГЭС.
Энергетический источник беспрерывно возобновляется природой. Основные затраты при сооружении гидроэлектростанции составляют работы по сооружению плотины для обеспечения перепада воды. Чем выше плотина, тем больше потенциальная энергия воды на “входе” конверсии в кинетическую, которая превращается последовательно в механическую энергию турбины и электрическую на “выходе” из электрогенератора.
Коэффициент полезного действия конверсии энергии потока воды в электроэнергетическую несравненно выше, нежели в системах конверсии тепловых и атомных электростанций и составляют более 90%. Эти преимущества стимулируют строительство гидроэлектростанций во всем мире.
Пример.Плотина одной из самых больших гидроэлектростанций мира Саяно-Шушенской (на р. Енесей, Россия) обеспечивает напор воды L на турбину в 200т ( высота плотины 245м и длина 1060м) при расходе воды V за минуту 21400м3. Коэффициент конверсии энергии воды в электрическую h= 0,92. Определите мощность (Р) одного гидроэлектроагрегата и всей ГЭС ( 10 гидроэлектроагрегатов) и сравните мощность такого гидроэлектроагрегата с мощностью одного энергоблока РБМК-1000 Чернобыльской АЭС.
Решение.
А
Определяющее равенство мощности Р = ------ ,
t
где Р – энергия (работа), Дж; t – время, с
Энергия падающей воды (А) будет прямо пропорциональна напору и массе m, которая обуславливает силу F, действующую на лопасти гидротурбины.
F=mg,
где g – ускорение свободного падения на земную поверхность – 9,8 м/с2
Массу воды m, которая проходит через турбину за минуту, определим из уравнения:
m = rН2ОхV = 1000 кг/м3х21400 м3 = 21,4х106кг
Сила потока воды F= mg=21,4 х 106 кг х 9,8 м/с2 = 209,7 х 106 (кгм/с2) = 209,7 МН
Робота, которую выполняет поток за 1 минуту
А=F x L = 209,7 х 106 Н х 200м= 41,9 х 109ГДж.
Электрическая мощность одного гидроэлектрогенератора с учетом коэффициента конверсии h=0,92 составит:
41,9 х 109Дж х 0,92
––––––––––––––––– = 642 х 106Дж = 642 МДж
То есть мощность ГЭС (10 блоков) составляет 6,4 ГВт.
Мощность одного блока РБМК-1000 (1000МВт) больше, чем гидроэлектрогенератора, в 1,5 раза.
При строительстве и эксплуатации ГЭС много аспектов не было учтено. Прежде всего, это касается водохранилищ, которые заливают большие площади сельскохозяйственных угодий и лесов. На каждый киловатт мощности гидроэлектростанции затапливается около 300м2 земли.
В бассейнах рек равнинных регионов значительная часть площадей таких водохранилищ мелководна (до 2м), где создаются благоприятные условия для широкого размещения сине-зеленых водорослей. Опасность этого явления – насыщенность воды токсичными химическими соединениями (фенолом, индолом и др.), которые выделяются в процессе отмирания и разложения водорослей. Это явление наблюдается как “цветение” воды и особенно расширилось в различных регионах мира во второй половине ХХ столетия. Объясняют это тем, что в связи с применением на полях удобрений в мелководные площади водных бассейнов, которые хорошо прогреваются солнцем, с дождевыми потоками с почвы попадает большое количество питательных для водорослей элементов – азот, фосфор, калий. В таких водохранилищах исчезает рыба, а вода, прежде чем она поступает к потребителю, требует увеличения средств на ее очистку.
Кроме того, образование громадных водохранилищ изменяет микроклимат региона и часто не в лучшую сторону. Так образование глубокого (свыше 100м) Красноярского водохранилища на Енисее (Россия) повлекло снижение температуры воды летом более чем на 10ОС, а зимой, наоборот, в сорокаградусный мороз река окутана густым туманом, не замерзает на протяжении 300км вниз по течению. При сооружении этой ГЭС были затоплены ценнейшие сельскохозяйственные угодья края.
Но существует и другая сторона проблемы. Для мощных ГЭС в 2000...3000 МВт необходимы большие водные артерии, которые бы обеспечивали поток воды свыше 1000м3за секунду. Таких рек немного, а в Европе – совсем нет.
Перспективное направление в гидроэнергетике – гидроаккумулирующие электростанции (ГАЭС). Они включаются в региональную электросеть с другими электростанциями и выполняют роль демпфера –сами потребляют электроэнергию, когда она имеется в избытке, и возвращают ее в сеть, когда ее недостаточно. Электрические машины станции могут работать как насосы, когда перекачивают воду в верхнее водохранилище, и как блок гидротурбины с электрогенератором, когда она с верхнего водохранилища перетекает в нижнее. Такие станции позволяют не только рационально расходовать электроэнергию, не снижая ее производства всеми станциями электросети, но и обеспечивать использование воды из верхних водохранилищ для сельскохозяйственных угодий. Первая гидроаккумулирующая электростанция была сооружена в 1971 году на правом берегу Киевского водохранилища мощностью 225МВт с напором 65м, длиной водохранилища 275м. Нижним является Киевское водохранилище. После 1980г. построены еще две ГАЭС: Загорская (Московская область) на реке Кумья мощностью 1200 МВт и самая большая в Литве на р.Неман –1600 МВт. В 1999г. пущена в эксплуатацию ГАЭС на реке Днестр
3.4. Система технологий АЭС и проблемы радиационной защиты
Первый атомный реактор был построен в 1942 году в США под руководством итальянского ученого Е. Ферми, а на европейском континенте в бывшем СССР – в 1946 году под руководством И.В. Курчатова. Его мощность составляла 0,5 МВт (г. Обнинск вблизи Москвы). В Украине в эксплуатации находится 4 атомных электростанций: Ровенская, Хмельницкая, Южно-Украинская и Запорожская. (см. табл. 3.1). Атомная электростанция (АЭС)– сложное техническое сооружение, в котором атомная (ядерная) энергия преобразуется в электрическую.
В самом общем виде это происходит следующим образом (рис. 3.2). Тепло, которое выделяют, расщепляясь, ядра радиоактивных веществ (ядерное горючее – а сегодня это уран (изотопы нагревает прокачиваемый через активную зону реактора теплоноситель (жидкость /вода, содержащая 16% борной кислоты/ или газ), который отбирает тепло у ядерного горючего. Эта замкнутая система с теплоносителями называется первым контуром. В теплообменнике тепло первого контура нагревает до кипения воду второго контура. Образующийся пар идет в обычную турбину, вырабатывающую электричество, а также используется для обогрева зданий. Следовательно, атомные электростанции отличаются от других только способом превращения воды в пар (рис.3.3), который используется для производства электроэнергии.
Дата добавления: 2016-03-27; просмотров: 1406;
