ТРОФИЧЕСКАЯ ФУНКЦИЯ ДВИГАТЕЛЬНЫХ НЕРВНЫХ ВОЛОКОН И ИХ ОКОНЧАНИЙ
Наряду с функцией передачи импульсов, вызывающих мышечные сокращения, нервные волокна и их окончания оказывают также трофическое воздействие на мышцу, т. е. участвуют в регуляции ее обмена веществ. Хорошо известно, что денервация мышцы, развивающаяся при дегенерации двигательного нерва, приводит к атрофии мышечных волокон, которая проявляется в том, что вначале уменьшается количество саркоплазмы, а затем и диаметр мышечных волокон; позднее происходит разрушение миофибрилл. Специальные исследования показали, что эта атрофия не является результатом лишь бездеятельности мышцы, потерявшей двигательную активность. Бездеятельность мышцы может быть вызвана и путем тендотомии, т. е. перерезки сухожилия. Однако, если сравнить мышцу после тендотомии и после денервации, можно убедиться, что в последнем случае в мышце развиваются качественно иные изменения ее свойств, не обнаруживающиеся при тендотомии. Наиболее ярко это проявляется в изменениях чувствительности мышцы к ацетилхолину. В нормальной и тендотомированной мышце к ацетилхолину чувствительна только постсинаптическая мембрана, в которой сосредоточены хемовозбудимые ионные каналы, снабженные холинорецепторами. Денервация приводит к тому, что такие же каналы появляются и во внесинаптических областях мышечного волокна. В результате чувствительность денервированной мышцы к ацетилхолину резко возрастает. Указанная гиперчувствительность к ацетилхолину не формируется, если при помощи определенных химических реагентов затормозить белковый синтез в мышечных волокнах. Реиннервация мышцы вследствие регенерации нервных волокон приводит к исчезновению холинорецептивных каналов области внепостсинаптической мембраны. Эти данные свидетельствуют о том, что нервные волокна регулируют синтез белков, образующих хемовозбудимые холинорецепторные каналы.
В денервированной мышце резко падает также активность ряда ферментов, в частности АТФ-азы, играющей важную роль в процессе освобождения энергии, заключенной в фосфатных связях АТФ. В то же время при денервации значительно усилены процессы распада белков. Это приводит к характерному для атрофии постепенному уменьшению массы мышечной ткани.
Все дегенеративные изменения в денервированной мышце начинаются тем раньше, чем на меньшем расстоянии от мышцы перерезают двигательный нерв. Это позволяет предположить, что определенные вещества («трофические агенты»), вырабатываемые в нервных клетках, продвигаются по нервным волокнам от проксимальных участков к дистальным и выделяются нервными окончаниями. Чем больший отрезок нерва остается соединенным с мышцей, тем дольше она получает важные для ее обмена вещества. Перемещение этих веществ осуществляется благодаря движению нейроплазмы, скорость которого 1—2 мм/ч.
Важную роль в осуществлении трофических влияний нерва играет ацетилхолин, секретируемый нервными окончаниями как в покое, так особенно при возбуждении. Имеются основания считать, что ацетилхолин и продукты его расщепления холинэстеразой — холин и уксусная кислота — участвуют в обмене веществ мышцы, оказывая активирующее влияние на определенные ферментные системы. Так, при введении ацетилхолина в денервированную мышцу кролика резко увеличивается распад аденозинтрифосфата, креатинфосфата и гликогена во время тетануса, вызванного прямым электрическим раздражением этой мышцы.
Из нервных окончаний выделяются вещества, которые оказывают специфическое влияние на синтез белков мышечного волокна. Об этом свидетельствуют опыты с перекрестным сшиванием двигательных нервов, иннервирующих быстрые и медленные скелетные мышцы. При таком сшивании периферические отрезки нервов и их окончания в мышце дегенерируют, а по их путям в мышцу прорастают новые волокна из центральных отрезков нервов. Вскоре после того, как эти волокна образуют двигательные окончания, происходит отчетливая перестройка функциональных свойств мышц. Мышцы, которые ранее были быстрыми, теперь становятся медленными, а те, которые были медленными, становятся быстрыми. При такой перестройке изменяется активность АТФ-азы их сократительного белка миозина: в бывших быстрых мышцах она резко падает, а в медленных возрастает. Соответственно в первых скорость распада АТФ увеличивается, а во вторых — уменьшается. Изменяются также свойства ионных каналов клеточной мембраны.
Трофическое влияние на скелетную мышцу оказывают и волокна симпатической нервной системы, окончания которых высвобождают норадреналин.
ОСОБЕННОСТИ НЕРВНО-МЫШЕЧНОЙ ПЕРЕДАЧИ ВОЗБУЖДЕНИЯ В ГЛАДКИХ МЫШЦАХ
Механизм передачи возбуждения с двигательного нервного волокна на волокна гладкой мышцы в принципе сходен с механизмом нервно-мышечной передачи в скелетной мускулатуре. Различия касаются лишь химической природы медиатора и особенностей суммации постсинаптических потенциалов.
Во всех скелетных мышцах возбуждающим медиатором является ацетилхолин. В гладких мышцах передача возбуждения в нервных окончаниях осуществляется при помощи разных медиаторов. Так, для гладких мышц желудочно-кишечного тракта возбуждающим медиатором является ацетилхолин, а для гладких мышц кровеносных сосудов — норадреналин.
Порция медиатора, высвобождаемая нервным окончанием в ответ на одиночный нервный импульс, в большинстве случаев оказывается недостаточной для критической деполяризации мембраны гладкомышечной клетки. Критическая деполяризация происходит только при поступлении к нервному окончанию нескольких следующих друг за другом импульсов. Тогда одиночные возбуждающие постсинаптические потенциалы суммируются (рис. 57) и в момент, когда их сумма достигает пороговой величины, возникает потенциал действия.
В скелетном мышечном волокне частота следования потенциалов действия соответствует частоте ритмического раздражения двигательного нерва. В отличие от этого в гладких мышцах такое соответствие нарушается уже при частотах 7—15 имп/с. Если же частота стимуляции превышает 50 имп/с, возникает торможение типа пессимального.
Тормозные синапсы в гладких мышцах. Раздражение некоторых нервных волокон, иннервирующих гладкие мышцы, может вызывать их торможение, а не возбуждение. Нервные импульсы, приходящие в определенные нервные окончания, высвобождают тормозной медиатор.
Воздействуя на постсинаптическую мембрану, тормозной медиатор взаимодействует с хемовозбудимыми каналами, обладающими преимущественной проницаемостью для ионов К+. Выходящий поток калия через эти каналы вызывает гиперполяризацию постсинаптической мембраны, проявляющуюся в форме «тормозного постсинаптического потенциала», подобного тому, который наблюдается в тормозных синапсах нейронов в ЦНС.
При ритмическом раздражении тормозных нервных волокон тормозные постсинаптические потенциалы суммируются друг с другом, причем эта суммация оказывается наиболее эффективной в диапазоне частот 5—25 имп/с (рис. 58).
Если раздражение тормозящего нерва несколько предшествует стимуляции активирующего нерва, то возбуждающий постсинаптический потенциал, вызываемый по-
 Рис.57. Суммация постсинаптических потенциалов в гладкомышечных волокнах морской свинки.
Рис.57. Суммация постсинаптических потенциалов в гладкомышечных волокнах морской свинки.
|
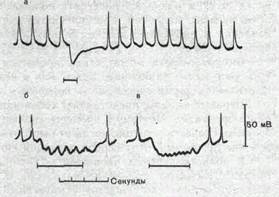 Рис. 58. Тормозные постсинаптические потенциалы в гладкомышечном волокне кишки морской свинки.
а — тормозный потенциал, вызванный одиночным раздражением интрамурального тормозного нерва; бив — сум-мация тормозных потенциалов при ритмическом раздражении этого нерва. Частота раздражении 2 в секунду (б) и 4 в секунду (в). Горизонтальная линия— период раздражения.
Рис. 58. Тормозные постсинаптические потенциалы в гладкомышечном волокне кишки морской свинки.
а — тормозный потенциал, вызванный одиночным раздражением интрамурального тормозного нерва; бив — сум-мация тормозных потенциалов при ритмическом раздражении этого нерва. Частота раздражении 2 в секунду (б) и 4 в секунду (в). Горизонтальная линия— период раздражения.
|
следним, ослабляется и может оказаться недостаточным для критической деполяризации мембраны. Раздражение тормозного нерва на фоне спонтанной активности мышцы угнетает генерацию потенциалов действия и, следовательно, приводит к прекращению ее сокращений.
Роль тормозного медиатора в гладких мышцах, возбуждаемых ацетилхолином (например, кишечника, бронхов), исполняет норадреналин. Наоборот, в мышечных клетках сфинктера мочевого пузыря и некоторых других гладких мышцах, для которых возбуждающим медиатором является норадреналин, тормозным медиатором служит ацетилхолин. Последний оказывает тормозящее действие и на клетки водителя ритма сердца.
В скелетных мышцах нервно-мышечная передача, осуществляемая при помощи ацетилхолина, блокируется препаратами кураре, обладающими большим сродством к холинорецепторам. В гладких мышцах холинорецептор имеет иную химическую структуру, чем в скелетных, поэтому она блокируется не препаратами кураре, а атропином.
В тех гладких мышцах, в которых медиатором служит норадреналин, хемовозбудимые каналы снабжены адренорецепторами. Различают два основных вида адренорецепторов: а-адренорецепторы. и (b-адренорецепторы, которые блокируются различными химическими соединениями — адреноблокаторами.
ЗАКЛЮЧЕНИЕ
К возбудимым тканям кроме нервной и мышечной относится и железистая ткань, но механизмы возбуждения клеток желез внешней секреции несколько отличны от таковых у нервных и мышечных.
Как показали микроэлектродные исследования мембрана секреторных клеток в состоянии покоя является поляризованной, причем наружная поверхность ее заряжена положительно, а внутренняя — отрицательно. Разность потенциалов составляет 30— 40 мв. При стимуляции секреторных нервов, иннервирующих железу, возникает не деполяризация, а гиперполяризация мембраны и разность потенциалов достигает 50—60 мв. Предполагают, что это происходит вследствие нагнетания С1~ и других отрицательных ионов в клетку. Под влиянием электростатических сил в клетку вслед за этим начинают поступать положительные ионы, что приводит к повышению осмотического давления, поступлению в клетку воды, увеличению гидростатического давления и набуханию клетки. В результате возникает выброс секрета из клетки в просвет железы.
Выброс секрета может стимулироваться не только нервными, но и химическими (гуморальными) влияниями. Здесь, как и везде в организме, регуляция функций осуществляется двумя способами — нервным и гуморальным.
Нервный импульс представляет собой наиболее быстрый способ передачи информации в организме. Поэтому в процессе эволюции в тех случаях, когда была необходима большая скорость реакций, когда от быстроты ответных реакций зависело само существование организма, этот способ передачи сигналов стал основным.
В области нервных окончаний — в синаптических щелях нервный импульс, как правило, вызывает выделение медиатора и, таким образом, взаимодействие между клетками остается по существу химическим. При этом вместо медленного распространения химического вещества с током жидкости (с движущейся кровью, лимфой, тканевой жидкостью и т. д.) в нервной системе с большой скоростью распространяется сигнал к выделению биологически активного вещества (медиатора) в области нервных окончаний (на месте). Все это резко повысило быстроту ответных реакций организма, сохранив по существу принцип химического взаимодействия между клетками. Вместе с тем в ряде случаев, когда при клеточном взаимодействии необходима еще более быстрая и притом всегда однозначная реакция, межклеточная передача сигнала обеспечивается прямым электрическим взаимодействием клеток. Такой тип связи наблюдается, например, при взаимодействии клеток миокарда, а также некоторых электрических синапсов ЦНС, получивших название эфапсов.
Межклеточные связи сводятся не только к электрическим взаимодействиям или влияниям медиаторов. Химическая взаимосвязь между клетками является более сложной. Клетки органов и тканей вырабатывают ряд специфических химических веществ, действующих на другие клетки и вызывающих не только включение и выключение (или усиление или ослабление) функции, но и изменение интенсивности обмена веществ и процессов синтеза клеткой специфических белков. Механизмы всех этих рефлекторных влияний и межклеточных взаимодействий подробно рассмотрены во втором разделе учебника.
Дата добавления: 2016-03-27; просмотров: 3187;
