Гормональная регуляция как механизм межклеточной и межорганной координации обмена веществ. Клетки-мишени и клеточные рецепторы гормонов. Гормоны гипоталамуса: либерины и статины.
| Краткое содержание | Конспект | ||||||
| 1. Гормональная регуляция как механизм межклеточной и межорганной координации обмена веществ. Клетки-мишени и клеточные рецепторы гормонов. Гормоны гипоталамуса: либерины и статины | |||||||
Учение о гормонах выделено в самостоятельную науку – эндокринологию. Современная эндокринология изучает химическую структуру гормонов, образующихся в железах внутренней секреции, зависимость между структурой и функцией гормонов, молекулярные механизмы действия, а также физиологию и патологию эндокринной системы.
Основные системы регуляции метаболизма и межклеточной коммуникации
1. Центральная и периферическая нервные системы.
2. Эндокринная система через эндокринные железы и гормоны, которые секретируются в кровь и влияют на метаболизм различных клеток-мишеней.
3. Паракринная и аутокринная системы посредством различных соединений, которые секретируются в межклеточное пространство и взаимодействуют с рецепторами либо близлежащих клеток, либо той же клетки (простагландины, гормоны ЖКТ, гистамин и др.).
4. Иммунная система через специфические белки (цитокины, антитела).
3 иерархических уровня системы регуляции обмена веществ и функций организма:
Первый уровень –ЦНС.
Второй уровень –эндокринная система.
Третий уровень –внутриклеточный.
Базальный (нестимулированный) уровень гормонов в крови – в пределах 10-6-10-12 М.
Схема взаимосвязи регуляторных систем организма:
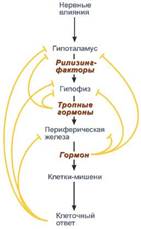 Существуют эндокринные железы, для которых отсутствуетрегуляция тропными гормонами – паращитовиднаяжелеза, мозговое вещество надпочечников, ренин-альдостероновая система и поджелудочнаяжелеза. Они контролируются нервными влияниями или концентрацией определенных веществ в крови.
Системы регуляции метаболизма:
Существуют эндокринные железы, для которых отсутствуетрегуляция тропными гормонами – паращитовиднаяжелеза, мозговое вещество надпочечников, ренин-альдостероновая система и поджелудочнаяжелеза. Они контролируются нервными влияниями или концентрацией определенных веществ в крови.
Системы регуляции метаболизма:
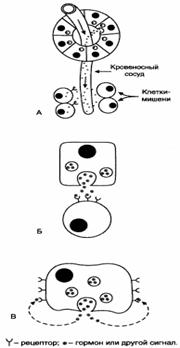 Физиологический эффект гормона:
• концентрацией гормона;
• сродством гормонов к белкам-переносчикам;
• количеством рецепторов на поверхности клеток-мишеней;
• типом рецепторов на поверхности клеток-мишеней.
Эволюционно сформировались два основных механизма действия сигнальных молекул в зависимости от локализации рецептора:
1. Мембранный– рецептор расположен на мембране. По данному механизму работают пептидные и белковые гормоны, катехоламины, эйкозаноиды.
2. Цитозольный– рецептор расположен в цитозоле.
Гормоны, связывающиеся с рецепторами на поверхности клетки:
Физиологический эффект гормона:
• концентрацией гормона;
• сродством гормонов к белкам-переносчикам;
• количеством рецепторов на поверхности клеток-мишеней;
• типом рецепторов на поверхности клеток-мишеней.
Эволюционно сформировались два основных механизма действия сигнальных молекул в зависимости от локализации рецептора:
1. Мембранный– рецептор расположен на мембране. По данному механизму работают пептидные и белковые гормоны, катехоламины, эйкозаноиды.
2. Цитозольный– рецептор расположен в цитозоле.
Гормоны, связывающиеся с рецепторами на поверхности клетки:
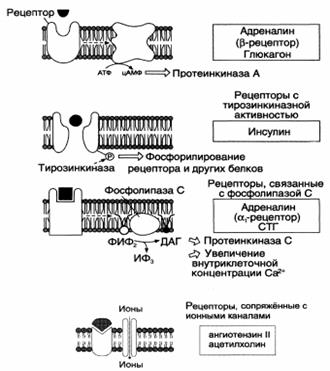 Гормоны, связывающиеся с внутриклеточными рецепторами:
Эстрогены, глюкокортикоиды, минералокортикоиды, прогестины, кальцитриол (1,25 [ОН]2-D3), андрогены, тиреоидные гормоны (Т3 и Т4).
Передача гормональных сигналов через внутриклеточные рецепторы:
Гормоны, связывающиеся с внутриклеточными рецепторами:
Эстрогены, глюкокортикоиды, минералокортикоиды, прогестины, кальцитриол (1,25 [ОН]2-D3), андрогены, тиреоидные гормоны (Т3 и Т4).
Передача гормональных сигналов через внутриклеточные рецепторы:
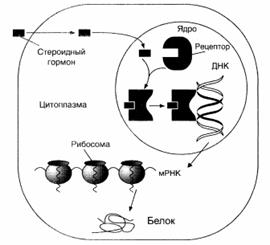 Гормоны гипоталамуса
К настоящему времени в гипоталамусе открыто 7 стимуляторов (либерины) и 3 ингибитора (статины) секреции гормонов гипофиза, а именно: кортиколиберин, тиролиберин, люлиберин, фолликулолиберин, соматолиберин, пролактолиберин, меланолиберин, соматостатин, пролактостатин и меланостатин. По химическому строению все гормоны гипоталамуса являются низкомолекулярными пептидами.
Строение и функции гормонов гипоталамуса:
Гормоны гипоталамуса
К настоящему времени в гипоталамусе открыто 7 стимуляторов (либерины) и 3 ингибитора (статины) секреции гормонов гипофиза, а именно: кортиколиберин, тиролиберин, люлиберин, фолликулолиберин, соматолиберин, пролактолиберин, меланолиберин, соматостатин, пролактостатин и меланостатин. По химическому строению все гормоны гипоталамуса являются низкомолекулярными пептидами.
Строение и функции гормонов гипоталамуса:
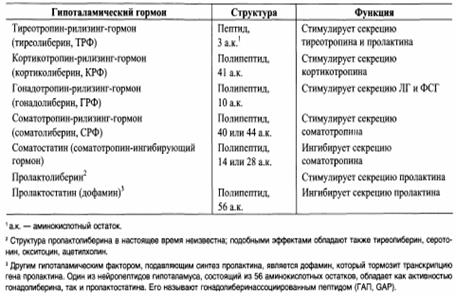 Тиролиберин
Пиро-Глу–Гис–Про–NH2
Гонадолиберин
Пиро-Глу–Гис–Трп–Сер–Тир–Гли–Лей–Арг–Про–Гли-NН2
Соматостатин
Тиролиберин
Пиро-Глу–Гис–Про–NH2
Гонадолиберин
Пиро-Глу–Гис–Трп–Сер–Тир–Гли–Лей–Арг–Про–Гли-NН2
Соматостатин
 Соматолиберин
Н-Вал–Гис–Лей–Сер–Ала–Глу–Глн–Лиз–Глу–Ала-ОН
Меланолиберин
Н-Цис–Тир–Иле–Глн–Асн–Цис-ОН
Меланостатин
Пиро-Глу–Гис–Фен–Aрг–Гли–NН2
Местом синтеза гипоталамических гормонов, вероятнее всего, являются нервные окончания – синаптосомы гипоталамуса, поскольку именно там отмечена наибольшая концентрация гормонов и биогенных аминов.
Соматолиберин
Н-Вал–Гис–Лей–Сер–Ала–Глу–Глн–Лиз–Глу–Ала-ОН
Меланолиберин
Н-Цис–Тир–Иле–Глн–Асн–Цис-ОН
Меланостатин
Пиро-Глу–Гис–Фен–Aрг–Гли–NН2
Местом синтеза гипоталамических гормонов, вероятнее всего, являются нервные окончания – синаптосомы гипоталамуса, поскольку именно там отмечена наибольшая концентрация гормонов и биогенных аминов.
| Зарождение науки об эндокринных железах и гормонах относится к 1855 г., когда Т. Аддисон впервые описал бронзовую болезнь, связанную с поражением надпочечников и сопровождающуюся специфической пигментацией кожных покровов. Клод Бернар ввел понятие о железах внутренней секреции, т.е. органах, выделяющих секрет непосредственно в кровь. Позже Ш. Броун-Секар показал, что недостаточность функции желез внутренней секреции вызывает развитие болезней, а экстракты, полученные из этих желез, оказывают хороший лечебный эффект.
Общие свойства гормонов:
- существует 3 класса гормонов (пептидные, стероидные, амины);
- некоторые полипептидные гормоны образуются из неактивных предшественников;
- гормоны действуют в очень низких концентрациях и в большинстве случаев имеют короткое время жизни;
- одни гормоны действуют быстро, другие – медленно;
- гормоны связываются со специфическими рецепторами, расположенными либо на поверхности, либо внутри клетки-мишени;
- действие гормонов может осуществляться через вторичные передатчики (посредники).
Все 75 триллионов клеток, содержащихся в организме человека, служат мишенями одного или нескольких из 50 известных гормонов. Мишенью гормона может быть одна ткань или же несколько тканей. В соответствии с классическим определением ткань-мишень – это такая ткань, в которой гормон вызывает специфическую биохимическую или физиологическую реакцию.
Основные эндокринные системы и их ткани-мишени:
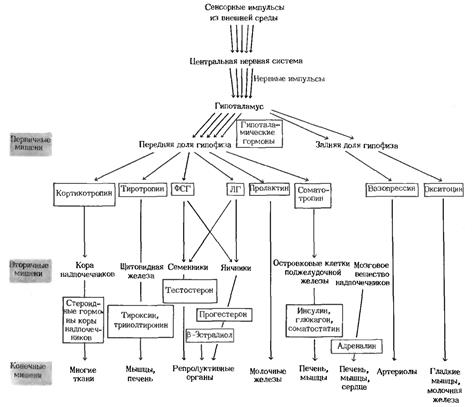 Обозначить системы регуляции метаболизма:
… - аутокринная система.
… - эндокринная система.
… - паракринная система.
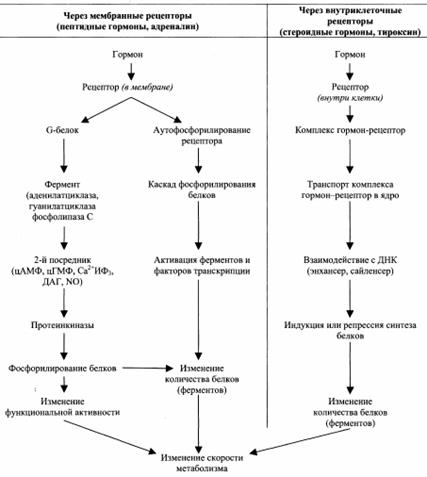
Классификация гормонов организма человека:
Обозначить системы регуляции метаболизма:
… - аутокринная система.
… - эндокринная система.
… - паракринная система.
Классификация гормонов организма человека:
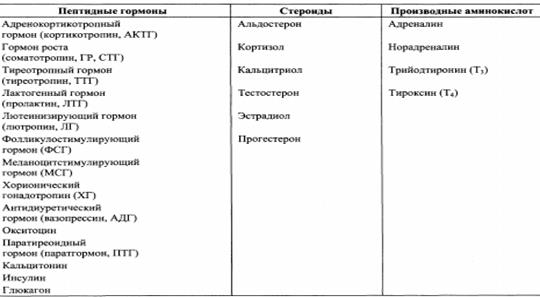 Пример системы регуляции по типу отрицательной обратной связи Такая система регулирует функцию щитовидной железы, надпочечников, яичников и семенников
Пример системы регуляции по типу отрицательной обратной связи Такая система регулирует функцию щитовидной железы, надпочечников, яичников и семенников
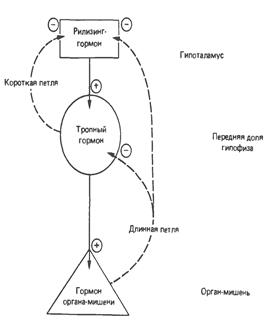 Основные этапы передачи гормональных сигналов и результат их действия:
Основные этапы передачи гормональных сигналов и результат их действия:
| ||||||
| 2. Гормоны гипофиза. ПОМК как предшественник АКТГ, b-липотропина, эндорфинов. Строение и биологическая роль вазопрессина и окситоцина. Йодсодержащие гормоны, строение и биосинтез. Изменение обмена веществ при гипертиреозе и гипотиреозе. Регуляция фосфорно-кальциевого обмена, участие паратгормона и кальцитонина, активных форм витамина D. | |||||||
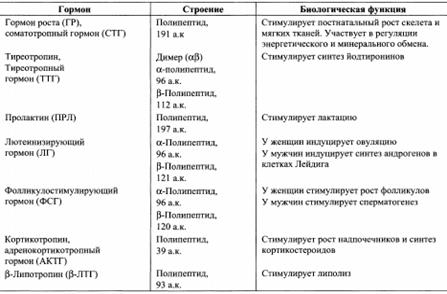
В зависимости от места синтеза различают гормоны передней, задней и промежуточной долей гипофиза. В передней доле вырабатываются в основном белковые и полипептидные гормоны, называемые тропными гормонами, или тропинами, вследствие их стимулирующего действия на ряд других эндокринных желез.
Строение и биологические функции гормонов передней доли гипофиза:
 Семейство пептидов проопиомеланокортина (ПОМК)
Это семейство состоит из пептидов, действующих либо как гормоны (адренокортикотропин, липотропин, меланоцит-стимулирующий гормон), либо как нейромедиаторы или нейромодуляторы. Проопиомеланокортин (ПОМК) синтезируется в виде молекулы предшественника, состоящей примерно из 285 аминокислотных остатков, и подвергается различному процессингу в разных отделах гипофиза.
Процессинг белка ПОМК в периферических тканях (кишечник, плацента, мужской половой тракт) сходен с таковым в промежуточной доле гипофиза. Существуют три основные группы пептидов семейства ПОМК:
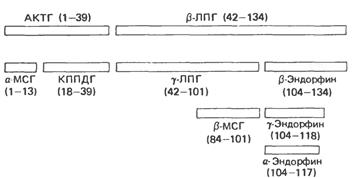
1) АКТГ, из которого могут образовываться меланоцит-стимулирующий гормон (α-МСГ) и кортикотропиноподобный пептид промежуточной доли;
2) β–-липотропин (β–ЛПГ), служащий предшественником α-липотропина, β-МСГ и β-эндорфина и. следовательно, α- и γ-эндорфинов;
3) большой N-концевой пептид, из которого образуетсяγ-МСГ.
Следующее расщепление продуктов ПОМК в передней и промежуточной доле гипофиза происходит на участке между АКТГ и β-ЛПГ, что приводит к отделению N-концевого пептида, включающего АКТГ, от Р-ЛПГ.
АКТГ1-39 затем отделяется от N-концевого пептида, дальнейших расщеплений в передней доле гипофиза практически не происходит. В промежуточной доле АКТГ1-39 расщепляется на α-МСГ (остатки 1-13) и кортикотропиноподобный пептид 18-39); β-липотропин 42-134) превращается в γ-липотропин 42-101) и β-эндорфин 104-134); β-МСГ (84-101) образуется из γ-липотропина.
Перечисленные пептиды претерпевают множество дополнительных модификаций. Большая часть N-концевого пептида и АКТГ1-39 находится в передней доле гипофиза в гликозилированном состоянии, α-МСГ обнаруживается преимущественно в N-ацетилированной и амидированной с С-конца форме; деацетилированный α-МСГ намного менее активен.
β-Эндорфин в промежуточной доле быстро ацетилируется; ацетилированный β-эндорфин в противоположность α-МСГ обладает в 1000 раз меньшей активностью, чем немодифицированная форма. Таким образом, β-эндорфин может находиться в гипофизе в неактивном состоянии. В гипоталамусе молекулы этого пептида не ацетилированы и, по-видимому, присутствуют в активной форме. β-Эндорфин подвергается также укорочению с С-конца с образованием λ- и γ-эндорфинов.
Функции большинства пептидов семейства ПОМК точно не установлены. Постулированные для них эффекты перечислены в табл.
Функции пептидов ПОМК
Семейство пептидов проопиомеланокортина (ПОМК)
Это семейство состоит из пептидов, действующих либо как гормоны (адренокортикотропин, липотропин, меланоцит-стимулирующий гормон), либо как нейромедиаторы или нейромодуляторы. Проопиомеланокортин (ПОМК) синтезируется в виде молекулы предшественника, состоящей примерно из 285 аминокислотных остатков, и подвергается различному процессингу в разных отделах гипофиза.
Процессинг белка ПОМК в периферических тканях (кишечник, плацента, мужской половой тракт) сходен с таковым в промежуточной доле гипофиза. Существуют три основные группы пептидов семейства ПОМК:
1) АКТГ, из которого могут образовываться меланоцит-стимулирующий гормон (α-МСГ) и кортикотропиноподобный пептид промежуточной доли;
2) β–-липотропин (β–ЛПГ), служащий предшественником α-липотропина, β-МСГ и β-эндорфина и. следовательно, α- и γ-эндорфинов;
3) большой N-концевой пептид, из которого образуетсяγ-МСГ.
Следующее расщепление продуктов ПОМК в передней и промежуточной доле гипофиза происходит на участке между АКТГ и β-ЛПГ, что приводит к отделению N-концевого пептида, включающего АКТГ, от Р-ЛПГ.
АКТГ1-39 затем отделяется от N-концевого пептида, дальнейших расщеплений в передней доле гипофиза практически не происходит. В промежуточной доле АКТГ1-39 расщепляется на α-МСГ (остатки 1-13) и кортикотропиноподобный пептид 18-39); β-липотропин 42-134) превращается в γ-липотропин 42-101) и β-эндорфин 104-134); β-МСГ (84-101) образуется из γ-липотропина.
Перечисленные пептиды претерпевают множество дополнительных модификаций. Большая часть N-концевого пептида и АКТГ1-39 находится в передней доле гипофиза в гликозилированном состоянии, α-МСГ обнаруживается преимущественно в N-ацетилированной и амидированной с С-конца форме; деацетилированный α-МСГ намного менее активен.
β-Эндорфин в промежуточной доле быстро ацетилируется; ацетилированный β-эндорфин в противоположность α-МСГ обладает в 1000 раз меньшей активностью, чем немодифицированная форма. Таким образом, β-эндорфин может находиться в гипофизе в неактивном состоянии. В гипоталамусе молекулы этого пептида не ацетилированы и, по-видимому, присутствуют в активной форме. β-Эндорфин подвергается также укорочению с С-конца с образованием λ- и γ-эндорфинов.
Функции большинства пептидов семейства ПОМК точно не установлены. Постулированные для них эффекты перечислены в табл.
Функции пептидов ПОМК
 Гормоны задней доли гипофиза:
вазопрессин(антидиуретический гормон - АДГ), окситоцин.
Оба гормона представляют собой нонапептиды следующего строения:
Гормоны задней доли гипофиза:
вазопрессин(антидиуретический гормон - АДГ), окситоцин.
Оба гормона представляют собой нонапептиды следующего строения:
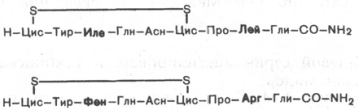 Основной биологический эффект окситоцина у млекопитающих связан со стимуляцией сокращения гладких мышц матки при родах и мышечных волокон вокруг альвеол молочных желез, что вызывает секрецию молока.
Вазопрессин стимулирует сокращение гладких мышечных волокон сосудов, оказывая сильное вазопрессорное действие, однако основная роль его в организме сводится к регуляции водного обмена, откуда его второе название антидиуретического гормона. В небольших концентрациях (0,2 нг на 1 кг массы тела) вазопрессин оказывает мощное антидиуретическое действие – стимулирует обратный ток воды через мембраны почечных канальцев. В норме он контролирует осмотическое давление плазмы крови и водный баланс организма человека. При патологии, в частности атрофии задней доли гипофиза, развивается несахарный диабет – заболевание, характеризующееся выделением чрезвычайно больших количеств жидкости с мочой. При этом нарушен обратный процесс всасывания воды в канальцах почек.
Соматотропный гормон (СТГ)
СТГ синтезируется в ацидофильных клетках передней доли гипофиза; концентрация его в гипофизе составляет 5–15 мг на 1 г ткани, что в 1000 раз превышает концентрацию других гормонов гипофиза. К настоящему времени полностью выяснена первичная структура белковой молекулы СТГ человека, быка и овцы. СТГ человека состоит из 191 аминокислоты и содержит две дисульфидные связи; N- и С-концевые аминокислоты представлены фенилаланином.
СТГ обладает широким спектром биологического действия. Он влияет на все клетки организма, определяя интенсивность обмена углеводов, белков, липидов и минеральных веществ. Он усиливает биосинтез белка, ДНК, РНК и гликогена и в то же время способствует мобилизации жиров из депо и распаду высших жирных кислот и глюкозы в тканях. Помимо активации процессов ассимиляции, сопровождающихся увеличением размеров тела, ростом скелета, СТГ координирует и регулирует скорость протекания обменных процессов. Кроме того, СТГ человека и приматов (но не других животных) обладает измеримой лактогенной активностью.
Патологическая биохимия
Гипофункция -при уменьшении выработки и снижении концентрации в крови возникает гипофизарный нанизм (карликовость), частота в России около 1:20000. Проявляется на 2-4 году жизни, критерием служит снижение скорости роста до 4 см в год и менее; при нарушении синтеза у взрослых отмечается снижение мышечной массы и тенденция к гипогликемии; при нарушении рецепции или пострецепторной передачи сигнала происходит пропорциональное, но недостаточное развитие тела. Примером могут служить пигмеи, племена Центральной Африки.
Гиперфункция -у детей возникает гигантизм, так как еще нет зарастания эпифизарных щелей и возможен ускоренный рост кости; у взрослых развивается акромегалия – из-за акрального роста кости происходит увеличение размера носа, стопы, кистей, челюсти.
Адренокортикотропный гормон (АКТГ)
АКТГ вырабатывается базофильными клетками аденогипофиза. АКТГ, помимо основного действия – стимуляции синтеза и секреции гормонов коры надпочечников, обладает жиромобилизующей и меланоцитстимулирующей активностью.
Молекула АКТГ у всех видов животных содержит 39 аминокислотных остатков.
Патологическая биохимия
В результате избыточного образования АКТГ гипофизом или его эктопического образования опухолью развивается синдром Кушинга.Слабое МСГ-подобное действие АКТГ, а также секреция β- или α-МСГ приводят к повышенной пигментации кожи. Возникающие метаболические нарушения обусловлены гиперпродукцией стероидов надпочечников, к ним относятся: 1) отрицательный азотный, калиевый и фосфорный баланс; 2) задержка натрия, которая может привести к повышению артериального давления и отекам; 3) нарушение толерантности к глюкозе или сахарный диабет; 4) повышение содержания жирных кислот в плазме; 5) уменьшение количества эозинофилов и лимфоцитов в крови при увеличении количества полиморфноядерных лейкоцитов. У больных с синдромом Кушинга может наблюдаться атрофия мышц и специфическое перераспределение жира с его отложением на туловище. Отсутствие АКТГ, связанное с опухолью, инфекцией или инфарктом гипофиза, вызывает противоположные сдвиги.
Тиреотропный гормон (ТТГ, тиротропин)
Тиротропин является сложным гликопротеином и содержит, кроме того, по две α- и β-субъединицы, которые в отдельности биологической активностью не обладают: мол. масса его около 30000.
Тиротропин контролирует развитие и функцию щитовидной железы и регулирует биосинтез и секрецию в кровь тиреоидных гормонов.
Предполагают, что действие тиротропина осуществляется, подобно действию других гормонов белковой природы, посредством связывания со специфическими рецепторами плазматических мембран и активирования аденилатциклазной системы.
Липотропные гормоны (ЛТГ, липотропины)
Среди гормонов передней доли гипофиза, структура и функция которых выяснены в последнее десятилетие, следует отметить липотропины, в частности β- и γ-ЛТГ.
К биологическим свойствам β-липотропина относятся жиромобилизующее действие, кортикотропная, меланоцитстимулирующая и гипокальциемическая активность и, кроме того, инсулиноподобный эффект, выражающийся в повышении скорости утилизации глюкозы в тканях.
Среди гормонов передней доли гипофиза, структура и функция которых выяснены в последнее десятилетие, следует отметить липотропины, в частности β- и γ-ЛТГ.
К биологическим свойствам β-липотропина относятся жиромобилизующее действие, кортикотропная, меланоцитстимулирующая и гипокальциемическая активность и, кроме того, инсулиноподобный эффект, выражающийся в повышении скорости утилизации глюкозы в тканях.
Перечисленные биологические свойства обусловлены не β-липотропином, оказавшимся лишенным гормональной активности, а продуктами его распада, образующимися при ограниченном протеолизе. Оказалось, что в ткани мозга и в промежуточной доле гипофиза синтезируются биологически активные пептиды, наделенные опиатоподобным действием.
Структуры некоторых из них приведены ниже:
Н–Тир–Гли–Гли–Фен–Мет–ОН
Метионин-энкефалин
Н–Тир–Гли–Гли–Фен–Лей–ОН
Лейцин-энкефалин
Н–Тир–Гли–Гли–Фен–Мет–Тре–Сер–Глу–Лиз–Сер–Глн–Тре–Про–
Лей–Вал–Тре–Лей–Фен–Лиз–Асн–Ала–Иле–Вал–Лиз–Асн–Ала–Гис–
–Лиз–Лиз–Гли–Глн–ОН
β-Эндорфин
Лактотропный гормон (пролактин, лютеотропный гормон)
Пролактин считается одним из наиболее «древних» гормонов гипофиза. Помимо основного действия (стимуляция развития молочных желез и лактации), пролактин имеет важное биологическое значение – стимулирует рост внутренних органов, секрецию желтого тела (отсюда его второе название «лютеотропный гормон»), оказывает ренотропное, эритропоэтическое и гипергликемическое действие и др. Избыток пролактина, образующийся обычно при наличии опухолей из секретирующих пролактин клеток, приводит к прекращению менструаций (аменорея) и увеличению молочных желез у женщин и к импотенции – у мужчин.
Расшифрована структура пролактина из гипофиза овцы, быка и человека. Это крупный белок, представленный одной полипептидной цепью с тремя дисульфидными связями, состоящий из 199 аминокислотных остатков. Видовые отличия в последовательности аминокислот касаются по существу 2–3 аминокислотных остатков.
В крови женщин уровень пролактина резко повышается перед родами: до 0,2 нг/л против 0,01 нг/л в норме.
Гормоны щитовидной железы
Щитовидная железа состоит из множества особых полостей – фолликулов, заполненных вязким секретом – коллоидом.
В состав коллоида входит особый йодсодержащий гликопротеин с высокой мол. массой – порядка 650000 (5000 аминокислотных остатков). Этот гликопротеин получил название йодтиреоглобулина. Он представляет собой запасную форму тироксина и трийодтиронина – основных гормонов фолликулярной части щитовидной железы.
Структура гормонов щитовидной железы:
Основной биологический эффект окситоцина у млекопитающих связан со стимуляцией сокращения гладких мышц матки при родах и мышечных волокон вокруг альвеол молочных желез, что вызывает секрецию молока.
Вазопрессин стимулирует сокращение гладких мышечных волокон сосудов, оказывая сильное вазопрессорное действие, однако основная роль его в организме сводится к регуляции водного обмена, откуда его второе название антидиуретического гормона. В небольших концентрациях (0,2 нг на 1 кг массы тела) вазопрессин оказывает мощное антидиуретическое действие – стимулирует обратный ток воды через мембраны почечных канальцев. В норме он контролирует осмотическое давление плазмы крови и водный баланс организма человека. При патологии, в частности атрофии задней доли гипофиза, развивается несахарный диабет – заболевание, характеризующееся выделением чрезвычайно больших количеств жидкости с мочой. При этом нарушен обратный процесс всасывания воды в канальцах почек.
Соматотропный гормон (СТГ)
СТГ синтезируется в ацидофильных клетках передней доли гипофиза; концентрация его в гипофизе составляет 5–15 мг на 1 г ткани, что в 1000 раз превышает концентрацию других гормонов гипофиза. К настоящему времени полностью выяснена первичная структура белковой молекулы СТГ человека, быка и овцы. СТГ человека состоит из 191 аминокислоты и содержит две дисульфидные связи; N- и С-концевые аминокислоты представлены фенилаланином.
СТГ обладает широким спектром биологического действия. Он влияет на все клетки организма, определяя интенсивность обмена углеводов, белков, липидов и минеральных веществ. Он усиливает биосинтез белка, ДНК, РНК и гликогена и в то же время способствует мобилизации жиров из депо и распаду высших жирных кислот и глюкозы в тканях. Помимо активации процессов ассимиляции, сопровождающихся увеличением размеров тела, ростом скелета, СТГ координирует и регулирует скорость протекания обменных процессов. Кроме того, СТГ человека и приматов (но не других животных) обладает измеримой лактогенной активностью.
Патологическая биохимия
Гипофункция -при уменьшении выработки и снижении концентрации в крови возникает гипофизарный нанизм (карликовость), частота в России около 1:20000. Проявляется на 2-4 году жизни, критерием служит снижение скорости роста до 4 см в год и менее; при нарушении синтеза у взрослых отмечается снижение мышечной массы и тенденция к гипогликемии; при нарушении рецепции или пострецепторной передачи сигнала происходит пропорциональное, но недостаточное развитие тела. Примером могут служить пигмеи, племена Центральной Африки.
Гиперфункция -у детей возникает гигантизм, так как еще нет зарастания эпифизарных щелей и возможен ускоренный рост кости; у взрослых развивается акромегалия – из-за акрального роста кости происходит увеличение размера носа, стопы, кистей, челюсти.
Адренокортикотропный гормон (АКТГ)
АКТГ вырабатывается базофильными клетками аденогипофиза. АКТГ, помимо основного действия – стимуляции синтеза и секреции гормонов коры надпочечников, обладает жиромобилизующей и меланоцитстимулирующей активностью.
Молекула АКТГ у всех видов животных содержит 39 аминокислотных остатков.
Патологическая биохимия
В результате избыточного образования АКТГ гипофизом или его эктопического образования опухолью развивается синдром Кушинга.Слабое МСГ-подобное действие АКТГ, а также секреция β- или α-МСГ приводят к повышенной пигментации кожи. Возникающие метаболические нарушения обусловлены гиперпродукцией стероидов надпочечников, к ним относятся: 1) отрицательный азотный, калиевый и фосфорный баланс; 2) задержка натрия, которая может привести к повышению артериального давления и отекам; 3) нарушение толерантности к глюкозе или сахарный диабет; 4) повышение содержания жирных кислот в плазме; 5) уменьшение количества эозинофилов и лимфоцитов в крови при увеличении количества полиморфноядерных лейкоцитов. У больных с синдромом Кушинга может наблюдаться атрофия мышц и специфическое перераспределение жира с его отложением на туловище. Отсутствие АКТГ, связанное с опухолью, инфекцией или инфарктом гипофиза, вызывает противоположные сдвиги.
Тиреотропный гормон (ТТГ, тиротропин)
Тиротропин является сложным гликопротеином и содержит, кроме того, по две α- и β-субъединицы, которые в отдельности биологической активностью не обладают: мол. масса его около 30000.
Тиротропин контролирует развитие и функцию щитовидной железы и регулирует биосинтез и секрецию в кровь тиреоидных гормонов.
Предполагают, что действие тиротропина осуществляется, подобно действию других гормонов белковой природы, посредством связывания со специфическими рецепторами плазматических мембран и активирования аденилатциклазной системы.
Липотропные гормоны (ЛТГ, липотропины)
Среди гормонов передней доли гипофиза, структура и функция которых выяснены в последнее десятилетие, следует отметить липотропины, в частности β- и γ-ЛТГ.
К биологическим свойствам β-липотропина относятся жиромобилизующее действие, кортикотропная, меланоцитстимулирующая и гипокальциемическая активность и, кроме того, инсулиноподобный эффект, выражающийся в повышении скорости утилизации глюкозы в тканях.
Среди гормонов передней доли гипофиза, структура и функция которых выяснены в последнее десятилетие, следует отметить липотропины, в частности β- и γ-ЛТГ.
К биологическим свойствам β-липотропина относятся жиромобилизующее действие, кортикотропная, меланоцитстимулирующая и гипокальциемическая активность и, кроме того, инсулиноподобный эффект, выражающийся в повышении скорости утилизации глюкозы в тканях.
Перечисленные биологические свойства обусловлены не β-липотропином, оказавшимся лишенным гормональной активности, а продуктами его распада, образующимися при ограниченном протеолизе. Оказалось, что в ткани мозга и в промежуточной доле гипофиза синтезируются биологически активные пептиды, наделенные опиатоподобным действием.
Структуры некоторых из них приведены ниже:
Н–Тир–Гли–Гли–Фен–Мет–ОН
Метионин-энкефалин
Н–Тир–Гли–Гли–Фен–Лей–ОН
Лейцин-энкефалин
Н–Тир–Гли–Гли–Фен–Мет–Тре–Сер–Глу–Лиз–Сер–Глн–Тре–Про–
Лей–Вал–Тре–Лей–Фен–Лиз–Асн–Ала–Иле–Вал–Лиз–Асн–Ала–Гис–
–Лиз–Лиз–Гли–Глн–ОН
β-Эндорфин
Лактотропный гормон (пролактин, лютеотропный гормон)
Пролактин считается одним из наиболее «древних» гормонов гипофиза. Помимо основного действия (стимуляция развития молочных желез и лактации), пролактин имеет важное биологическое значение – стимулирует рост внутренних органов, секрецию желтого тела (отсюда его второе название «лютеотропный гормон»), оказывает ренотропное, эритропоэтическое и гипергликемическое действие и др. Избыток пролактина, образующийся обычно при наличии опухолей из секретирующих пролактин клеток, приводит к прекращению менструаций (аменорея) и увеличению молочных желез у женщин и к импотенции – у мужчин.
Расшифрована структура пролактина из гипофиза овцы, быка и человека. Это крупный белок, представленный одной полипептидной цепью с тремя дисульфидными связями, состоящий из 199 аминокислотных остатков. Видовые отличия в последовательности аминокислот касаются по существу 2–3 аминокислотных остатков.
В крови женщин уровень пролактина резко повышается перед родами: до 0,2 нг/л против 0,01 нг/л в норме.
Гормоны щитовидной железы
Щитовидная железа состоит из множества особых полостей – фолликулов, заполненных вязким секретом – коллоидом.
В состав коллоида входит особый йодсодержащий гликопротеин с высокой мол. массой – порядка 650000 (5000 аминокислотных остатков). Этот гликопротеин получил название йодтиреоглобулина. Он представляет собой запасную форму тироксина и трийодтиронина – основных гормонов фолликулярной части щитовидной железы.
Структура гормонов щитовидной железы:
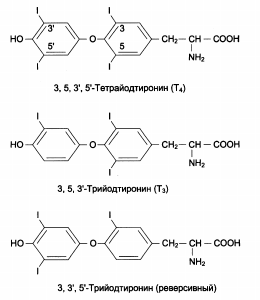 Патологическая биохимия: зоб(увеличение щитовидной железы – недостаток или избыто йодида), гипотиреоз(дефицит свободных Т3 или Т4), гипертиреоз(тиреотоксикоз – избыточное образование тиреоидных гормонов).
Паратиреоидный гормон (ПТГ)
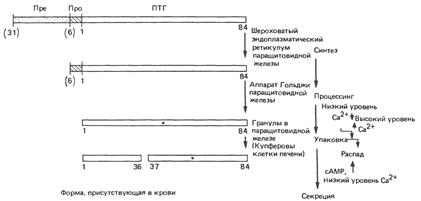
Предшественники и продукты расщепления ПТГ и локализация отдельных этапов расщепления в паращитовидных железах и печени. Цифры в скобках соответствуют числу аминокислот в пре(31) и про(6) фрагментах: →
Патологическая биохимия: недостаток ПТГ приводит к гипопаратиреозу(сниженный уровень ионизированного кальция и повышенный уровень фосфата в сыворотке крови); псевдогипопаратиреоз (органы-мишени резистентны к ПТГ); гиперпаратиреоз (избыточная продукция ПТГ возникает, как правило, вследствие аденомы паратиреоидных желёз); вторичный гиперпаратиреоз (гиперплазия паратиреоидных желёз и гиперсекреция ПТГ).
Кальцитонин (КТ)
Патологическая биохимия: зоб(увеличение щитовидной железы – недостаток или избыто йодида), гипотиреоз(дефицит свободных Т3 или Т4), гипертиреоз(тиреотоксикоз – избыточное образование тиреоидных гормонов).
Паратиреоидный гормон (ПТГ)
Предшественники и продукты расщепления ПТГ и локализация отдельных этапов расщепления в паращитовидных железах и печени. Цифры в скобках соответствуют числу аминокислот в пре(31) и про(6) фрагментах: →
Патологическая биохимия: недостаток ПТГ приводит к гипопаратиреозу(сниженный уровень ионизированного кальция и повышенный уровень фосфата в сыворотке крови); псевдогипопаратиреоз (органы-мишени резистентны к ПТГ); гиперпаратиреоз (избыточная продукция ПТГ возникает, как правило, вследствие аденомы паратиреоидных желёз); вторичный гиперпаратиреоз (гиперплазия паратиреоидных желёз и гиперсекреция ПТГ).
Кальцитонин (КТ)
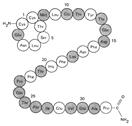 Кальцитонин человека
Патологическая биохимия:клинические проявления недостаточности КТ не выявлены. Избыточность КТ наблюдается при медуллярной тиреокарциноме – заболевании, которое может быть спорадическим или семейным.
Биологическое действие кальцитонина прямо противоположно эффекту паратгормона: он вызывает подавление в костной ткани резорбтивных процессов и соответственно гипокальциемию и гипофосфатемию. Таким образом, постоянство уровня кальция в крови человека и животных обеспечивается главным образом паратгормоном, кальцитриолом и кальцитонином.
Биологическое действие гормонов щитовидной железы распространяется на множество физиологических функций организма. В частности, гормоны регулируют скорость основного обмена, рост и дифференцировку тканей, обмен белков, углеводов и липидов, водно-электролитный обмен, деятельность ЦНС, пищеварительного тракта, гемопоэз, функцию сердечнососудистой системы, потребность в витаминах, сопротивляемость организма инфекциям и др. Точкой приложения действия тиреоидных гормонов, как и всех стероидов, считается генетический аппарат.
Специфические рецепторы – белки – обеспечивают транспорт тиреоидных гормонов в ядро и взаимодействие со структурными генами, в результате чего увеличивается синтез ферментов, регулирующих скорость окислительно-восстановительных процессов. Естественно поэтому, что недостаточная функция щитовидной железы (гипофункция) или, наоборот, повышенная секреция гормонов (гиперфункция) вызывает глубокие расстройства физиологического статуса организма.
Гипофункция щитовидной железы в раннем детском возрасте приводит к развитию болезни, известной в литературе как кретинизм. Помимо остановки роста, специфических изменений кожи, волос, мышц, резкого снижения скорости процессов обмена, при кретинизме отмечаются глубокиенарушения психики; специфическое гормональное лечение в этом случае не дает положительных результатов.
Недостаточная функция щитовидной железы в зрелом возрасте сопровождается развитием гипотиреоидного отека, или микседемы (от греч. myxa – слизь, oedemo – отек). Это заболевание чаще встречается у женщин и характеризуется нарушением водно-солевого, основного и жирового обмена.
У больных отмечаются слизистый отек, патологическое ожирение, резкое снижение основного обмена, выпадение волос и зубов, общие мозговые нарушения и психические расстройства. Кожа становится сухой, температура тела снижается; в крови повышено содержание глюкозы. Гипотиреоидизм сравнительно легко поддается лечению препаратами щитовидной железы. Кальцитонин человека
Патологическая биохимия:клинические проявления недостаточности КТ не выявлены. Избыточность КТ наблюдается при медуллярной тиреокарциноме – заболевании, которое может быть спорадическим или семейным.
Биологическое действие кальцитонина прямо противоположно эффекту паратгормона: он вызывает подавление в костной ткани резорбтивных процессов и соответственно гипокальциемию и гипофосфатемию. Таким образом, постоянство уровня кальция в крови человека и животных обеспечивается главным образом паратгормоном, кальцитриолом и кальцитонином.
Биологическое действие гормонов щитовидной железы распространяется на множество физиологических функций организма. В частности, гормоны регулируют скорость основного обмена, рост и дифференцировку тканей, обмен белков, углеводов и липидов, водно-электролитный обмен, деятельность ЦНС, пищеварительного тракта, гемопоэз, функцию сердечнососудистой системы, потребность в витаминах, сопротивляемость организма инфекциям и др. Точкой приложения действия тиреоидных гормонов, как и всех стероидов, считается генетический аппарат.
Специфические рецепторы – белки – обеспечивают транспорт тиреоидных гормонов в ядро и взаимодействие со структурными генами, в результате чего увеличивается синтез ферментов, регулирующих скорость окислительно-восстановительных процессов. Естественно поэтому, что недостаточная функция щитовидной железы (гипофункция) или, наоборот, повышенная секреция гормонов (гиперфункция) вызывает глубокие расстройства физиологического статуса организма.
Гипофункция щитовидной железы в раннем детском возрасте приводит к развитию болезни, известной в литературе как кретинизм. Помимо остановки роста, специфических изменений кожи, волос, мышц, резкого снижения скорости процессов обмена, при кретинизме отмечаются глубокиенарушения психики; специфическое гормональное лечение в этом случае не дает положительных результатов.
Недостаточная функция щитовидной железы в зрелом возрасте сопровождается развитием гипотиреоидного отека, или микседемы (от греч. myxa – слизь, oedemo – отек). Это заболевание чаще встречается у женщин и характеризуется нарушением водно-солевого, основного и жирового обмена.
У больных отмечаются слизистый отек, патологическое ожирение, резкое снижение основного обмена, выпадение волос и зубов, общие мозговые нарушения и психические расстройства. Кожа становится сухой, температура тела снижается; в крови повышено содержание глюкозы. Гипотиреоидизм сравнительно легко поддается лечению препаратами щитовидной железы.
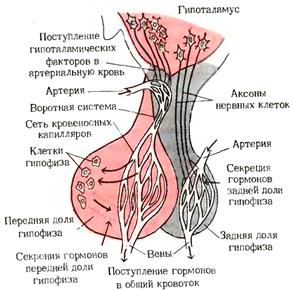
| Подробная схема гипоталамо-гипофизарной системы:
 Продукты расщепления проопиомеланокортина (ПОМК). МСГ – меланоцит-стимулирующий гормон: КПНДГ – кортикотропиноподобный пептид промежуточной доли гипофиза; ЛПГ – липотропин.
Продукты расщепления проопиомеланокортина (ПОМК). МСГ – меланоцит-стимулирующий гормон: КПНДГ – кортикотропиноподобный пептид промежуточной доли гипофиза; ЛПГ – липотропин.
 Патологическая биохимия:
Нарушения секреции или действия АДГ приводят к несахарному диабету, который характеризуется выделением больших объемов разбавленной мочи. Первичный несахарный диабет, связанный с дефицитом АДГ, обычно развивается при повреждении гипоталамо-гипофизарного тракта вследствие перелома основания черепа, опухоли или инфекции: однако он может иметь и наследственную природу. При наследственном нефрогенном несахарном диабете секреция АДГ остается нормальной, но клетки-мишени утрачивают способность реагировать на гормон, вероятно, из-за нарушения его рецепции. Этот наследственный дефект отличается от приобретенного нефрогенного несахарного диабета, который чаще всего возникает при терапевтическом введении лития больным с маниакально-депрессивным психозом. Синдром неадекватной секреции АДГ связан обычно с эктопическим образованием гормона различными опухолями (обычно опухолями легких), но может также наблюдаться и при болезнях мозга, легочных инфекциях или гипотиреозе. Неадекватной такая секреция считается потому, что продукция АДГ происходит с нормальной или повышенной скоростью в условиях гипоосмоляльности, и это вызывает устойчивую и прогрессивную гипонатриемию с выделением гипертонической мочи.
Структура молекулы гормона роста человека. Цифры обозначают положение аминокислотных остатков, начи-
начиная с N-конца.
Патологическая биохимия:
Нарушения секреции или действия АДГ приводят к несахарному диабету, который характеризуется выделением больших объемов разбавленной мочи. Первичный несахарный диабет, связанный с дефицитом АДГ, обычно развивается при повреждении гипоталамо-гипофизарного тракта вследствие перелома основания черепа, опухоли или инфекции: однако он может иметь и наследственную природу. При наследственном нефрогенном несахарном диабете секреция АДГ остается нормальной, но клетки-мишени утрачивают способность реагировать на гормон, вероятно, из-за нарушения его рецепции. Этот наследственный дефект отличается от приобретенного нефрогенного несахарного диабета, который чаще всего возникает при терапевтическом введении лития больным с маниакально-депрессивным психозом. Синдром неадекватной секреции АДГ связан обычно с эктопическим образованием гормона различными опухолями (обычно опухолями легких), но может также наблюдаться и при болезнях мозга, легочных инфекциях или гипотиреозе. Неадекватной такая секреция считается потому, что продукция АДГ происходит с нормальной или повышенной скоростью в условиях гипоосмоляльности, и это вызывает устойчивую и прогрессивную гипонатриемию с выделением гипертонической мочи.
Структура молекулы гормона роста человека. Цифры обозначают положение аминокислотных остатков, начи-
начиная с N-конца.
 Строение АКТГ человека
Н-Сер–Тир–Сер–Мет–Глу–Гис–Фен–Арг–Трп–Гли–Лиз–Про–Вал–Гли–
–Лиз–Лиз–Aрг–Aрг–Про–Вал–Лиз–Вал–Тир–Про–Асп–Ала–Гли–Глу–
–Асп–Глн–Сер–Ала–Глу–Ала–Фен–Про–Лей–Глу–Фен-ОН
Биосинтез гормонов щитовидной железы регулируется тиротропином – гормоном гипофиза
Строение АКТГ человека
Н-Сер–Тир–Сер–Мет–Глу–Гис–Фен–Арг–Трп–Гли–Лиз–Про–Вал–Гли–
–Лиз–Лиз–Aрг–Aрг–Про–Вал–Лиз–Вал–Тир–Про–Асп–Ала–Гли–Глу–
–Асп–Глн–Сер–Ала–Глу–Ала–Фен–Про–Лей–Глу–Фен-ОН
Биосинтез гормонов щитовидной железы регулируется тиротропином – гормоном гипофиза
 Следует отметить еще одно поражение щитовидной железы – эндемический зоб. Болезнь обычно развивается у лиц, проживающих в горных местностях, где содержание йода в воде и растениях недостаточно. Недостаток йода приводит к компенсаторному увеличению массы ткани щитовидной железы за счет преимущественного разрастания соединительной ткани, однако, этот процесс не сопровождается увеличением секреции тиреоидных гормонов. Болезнь не приводит к серьезным нарушениям функций организма, хотя увеличенная в размерах щитовидная железа создает определенные неудобства. Лечение сводится к обогащению продуктов питания, в частности поваренной соли, неорганическим йодом.
Повышенная функция щитовидной железы (гиперфункция) вызывает развитие гипертиреоза, известного в литературе под названием «зоб диффузный токсический» (болезнь Грейвса, или базедова болезнь). Резкое повышение обмена веществ сопровождается усиленным распадом тканевых белков, что приводит к развитию отрицательного азотистого баланса. Наиболее характерным проявлением болезни считается триада симптомов: резкое увеличение числа сердечных сокращений (тахикардия), пучеглазие (экзофтальм) и зоб, т.е. увеличенная в размерах щитовидная железа; у больных отмечаются общее истощение организма, а также психические расстройства.
Следует отметить еще одно поражение щитовидной железы – эндемический зоб. Болезнь обычно развивается у лиц, проживающих в горных местностях, где содержание йода в воде и растениях недостаточно. Недостаток йода приводит к компенсаторному увеличению массы ткани щитовидной железы за счет преимущественного разрастания соединительной ткани, однако, этот процесс не сопровождается увеличением секреции тиреоидных гормонов. Болезнь не приводит к серьезным нарушениям функций организма, хотя увеличенная в размерах щитовидная железа создает определенные неудобства. Лечение сводится к обогащению продуктов питания, в частности поваренной соли, неорганическим йодом.
Повышенная функция щитовидной железы (гиперфункция) вызывает развитие гипертиреоза, известного в литературе под названием «зоб диффузный токсический» (болезнь Грейвса, или базедова болезнь). Резкое повышение обмена веществ сопровождается усиленным распадом тканевых белков, что приводит к развитию отрицательного азотистого баланса. Наиболее характерным проявлением болезни считается триада симптомов: резкое увеличение числа сердечных сокращений (тахикардия), пучеглазие (экзофтальм) и зоб, т.е. увеличенная в размерах щитовидная железа; у больных отмечаются общее истощение организма, а также психические расстройства.
| ||||||
| 3. Гормоны поджелудочной железы. Строение, механизм действия инсулина, глюкагона. | |||||||
Поджелудочная железа относится к железам со смешанной секрецией. Внешнесекреторная функция ее заключается в синтезе ряда ключевых ферментов пищеварения, в частности амилазы, липазы, трипсина, химотрипсина, карбоксипептидазы и др., поступающих в кишечник с соком поджелудочной железы. Внутрисекреторную функцию выполняют, как было установлено в 1902 г. Л.В. Соболевым, панкреатические островки (островки Лангерганса), состоящие из клеток разного типа и вырабатывающие гормоны, как правило, противоположного действия. Так, α- (или А-)клетки продуцируют глюкагон, β- (или В-) клетки синтезируют инсулин, δ-(или D-) клетки вырабатывают соматостатин и F-клетки – малоизученный панкреатический полипептид.
Гормоны поджелудочной железы: инсулин, глюкагон, соматостатин, панкреатический полипептид.
Структура проинсулина и инсулина человека:
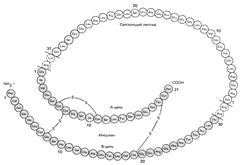 Проинсулин Проинсулин
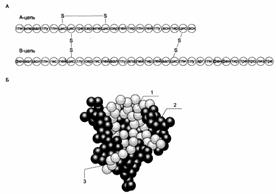 Инсулин
Синтезированный из проинсулина инсулин может существовать в нескольких формах, различающихся по биологическим, иммунологическим и физико-химическим свойствам. Различают две формы инсулина: 1) свободную, вступающую во взаимодействие с антителами, полученными к кристаллическому инсулину, и стимулирующую усвоение глюкозы мышечной и жировой тканями; 2) связанную, не реагирующую с антителами и активную только в отношении жировой ткани.
В физиологической регуляции синтеза инсулина доминирующую роль играет концентрация глюкозы в крови. Так, повышение содержания глюкозы в крови вызывает увеличение секреции инсулина в панкреатических островках, а снижение ее содержания, наоборот,– замедление секреции инсулина. Этот феномен контроля по типу обратной связи рассматривается как один из важнейших механизмов регуляции содержания глюкозы в крови.
Механизм действия инсулина окончательно не расшифрован, несмотря на огромное количество фактических данных, свидетельствующих о существовании тесной и прямой зависимости между инсулином и процессами обмена веществ в организме. В соответствии с «унитарной» теорией все эффекты инсулина вызваны его влиянием на обмен глюкозы через фермент гексокиназу. Новые экспериментальные данные свидетельствуют, что усиление и стимуляция инсулином таких процессов, как транспорт ионов и аминокислот, трансляция и синтез белка, экспрессия генов и др., являются независимыми. Это послужило основанием для предположения о множественных механизмах действия инсулина.
Наиболее вероятной в настоящее время представляется мембранная локализация первичного действия почти всех белковых гормонов, включая инсулин. Получены доказательства существования специфического рецептора инсулина на внешней плазматической мембране почти всех клеток организма, а также образования инсулинрецепторного комплекса. Рецептор синтезируется в виде предшественника – полипептида (1382 аминокислотных остатка, мол. масса 190000), который далее расщепляется на α- и β-субъединицы, т.е. на гетеродимер (в формуле α2–β2), связанные дисульфидными связями. Оказалось, что если α-субъединицы (мол. масса 135000) почти целиком располагаются на внешней стороне биомембраны, выполняя функцию связывания инсулина клетки, то β-субъединицы (мол. масса 95000) представляют собой трансмембранный белок, выполняющий функцию преобразования сигнала. Концентрация рецепторов инсулина на поверхности достигает 20000 на клетку, и период их полужизни составляет 7–12 ч.
Патологическая биохимия: сахарный диабет(сахарный диабет I типа – инсулинзависимый, сахарный диабет II типа – инсулин-незавысимый).
Сахарный диабет характеризуется рядом специфических нарушений процессов обмена. Так, у больных развиваются гипергликемия (увеличение уровня глюкозы в крови) и гликозурия (выделение глюкозы с мочой, в которой в норме она отсутствует). К расстройствам обмена относят также усиленный распад гликогена в печени и мышцах, замедление биосинтеза белков и жиров, снижение скорости окисления глюкозы в тканях, развитие отрицательного азотистого баланса, увеличение содержания холестерина и других липидов в крови. При диабете усиливаются мобилизация жиров из депо, синтез углеводов из аминокислот (глюконеогенез) и избыточный синтез кетоновых тел (кетонурия).
Глюкагон
Глюкагон синтезируется в основном в α-клетках панкреатических островков поджелудочной железы, а также в ряде клеток кишечника (см. далее). Он представлен одной линейно расположенной полипептидной цепью, в состав которой входит 29 аминокислотных остатков в следующей последовательности:
Н–Гис–Сер–Глн–Гли–Тре–Фен–Тре–Сер–Асп–Тир–Сер–Лиз–Тир–Лей––Асп–Сер–Aрг–Aрг–Ала–Глн–Асп–Фен–Вал–Глн–Трп–Лей–Мет–Асн––Тре–ОН
Глюкагон образуется из своего предшественника проглюкагона, содержащего на С-конце полипептида дополнительный октапептид (8 остатков), отщепляемый в процессе постсинтетического протеолиза.
По биологическому действию глюкагон, как и адреналин, относятся к гипергликемическим факторам, вызывает увеличение концентрации глюкозы в крови главным образом за счет распада гликогена в печени.
Органами-мишенями для глюкагона являются печень, миокард, жировая ткань, но не скелетные мышцы. Биосинтез и секреция глюкагона контролируются главным образом концентрацией глюкозы по принципу обратной связи. Инсулин
Синтезированный из проинсулина инсулин может существовать в нескольких формах, различающихся по биологическим, иммунологическим и физико-химическим свойствам. Различают две формы инсулина: 1) свободную, вступающую во взаимодействие с антителами, полученными к кристаллическому инсулину, и стимулирующую усвоение глюкозы мышечной и жировой тканями; 2) связанную, не реагирующую с антителами и активную только в отношении жировой ткани.
В физиологической регуляции синтеза инсулина доминирующую роль играет концентрация глюкозы в крови. Так, повышение содержания глюкозы в крови вызывает увеличение секреции инсулина в панкреатических островках, а снижение ее содержания, наоборот,– замедление секреции инсулина. Этот феномен контроля по типу обратной связи рассматривается как один из важнейших механизмов регуляции содержания глюкозы в крови.
Механизм действия инсулина окончательно не расшифрован, несмотря на огромное количество фактических данных, свидетельствующих о существовании тесной и прямой зависимости между инсулином и процессами обмена веществ в организме. В соответствии с «унитарной» теорией все эффекты инсулина вызваны его влиянием на обмен глюкозы через фермент гексокиназу. Новые экспериментальные данные свидетельствуют, что усиление и стимуляция инсулином таких процессов, как транспорт ионов и аминокислот, трансляция и синтез белка, экспрессия генов и др., являются независимыми. Это послужило основанием для предположения о множественных механизмах действия инсулина.
Наиболее вероятной в настоящее время представляется мембранная локализация первичного действия почти всех белковых гормонов, включая инсулин. Получены доказательства существования специфического рецептора инсулина на внешней плазматической мембране почти всех клеток организма, а также образования инсулинрецепторного комплекса. Рецептор синтезируется в виде предшественника – полипептида (1382 аминокислотных остатка, мол. масса 190000), который далее расщепляется на α- и β-субъединицы, т.е. на гетеродимер (в формуле α2–β2), связанные дисульфидными связями. Оказалось, что если α-субъединицы (мол. масса 135000) почти целиком располагаются на внешней стороне биомембраны, выполняя функцию связывания инсулина клетки, то β-субъединицы (мол. масса 95000) представляют собой трансмембранный белок, выполняющий функцию преобразования сигнала. Концентрация рецепторов инсулина на поверхности достигает 20000 на клетку, и период их полужизни составляет 7–12 ч.
Патологическая биохимия: сахарный диабет(сахарный диабет I типа – инсулинзависимый, сахарный диабет II типа – инсулин-незавысимый).
Сахарный диабет характеризуется рядом специфических нарушений процессов обмена. Так, у больных развиваются гипергликемия (увеличение уровня глюкозы в крови) и гликозурия (выделение глюкозы с мочой, в которой в норме она отсутствует). К расстройствам обмена относят также усиленный распад гликогена в печени и мышцах, замедление биосинтеза белков и жиров, снижение скорости окисления глюкозы в тканях, развитие отрицательного азотистого баланса, увеличение содержания холестерина и других липидов в крови. При диабете усиливаются мобилизация жиров из депо, синтез углеводов из аминокислот (глюконеогенез) и избыточный синтез кетоновых тел (кетонурия).
Глюкагон
Глюкагон синтезируется в основном в α-клетках панкреатических островков поджелудочной железы, а также в ряде клеток кишечника (см. далее). Он представлен одной линейно расположенной полипептидной цепью, в состав которой входит 29 аминокислотных остатков в следующей последовательности:
Н–Гис–Сер–Глн–Гли–Тре–Фен–Тре–Сер–Асп–Тир–Сер–Лиз–Тир–Лей––Асп–Сер–Aрг–Aрг–Ала–Глн–Асп–Фен–Вал–Глн–Трп–Лей–Мет–Асн––Тре–ОН
Глюкагон образуется из своего предшественника проглюкагона, содержащего на С-конце полипептида дополнительный октапептид (8 остатков), отщепляемый в процессе постсинтетического протеолиза.
По биологическому действию глюкагон, как и адреналин, относятся к гипергликемическим факторам, вызывает увеличение концентрации глюкозы в крови главным образом за счет распада гликогена в печени.
Органами-мишенями для глюкагона являются печень, миокард, жировая ткань, но не скелетные мышцы. Биосинтез и секреция глюкагона контролируются главным образом концентрацией глюкозы по принципу обратной связи.
|
 Местом синтеза проинсулина считается фракция микросом β-клеток панкреатических островков; превращение неактивного проинсулина в активный инсулин (наиболее существенная часть синтеза) происходит при перемещении проинсулина от рибосом к секреторным гранулам путем частичного протеолиза (отщепление с С-конца полипептидной цепи пептида, содержащего 33 аминокислотных остатка и получившего наименование соединяющего пептида, или С-пептида).
Метаболические сдвиги при инсулиновой недостаточности (сахарный диабет):
Местом синтеза проинсулина считается фракция микросом β-клеток панкреатических островков; превращение неактивного проинсулина в активный инсулин (наиболее существенная часть синтеза) происходит при перемещении проинсулина от рибосом к секреторным гранулам путем частичного протеолиза (отщепление с С-конца полипептидной цепи пептида, содержащего 33 аминокислотных остатка и получившего наименование соединяющего пептида, или С-пептида).
Метаболические сдвиги при инсулиновой недостаточности (сахарный диабет):
 Самым интересным свойством рецептора инсулина, отличным от всех других рецепторов гормонов белковой и пептидной природы, является его способность аутофосфорилирования, т.е. когда рецептор наделен сам протеинкиназной (тирозинкиназной) активностью. При связывании инсулина с α-цепями рецептора происходит активирование тирозинкиназной активности β-цепей путем фосфорилирования их тирозиновых остатков. В свою очередь активная тирозинкиназа β-цепей запускает каскад фосфорилирования–дефосфорилирования протеинкиназ, в частности мембранных или цитозольных серин- или треонинкиназ, т.е. протеинкиназ и белков-мишеней, фосфорилирование в которых осуществляется за счет ОН-групп серина и треонина.
Соответственно имеют место изменения клеточной активности, в частности активация и ингибирование ферментов, транспорт глюкозы, синтез полимерных молекул нуклеиновых кислот и белков и т.д. (Следует указать, что у инсулинрезистентных больных сахарным диабетом синтез инсулина не нарушен, однако организм больных не реагирует ни на свой, ни на инъецированный инсулин. Оказалось, что у части этих больных имеет место мутация в тирозинкиназном домене рецептора и, хотя инсулин связывается нормально с этим мутантным рецептором, дальнейшей передачи сигнала не происходит, так как тирозинкиназа инактивирована. Поэтому лечение больных этой формой диабета инсулином оказывается неэффективным).
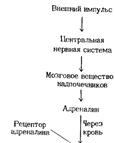
В механизме действия глюкагона первичным является связывание со специфическими рецепторами мембраны клеток, образовавшийся глюкагонрецепторный комплекс активирует аденилатциклазу и соответственно образование цАМФ. Последний, являясь универсальным эффектором внутриклеточных ферментов, активирует протеинкиназу, которая в свою очередь фосфорилирует киназу фосфорилазы и гликогенсинтазу. Фосфорилирование первого фермента способствует формированию активной гликогенфосфорилазы и соответственно распаду гликогена с образованием глюкозо-1-фосфата, в то время как фосфорилирование гликогенсинтазы сопровождается переходом ее в неактивную форму и соответственно блокированием синтеза гликогена. Общим итогом действия глюкагона являются ускорение распада гликогена и торможение его синтеза в печени, что приводит к увеличению концентрации глюкозы в крови.
Установлено, что глюкагон способствует образованию глюкозы из промежуточных продуктов обмена белков и жиров. Глюкагон стимулирует образование глюкозы из аминокислот путем индукции синтеза ферментов глюконеогенеза при участии цАМФ. Глюкагон в отличие от адреналина тормозит гликолитический распад глюкозы до молочной кислоты, способствуя тем самым гипергликемии. Он активирует опосредованно через цАМФ липазу тканей, оказывая мощный липолитический эффект. Существуют и различия в физиологическом действии: в отличие от адреналина глюкагон не повышает кровяного давления и не увеличивает частоту сердечных сокращений.
Самым интересным свойством рецептора инсулина, отличным от всех других рецепторов гормонов белковой и пептидной природы, является его способность аутофосфорилирования, т.е. когда рецептор наделен сам протеинкиназной (тирозинкиназной) активностью. При связывании инсулина с α-цепями рецептора происходит активирование тирозинкиназной активности β-цепей путем фосфорилирования их тирозиновых остатков. В свою очередь активная тирозинкиназа β-цепей запускает каскад фосфорилирования–дефосфорилирования протеинкиназ, в частности мембранных или цитозольных серин- или треонинкиназ, т.е. протеинкиназ и белков-мишеней, фосфорилирование в которых осуществляется за счет ОН-групп серина и треонина.
Соответственно имеют место изменения клеточной активности, в частности активация и ингибирование ферментов, транспорт глюкозы, синтез полимерных молекул нуклеиновых кислот и белков и т.д. (Следует указать, что у инсулинрезистентных больных сахарным диабетом синтез инсулина не нарушен, однако организм больных не реагирует ни на свой, ни на инъецированный инсулин. Оказалось, что у части этих больных имеет место мутация в тирозинкиназном домене рецептора и, хотя инсулин связывается нормально с этим мутантным рецептором, дальнейшей передачи сигнала не происходит, так как тирозинкиназа инактивирована. Поэтому лечение больных этой формой диабета инсулином оказывается неэффективным).
В механизме действия глюкагона первичным является связывание со специфическими рецепторами мембраны клеток, образовавшийся глюкагонрецепторный комплекс активирует аденилатциклазу и соответственно образование цАМФ. Последний, являясь универсальным эффектором внутриклеточных ферментов, активирует протеинкиназу, которая в свою очередь фосфорилирует киназу фосфорилазы и гликогенсинтазу. Фосфорилирование первого фермента способствует формированию активной гликогенфосфорилазы и соответственно распаду гликогена с образованием глюкозо-1-фосфата, в то время как фосфорилирование гликогенсинтазы сопровождается переходом ее в неактивную форму и соответственно блокированием синтеза гликогена. Общим итогом действия глюкагона являются ускорение распада гликогена и торможение его синтеза в печени, что приводит к увеличению концентрации глюкозы в крови.
Установлено, что глюкагон способствует образованию глюкозы из промежуточных продуктов обмена белков и жиров. Глюкагон стимулирует образование глюкозы из аминокислот путем индукции синтеза ферментов глюконеогенеза при участии цАМФ. Глюкагон в отличие от адреналина тормозит гликолитический распад глюкозы до молочной кислоты, способствуя тем самым гипергликемии. Он активирует опосредованно через цАМФ липазу тканей, оказывая мощный липолитический эффект. Существуют и различия в физиологическом действии: в отличие от адреналина глюкагон не повышает кровяного давления и не увеличивает частоту сердечных сокращений.
| ||||||
| 4. Гормоны коры надпочечников: минерало- и глюкокортикоидов. Биосинтез и распад адреналина. Половые гормоны: мужские и женские, влияние на обмен веществ. Гипер- и гипопродукция гормонов | |||||||
Гормоны коры надпочечников
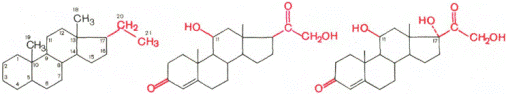
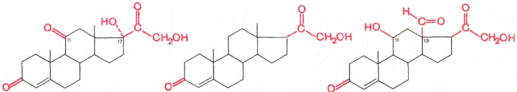
Биологически активные кортикостероиды объединяют в 3 основные класса:
1. Глюкокортикоиды (С21-стероиды). Основной глюкокортикоид человека – кортизол.
2. Минералокортикоиды (С21-стероиды). Самый активный гормон этого класса – альдостерон.
3. Андрогены – С19-стероиды. Самый мощный андроген надпочечников – тестостерон.
Гормоны мозгового вещества надпочечников
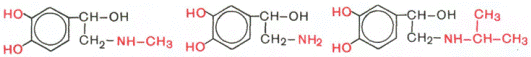
О способности экстрактов из надпочечников повышать кровяное давление было известно еще в XIX в., однако только в 1901 г. Дж. Такамине и сотр. выделили из мозгового слоя надпочечников активное начало, идентифицированное с адреналином. Это был первый гормон, полученный в чистом кристаллическом виде. Спустя более 40 лет, в 1946 г., из мозгового вещества был выделен еще один гормон – норадреналин, который до этого был синтезирован химическим путем. Помимо этих двух главных гормонов, в надпочечниках в следовых количествах синтезируется еще один гормон – изопропиладреналин. Все указанные гормоны имеют сходное строение.
В мозговом веществе надпочечников человека массой 10 г содержится около 5 мг адреналина и 0,5 мг норадреналина. Содержание их в крови составляет соответственно 1,9 и 5,2 нмоль/л. В плазме крови оба гормона присутствуют как в свободном, так и в связанном, в частности, с альбуминами состоянии. Небольшие количества обоих гормонов откладываются в виде соли с АТФ в нервных окончаниях, освобождаясь в ответ на их раздражение. Адреналин и норадреналин, как и дофамин (см. структуру), относятся к катехоламинам, т.е. к классу органических веществ, оказывающих сильное биологическое действие.
Кроме того, все они оказывают мощное сосудосуживающее действие, вызывая повышение артериального давления, и в этом отношении действие их сходно с действием симпатической нервной системы. Известно мощное регулирующее влияние этих гормонов на обмен углеводов в организме. Так, в частности, адреналин вызывает резкое повышение уровня глюкозы в крови, что обусловлено ускорением распада гликогена в печени под действием фермента фосфорилазы.
Известно, что и адреналин, и норадреналин быстро разрушаются в организме; с мочой выделяются неактивные продукты их обмена, главным образом в виде 3-метокси-4-оксиминдальной кислоты, оксоадренохрома, метоксинорадреналина и метоксиадреналина. Эти метаболиты содержатся в моче преимущественно в связанной с глюкуроновой кислотой форме.
Гормоны коркового вещества надпочечников
Со второй половины XIX в. известно заболевание, названное бронзовой болезнью, или болезнью Аддисона, по имени автора, впервые описавшего его. Заболевание характеризуется усиленной пигментацией кожи, мышечной рушением водно-солевого обмена и обмена белков и углеводов. Как установлено, в основе заболевания лежит туберкулезное поражение надпочечников, которое приводит к недостаточности или отсутствию синтеза гормонов в корковом веществе.
При болезни Аддисона расстройства обмена выражаются резким снижением концентрации ионов натрия и хлора и повышением уровня ионов калия в крови и мышцах, потерей воды организмом и снижением уровня глюкозы в крови. Нарушения белкового обмена проявляются снижением синтеза белков из аминокислот и увеличением уровня остаточного азота в крови.
В зависимости от характера биологического эффекта гормоны коркового вещества надпочечников условно делят на глюкокортикоиды(кортикостероиды, оказывающие влияние на обмен углеводов, белков, жиров и нуклеиновых кислот) и минералокортикоиды(кортикостероиды, оказывающие преимущественное влияние на обмен солей и воды).
В надпочечниках открыты, кроме того, неспецифические (не свойственные данной ткани) половые гормоны: андро- и эстрокортикостероиды). К первым относятся кортикостерон, кортизон, гидрокортизон (кортизол), 11-дезоксикортизол и 11-дегидрокортикостерон, ко вторым – дезоксикортикостерон и альдостерон.
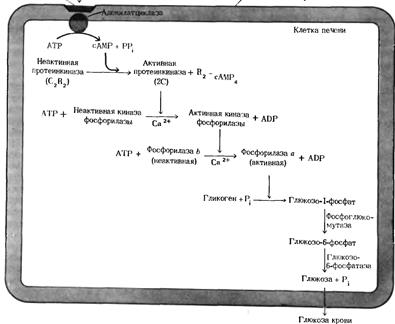
В основе их структуры, так же как и в основе строения холестерина, эргостерина, желчных кислот, витаминов группы D, половых гормонов и ряда других веществ, лежит конденсированная кольцевая система циклопентанпергидрофенантрена.
Установлено, что предшественником кортикостероидов является холестерин(ол) и процесс стероидогенеза, как и нормальное гистологическое строение и масса надпочечников, регулируется АКТГ гипофиза.
Строение и основные этапы синтеза кортикостероидов:
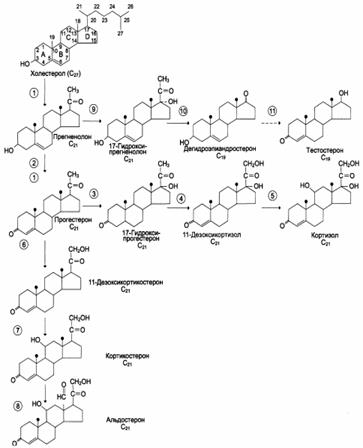 Патологическая биохимия:
Гипогликемия –первичная недостаточность надпочечников (Аддисонова болезнь); вторичная недостаточность надпочечниковвызывается дефицитом АКТГ; избыток глюкокортикоидов(болезнь Кушинга); первичный альдостеронизм(синдром Кона – сниженный ровень ренина и ангиотензина II); вторичный альдостеронизм(повышенный уровень ренина и ангиотензина II); врождённая гиперплазия надпочечников(недостаточность продукции кортизола на фоне гиперпродукции АКТГ);андрогенитальный синдром (гиперпродукция андрогенов).
Гормоны мозгового вещества надпочечников:
дофамин, норадреналин, адреналин(катехоламиновые гормоны).
Эти гормоны – основные элементы реакции «борьбы или бегства».
Патологическая биохимия:гиперпродукция адреналина и норадреналина (феохромоцитомы – опухоли мозгового слоя надпочечников).
Глюкокортикоидыоказывают разностороннее влияние на обмен веществ в разных тканях. В мышечной, лимфатической, соединительной и жировой тканях глюкокортикоиды, проявляя катаболическое действие, вызывают снижение проницаемости клеточных мембран и соответственно торможение поглощения глюкозы и аминокислот; в то же время в печени они оказывают противоположное действие. Конечным итогом воздействия глюкокортикоидов является развитие гипергликемии, обусловленной главным образом глюконеогенезом.
Минералокортикоиды(дезоксикортикостерон и альдостерон) регулируют главным образом обмен натрия, калия, хлора и воды; они способствуют удержанию ионов натрия и хлора в организме и выведению с мочой ионов калия. По-видимому, происходит обратное всасывание ионов натрия и хлора в канальцах почек в обмен на выведение других продуктов обмена, в частности мочевины. Альдостерон получил свое название на основании наличия в его молекуле альдегидной группы у 13-го углеродного атома вместо метильной группы, как у всех остальных кортикостероидов.
Альдостерон – наиболее активный минералокортикоид среди других кортикостероидов; в частности, он в 50–100 раз активнее дезоксикортикостерона по влиянию на минеральный обмен.
Известно, что период полураспада кортикостероидов составляет всего 70–90 мин.
В норме в суточной моче содержится от 10 до 25 мг 17-кетостероидов у мужчин и от 5 до 15 мг – у женщин. Повышенная экскреция их наблюдается, например, при опухолях интерстициальной ткани семенников, тогда как при других тестикулярных опухолях она нормальная. При опухолях коркового вещества надпочечников резко увеличивается экскреция 17-кетостероидов с мочой – до 600 мг в сутки.
Гормоны половых желёз
Половые гормоны синтезируются в основном в половых железах женщин (яичники) и мужчин (семенники); некоторое количество половых гормонов образуется, кроме того, в плаценте и корковом веществе надпочечников.
Женские половые гормоны
Основным местом синтеза женских половых гормонов – эстрогенов (от греч. oistros – страстное влечение) – являются яичники и желтое тело; доказано также образование этих гормонов в надпочечниках, семенниках и плаценте.
В настоящее время открыты 2 группы женских половых гормонов, различающихся своей химической структурой и биологической функцией: эстрогены (главный представитель – эстрадиол) и прогестины (главный представитель – прогестерон).
Наиболее активный эстроген – эстрадиол, синтезируется преимущественно в фолликулах; два остальных эстрогена являются производными эстрадиола и синтезируются также в надпочечниках и плаценте.
Предшественником этих гормонов, как и кортикостероидов, в организме является холестерин.
Ведущую роль в регуляции синтеза эстрогенов и прогестерона играют гонадотропные гормоны гипофиза (фоллитропин и лютропин).
Основная биологическая роль эстрогенов и прогестерона, синтез которых начинается после наступления половой зрелости, заключается в обеспечении репродуктивной функции организма женщины. В этот период они вызывают развитие вторичных половых признаков и создают оптимальные условия, обеспечивающие возможность оплодотворения яйцеклетки после овуляции. Прогестерон выполняет в организме ряд специфических функций: подготавливает слизистую оболочку матки к успешной имплантации яйцеклетки в случае ее оплодотворения, а при наступлении беременности основная роль – сохранение беременности; оказывает тормозящее влияние на овуляцию и стимулирует развитие ткани молочной железы. Эстрогены оказывают анаболическое действие на организм, стимулируя синтез белка.
Патологическая биохимия: первичный гипогонадизм(недостаточность выработки гормонов); вторичный гипогонадизм(выпадение гонадотропной функции гипофиза); дисгенезия гонад (синдром Тернера)(кариотип ХО); синдром поликистозных яичников (синдром штейна-Левенталя) – гиперпродукция андрогенов.
Мужские половые гормоны
Внутрисекреторная функция мужских половых желез была установлена в 1849 г., однако только в 1931 г. А. Бутенандтом из мочи мужчин был выделен гормон в кристаллическом виде
Этот гормон был назван андростероном (от греч. andros – мужчина, а предложенная его химическая структура подтверждена химическим синтезом, осуществленным в 1934 г. одновременно А. Бутенандтом и Л. Ружичкой. Позже из мочи мужчин был выделен еще один гормон – дегидроэпиандростерон, который обладал меньшей биологической активностью. В дальнейшем группа С19-стероидов (состоят из 19 атомов углерода), была названа андрогенами. В то же время гормон, выделенный из ткани семенников, оказался активнее андростерона почти в 10 раз и был идентифицирован в виде тестостерона (от лат. testis – семенник).
Биосинтез андрогенов осуществляется главным образом в семенниках и частично в яичниках и надпочечниках. Основными источниками и предшественниками андрогенов, в частности тестостерона, являются уксусная кислота и холестерин.
Биологическая роль андрогенов в мужском организме в основном связана с дифференцировкой и функционированием репродуктивной системы, причем в отличие от эстрогенов андрогенные гормоны уже в эмбриональном периоде оказывают существенное влияние на дифференцировку мужских половых желез, а также других тканей, определяя характер секреции гонадотропных гормонов у взрослых. Во взрослом организме андрогены регулируют развитие мужских вторичных половых признаков, сперматогенез в семенниках и т.д. Следует отметить, что андрогены оказывают значительное анаболическое действие, выражающееся в стимуляции синтеза белка во всех тканях, но в большей степени в мышцах.
Период полураспада тестостерона не превышает нескольких десятков минут. У взрослых мужчин с мочой экскретируется не более 1% неизмененного тестостерона, что свидетельствует о его расщеплении преимущественно в печени до конечных продуктов обмена.
Патологическая биохимия: гипогонадизм(снижение уровня синтеза тестостерона)
Патологическая биохимия:
Гипогликемия –первичная недостаточность надпочечников (Аддисонова болезнь); вторичная недостаточность надпочечниковвызывается дефицитом АКТГ; избыток глюкокортикоидов(болезнь Кушинга); первичный альдостеронизм(синдром Кона – сниженный ровень ренина и ангиотензина II); вторичный альдостеронизм(повышенный уровень ренина и ангиотензина II); врождённая гиперплазия надпочечников(недостаточность продукции кортизола на фоне гиперпродукции АКТГ);андрогенитальный синдром (гиперпродукция андрогенов).
Гормоны мозгового вещества надпочечников:
дофамин, норадреналин, адреналин(катехоламиновые гормоны).
Эти гормоны – основные элементы реакции «борьбы или бегства».
Патологическая биохимия:гиперпродукция адреналина и норадреналина (феохромоцитомы – опухоли мозгового слоя надпочечников).
Глюкокортикоидыоказывают разностороннее влияние на обмен веществ в разных тканях. В мышечной, лимфатической, соединительной и жировой тканях глюкокортикоиды, проявляя катаболическое действие, вызывают снижение проницаемости клеточных мембран и соответственно торможение поглощения глюкозы и аминокислот; в то же время в печени они оказывают противоположное действие. Конечным итогом воздействия глюкокортикоидов является развитие гипергликемии, обусловленной главным образом глюконеогенезом.
Минералокортикоиды(дезоксикортикостерон и альдостерон) регулируют главным образом обмен натрия, калия, хлора и воды; они способствуют удержанию ионов натрия и хлора в организме и выведению с мочой ионов калия. По-видимому, происходит обратное всасывание ионов натрия и хлора в канальцах почек в обмен на выведение других продуктов обмена, в частности мочевины. Альдостерон получил свое название на основании наличия в его молекуле альдегидной группы у 13-го углеродного атома вместо метильной группы, как у всех остальных кортикостероидов.
Альдостерон – наиболее активный минералокортикоид среди других кортикостероидов; в частности, он в 50–100 раз активнее дезоксикортикостерона по влиянию на минеральный обмен.
Известно, что период полураспада кортикостероидов составляет всего 70–90 мин.
В норме в суточной моче содержится от 10 до 25 мг 17-кетостероидов у мужчин и от 5 до 15 мг – у женщин. Повышенная экскреция их наблюдается, например, при опухолях интерстициальной ткани семенников, тогда как при других тестикулярных опухолях она нормальная. При опухолях коркового вещества надпочечников резко увеличивается экскреция 17-кетостероидов с мочой – до 600 мг в сутки.
Гормоны половых желёз
Половые гормоны синтезируются в основном в половых железах женщин (яичники) и мужчин (семенники); некоторое количество половых гормонов образуется, кроме того, в плаценте и корковом веществе надпочечников.
Женские половые гормоны
Основным местом синтеза женских половых гормонов – эстрогенов (от греч. oistros – страстное влечение) – являются яичники и желтое тело; доказано также образование этих гормонов в надпочечниках, семенниках и плаценте.
В настоящее время открыты 2 группы женских половых гормонов, различающихся своей химической структурой и биологической функцией: эстрогены (главный представитель – эстрадиол) и прогестины (главный представитель – прогестерон).
Наиболее активный эстроген – эстрадиол, синтезируется преимущественно в фолликулах; два остальных эстрогена являются производными эстрадиола и синтезируются также в надпочечниках и плаценте.
Предшественником этих гормонов, как и кортикостероидов, в организме является холестерин.
Ведущую роль в регуляции синтеза эстрогенов и прогестерона играют гонадотропные гормоны гипофиза (фоллитропин и лютропин).
Основная биологическая роль эстрогенов и прогестерона, синтез которых начинается после наступления половой зрелости, заключается в обеспечении репродуктивной функции организма женщины. В этот период они вызывают развитие вторичных половых признаков и создают оптимальные условия, обеспечивающие возможность оплодотворения яйцеклетки после овуляции. Прогестерон выполняет в организме ряд специфических функций: подготавливает слизистую оболочку матки к успешной имплантации яйцеклетки в случае ее оплодотворения, а при наступлении беременности основная роль – сохранение беременности; оказывает тормозящее влияние на овуляцию и стимулирует развитие ткани молочной железы. Эстрогены оказывают анаболическое действие на организм, стимулируя синтез белка.
Патологическая биохимия: первичный гипогонадизм(недостаточность выработки гормонов); вторичный гипогонадизм(выпадение гонадотропной функции гипофиза); дисгенезия гонад (синдром Тернера)(кариотип ХО); синдром поликистозных яичников (синдром штейна-Левенталя) – гиперпродукция андрогенов.
Мужские половые гормоны
Внутрисекреторная функция мужских половых желез была установлена в 1849 г., однако только в 1931 г. А. Бутенандтом из мочи мужчин был выделен гормон в кристаллическом виде
Этот гормон был назван андростероном (от греч. andros – мужчина, а предложенная его химическая структура подтверждена химическим синтезом, осуществленным в 1934 г. одновременно А. Бутенандтом и Л. Ружичкой. Позже из мочи мужчин был выделен еще один гормон – дегидроэпиандростерон, который обладал меньшей биологической активностью. В дальнейшем группа С19-стероидов (состоят из 19 атомов углерода), была названа андрогенами. В то же время гормон, выделенный из ткани семенников, оказался активнее андростерона почти в 10 раз и был идентифицирован в виде тестостерона (от лат. testis – семенник).
Биосинтез андрогенов осуществляется главным образом в семенниках и частично в яичниках и надпочечниках. Основными источниками и предшественниками андрогенов, в частности тестостерона, являются уксусная кислота и холестерин.
Биологическая роль андрогенов в мужском организме в основном связана с дифференцировкой и функционированием репродуктивной системы, причем в отличие от эстрогенов андрогенные гормоны уже в эмбриональном периоде оказывают существенное влияние на дифференцировку мужских половых желез, а также других тканей, определяя характер секреции гонадотропных гормонов у взрослых. Во взрослом организме андрогены регулируют развитие мужских вторичных половых признаков, сперматогенез в семенниках и т.д. Следует отметить, что андрогены оказывают значительное анаболическое действие, выражающееся в стимуляции синтеза белка во всех тканях, но в большей степени в мышцах.
Период полураспада тестостерона не превышает нескольких десятков минут. У взрослых мужчин с мочой экскретируется не более 1% неизмененного тестостерона, что свидетельствует о его расщеплении преимущественно в печени до конечных продуктов обмена.
Патологическая биохимия: гипогонадизм(снижение уровня синтеза тестостерона)
|
Надпочечники состоят из двух индивидуальных в морфологическом и функциональном отношениях частей – мозгового и коркового вещества. Мозговое вещество относится к хромаффинной, или адреналовой, системе и вырабатывает гормоны, которые считаются производными аминокислот. Корковое вещество состоит из эпителиальной ткани и секретирует гормоны стероидной природы.
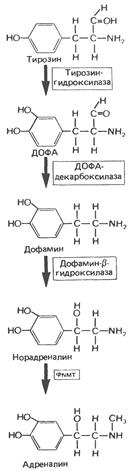
Биосинтез катехоламинов:
ДОФА – дигидроксифенилаланин.
Пониженное выделение 17-кетостероидов с мочой отмечается при евнухоидизме, гипофункции передней доли гипофиза. При аддисоновой болезни у мужчин экскреция 17-кетостероидов резко снижена (от 1 до 4 мг/сут), а у женщин при этом заболевании она практически не наблюдается. При микседеме (гипофункция щитовидной железы) суточное количество экскретируемых 17-кетостероидов близко к минимальному уровню (2–4 мг). Следует указать, однако, что применение гормонов щитовидной железы, хотя и эффективно при лечении основного заболевания, оказывает незначительное влияние на количество экскретируемых с мочой 17-кетостероидов. Обладая противовоспалительной, антиаллергической и антииммунной активностью, глюкокортикоиды нашли широкое применение при лечении таких заболеваний, как бронхиальная астма, ревматоидный артрит, красная волчанка, пузырчатка, сенная лихорадка, различные аутоиммунные болезни, дерматозы и др.
|
| <== предыдущая лекция | | | следующая лекция ==> |
| широчайший спектр используемых средств для завоевания, удержания и реализации власти. | | | Биохимия соединительной ткани |
Дата добавления: 2016-03-04; просмотров: 7096;