Законы идеальных газов
Примеры решения задач
Пример 9.1.4.Газ при давлении 5 ат (Р1) занимает объем, равный 60 м3 (V1). Какой объем займет газ при 15 ат (Р2) и той же температуре?
Решение
Согласно закону Бойля-Мариотта при Т=const P2V2=P1V1
Следовательно:
 м3
м3
Пример 9.1.5.Коксовый газ, образовавшийся в камере коксовой печи, охладился с 1000 до 500С. Во сколько раз уменьшился объем коксового газа, если давление его не изменилось?
Решение
Исходя из закона Гей-Люссака при P=const можно записать

Откуда, принимая конечный объем за 1, получим
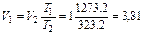 раза.
раза.
Пример 9.1.6.Имеется смесь газов под давлением 30 ат (2,94 МПа). Молярная концентрация первого газа r1=0,4; второго r2=0,2; третьего r3=0,3 и четвертого r4=0,1. Определить парциальное давление этих компонентов в смеси.
Решение
Согласно закону Дальтона Pi=riP, тогда
Р1=0,4∙30=12 ат (1,18) МПа
Р2=0,2∙30=6 ат (0,59) МПа
Р3=0,3∙30=9 ат (0,88) МПа
Р4=0,1∙30=3 ат (0,29) МПа
Итого Р=30 ат (2,94) МПа
Пример 9.1.7.Сжиженный газ состоит из пропана 40%, изо-бутана 25% и н-бутана 35%.
Определить парциальное давление компонентов при 400С и состав паровой фазы.
Решение
Согласно закону Рауля Рi=xiθi (упругость паров θi чистых компонентов при 40 0С равна θ1=1,36 МПа, θ2=0,51 МПа и θ3=0,37 МПа.
Парциальное давление компонентов будет равно (в МПа):
Р1=0,4∙1,36=0,544
Р2=0,25∙0,51=0,126
Р3=0,35∙0,37=0,129
Р=Р1+Р2+Р3=0,544+0,126+0,129=0,799
Согласно уравнению  находим состав паровой фазы:
находим состав паровой фазы:


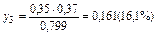 .
.
Пример 9.1.8.Рассчитать состав растворенного в воде при температуре 0 0С газа, состоящего из 90% метана и 10% этана.
Решение
При общем давлении в 0,1 МПа (растворение идет при нормальном давлении) парциальное давление метана будет 0,09, а этана 0,01 МПа. Известно, что при температуре 0 0С в 100 см3 воды растворяется 5,56 см3 метана и 9,87 см3 этана. При указанных выше парциальных давлениях будет растворяться:
метана 0,9∙5,56=4,91 см3
этана 0,1∙9,89=0,99 см3
Итого 5,9 см3
Состав растворенной газовой смеси (в %):
метана 4,91∙100/5,9=83,3
этана 0,99∙100/5,9=16,7.
Дата добавления: 2016-02-27; просмотров: 1501;
