ЗАДАНИЕ 1. Определение величины адсорбции поверхностно-активных веществ на жидкой поверхности методом Ребиндера.
Цель работы.
1. Освоить методику определения поверхностного натяжения жидкостей по методу Ребиндера (с 316-319 ).
2. Определить поверхностное натяжение растворов бутилового спирта разных концентраций.
3. Рассчитать величину адсорбции бутилового спирта на воде и построить изотермы адсорбции и поверхностного натяжения.
4.Сделать выводы о принадлежности бутилового спирта к поверхностно-активным веществам (ПАВ).
ЗАДАНИЕ 2. Определение поверхностного натяжения и установление влияния длины цепи на поверхностное натяжение алифатических спиртов.
Цель работы
.
1. Освоить методику определения поверхностного натяжения жидкостей по методу Ребиндера (с 319 ).
2. Определить поверхностное натяжение спиртов при постоянной температуре.
3. Изобразить графически зависимость числа атомов углерода от поверхностного натяжения.
4. Сделать вывод об экспериментальном подтверждении правила Траубе-Дюкло.
ЗАДАНИЕ 3. Определение величины адсорбции поверхностно-активных веществ на жидкой поверхности методом поднятия жидкости в капилляре.
Цель работы.
1. Освоить методику определения поверхностного натяжения по методу капиллярного поднятия жидкостей (с.320-322 ).
2. Определить поверхностное натяжение растворов бутилового спирта разных концентраций.
3. Рассчитать величину адсорбции бутилового спирта на воде и построить изотермы адсорбции и поверхностного натяжения.
4.Сделать выводы о принадлежности бутилового спирта к поверхностно-активным веществам (ПАВ).
ЗАДАНИЕ 4. Определение поверхностного натяжения и установление влияния длины цепи на поверхностное натяжение алифатических спиртов методом поднятия жидкости в капилляре.
.
Цель работы
.
1. 1. Освоить методику определения поверхностного натяжения й по методу капиллярного поднятия жидкостей ( с.322-323138-139 ).
2. Определить поверхностное натяжение спиртов при постоянной температуре.
3. Изобразить графически зависимость числа атомов углерода от поверхностного натяжения.
4. Сделать вывод об экспериментальном подтверждении правила Траубе-Дюкло.
ЗАДАНИЕ 5. Определение величины адсорбции уксусной ки
Слоты на угле или почве.
Цель работы.
1. Освоить методику определения величины адсорбции из растворов на твердом адсорбенте ( с.323-324).
2. Определить величину адсорбции уксусной кислоты на угле или почве из растворов разной концентрации.
3.Построить изотермы адсорбции по Ленгмюру и Фрейндлиху, определить максимальную адсорбцию и константы адсорбции.
ЗАДАНИЕ 6. Определение обменных катионов Н+ в системе
Почва /раствор.
Цель работы.
1. Изучить методику ионообменного метода исследования (с.324-325).
2. Определить содержание обменного катиона Н+ в почве.
3. Обобщить полученные результаты исследования для разных почв.
ЗАДАНИЕ 7. Определение содержания ионов в пробе питьевой или технической воды в пересчете на анион ОН- методом ионного обмена.
Цель работы.
1. Изучить методику ионообменного метода исследования (с.325-327 ).
2. Определить общее содержание анионов в воде в пересчете на ОН-- ион с помощью анионита ЭДЭ-10П.
3.делать выводы о возможности использования проанализированной воды в питьевых или технических целях.
МЕТОДИКИ ВЫПОЛНЕНИЯ РАБОТ
Задание 1. Определение величины адсорбции поверхностно- активных веществ на жидкой поверхности методом Ребиндера
В термостат Т-прибора для определения поверхностного натяжения помещают пробирку П, заполненную испытуемой жидкостью и закрывают ее пробиркой с капилляром. Пробирка П при помощи бокового отростка соединяется с манометром М и аспиратором С. При истечении воды из аспиратора С в системе создается разряжение. Величину давления измеряют манометром М ( cм. рис. 5.9).
Рис. 9. Установка для определения поверхностного натяжения
При определении постоянной капилляра пробирку П заполняют дистиллированной водой, при этом конец капилляра должен слегка касаться поверхности жидкости (не глубже, иначе нужно вводить поправку на погружение). После установления постоянной температуры выпускают воду из аспиратора с такой скоростью, чтобы воздух проскакивал отдельными пузырьками. В момент проскакивания пузырька замечают разность высоты столбов в левом и правом коленах манометра (hл и hn) и записывают значения Ро=(hл -- hn ). Заменяют дистиллированную воду в пробирке на испытуемую жидкость(растворы бутилового спирта различных концентраций),затем, предварительно промыв ею пробирку и капилляр, точно так же измеряют Рх. Результаты измерений записывают в табл. 5.2
Таблица 5.2 Данные для определения поверхностного натяжения
| Исследуемая жидкость | С, кмоль/м3 | Показание манометра | Р = Δh Δh = /hл -hn/ | σ, Н/м |
| Н2О | 0,000 | 1…1… | 1… | |
| 2…2… | 2…Р0 = | |||
| 3…3… | 3… | |||
| Бутиловый спирт | 0,031 | 1…1… | 1…P1 = | |
| 2…2… | ||||
| 3…3… | ||||
| 0.062 | …. …. | Р2 = | ||
| 0.125 | …. …. | Р3 = | ||
| 0.250 | ……… | Р4 = | ||
| 0.500 | ……… | Р5 = | ||
| 1.000 | ……… | Р6 = |
На основании экспериментальных данных рассчитывают поверхностное натяжение исследуемой жидкости по следующей формуле:
sх = К РХ или sх =s0 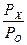 5.11
5.11
По данным таблицы 5.2 и 5.3, вычисляют величину адсорбцию по уравнению Гиббса (ур.5.6);
где СР – определяется как СР(1) = 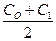 , СР( 2) =
, СР( 2) = 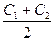 и тд.
и тд.
Δs - рассчитывается - Δs1 = s1–s0, Δs2 = s2 – s1 и тд
ΔС – находится ΔС1=С1 – С0 , ΔС2 =С2 - С1 и тд.
Результатов расчетов записывают в табл. 5.3.
Таблица 5.3
| С, кмоль/м3 | Ср, кмоль/м3 | ΔС | Δσ | Δs/ΔС | Г, кмоль/м3 |
| 0,000 | |||||
| 0,031 | |||||
| 0,062 | |||||
| 0,125 | |||||
| 0,250 | |||||
| и т.д. |
На основании данных табл. 5.2 и 5.3 строят изотермы адсорбции и поверхностного натяжения, откладывая по оси абсцисс значения равновесных концентраций растворов, а по оси ординат – величины адсорбции Г в кмоль/м3 и поверхностного натяжения (d) в Н/м.В заключении по характеру изменения делают вывод о принадлежности бутилового спирта к ПАВ. Если Δσ< 0, а Г будет (+),вещество накапливается в поверхностном слое и является поверхностно - активным (ПАВ).
Если Δσ > 0, Г будет отрицательной - вещество поверхностно - неактивно.
ЗАДАНИЕ 2. Определение поверхностного натяжения 0,1 М раствораспиртов жирного ряда С2Н5ОН, С3Н7ОН, С5Н11ОН, и т.д. проводят методом Ребиндера (см. методику задания 1).
Результаты измерений заносят в табл. 5.4.
Затем рассчитывают поверхностное натяжение спиртов по формуле (5.11) и по результатам строят график, откладывая на оси абсцисс число атомов углерода, а на оси ординат – значения d.
Понятие d в разбавленных растворах может служить мерой поверхностной активности.
Найдя последовательное отношение d спиртов, необходимо показать, во сколько раз уменьшается поверхностное натяжение с удлинением углеродной цепи на группу - СН2 -, т.е., соблюдается ли правило Траубе-Дюкло (с увеличением длины углеводородной цепи на –СН2 –адсорбционная активность возрастает в 3-3,2 раза).
Таблица 5.4. Данные для определения поверхностного
натяжения
| Исследуемая жидкость | С, кмоль/м3 | Показание манометра | Р = Δh Δh = /hл -hn/ | d, Н/м |
| Н 2О | 0,000 | 1…1… | ||
| 2…2… | 2…Р0= | |||
| 3…3… | 3… | |||
| С2Н5ОН | 0,1 | 1…1… | Р 1= Δh1ср | |
| 2…2… | ||||
| 3…3… | ||||
| С3Н7ОН | 0,1 | …. …. | Р2 … | |
| С4Н9ОН | 0,1 | …. …. | Р3 | |
| С5Н11ОН | 0,1 | ……… | Р4 | |
| ………. | ……… | Р5 | ||
| ………… | ……… | Р6 |
Дата добавления: 2016-02-20; просмотров: 1619;
