ЗАДАНИЕ 5. Определение величины адсорбции уксусной кислоты на угле или почве
Для изучения адсорбции уксусной кислоты активизированным углем или почвой определяют ее концентрацию в испытуемом растворе методом титрования до и после адсорбции.
В титровальные колбы отбирают по 10 см3 растворов, добавляют к ним 1-2 капли раствора фенолфталеина и титруют из бюретки 0,1 н раствором щелочи до появления слабой малиновой окраски, не исчезающей в течение одной минуты. Титрование каждого раствора следует проводить в 2-3-х кратной повторности.
Расчет концентрации кислоты в растворах осуществляют, используя усредненные данные результатов титрования, по формуле:
С К = 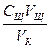 5.15
5.15
где:
Ск – молярная концентрация эквивалента кислоты, моль/дм3;
Сщ – молярная концентрация эквивалента щелочи, моль/дм3;
Vк - объем кислоты, см3;
Vщ - объем щелочи, см3.
Адсорбцию проводят в отдельных колбах, куда помещают по 1 г активированного угля или по 10 г почвы, заливают 50 см3 исходных растворов уксусной кислоты и содержимое перемешивают или встряхивают.
Затем адсорбент отфильтровывают через двойной складчатый фильтр, а фильтрат используют для титрования. Результаты титрования заносят в табл. 5.8.
Таблица 5.8 Результаты титрования при адсорбции.
| Раствор N по порядку | До адсорбции | После адсорбции | |||||||
| Измерение, Vщ | Ск | Измерение, Vщ | Ск | Г | |||||
| среднее | среднее | ||||||||
и по данным рассчитывают величину адсорбции по уравнению Ловица (см ур. 5.8)
При изучении адсорбции из растворов для нахождения константы адсорбции удобнее применять графические выражения уравнения Фрейндлиха и Ленгмюра (см ур. 5.3 -5.5, рис 5.2, 5.3 )
Значение константы К и 1/n находят из графика изотермы адсорбции по Фрейндлиху (см ур. 5.3-5.4, рис 5.3 ) откладывая на оси абцисс значения lgC на оси ординат –lg Х / m.
ЗАДАНИЕ 6. Определение обменных катионов Н+ в системе почва -раствор
10 г воздушно-сухой почвы и 50 см3 дистиллированной воды встряхивают в конической колбе в течение 6 мин. Затем суспензию отфильтровывают через складчатый бумажный фильтр. Последние капли фильтрата наносят на полосу фильтровальной бумаги, добавляют каплю индикатора (метилового оранжевого или фенолфталеина) и проверяют наличие ионов Н+. Если индикатор дает положительную реакцию, то промывку продолжают, приливая еще 10 см3 дистиллированной воды на фильтр с почвой. Операцию продолжают до тех пор, пока индикатор не дает отрицательную реакцию на ионы Н+.
Отмытую от свободный ионов Н+, почву с фильтра переносят снова в коническую колбу, смывают почву с фильтра 50 см3 1,0 н KCl, энергично встряхивают и фильтруют через бумажный складчатый фильтр в мерную колбу объемом 50 см3. Фильтрат доводят до метки водой и, отобрав 25 см3, добавляют индикатор (фенолфталеин) и титруют 0,001 н NaOH до изменения окраски индикатора. Титрование повторяют, данные заносят в табл. 5.6.
Таблица 5.9. Результаты титрования при ионном
Обмене
| Объем отобранного фильтрата Vк, см3 | Ср(щ), моль/дм3 | Vщ, см3 | Сн(к), моль/дм3 | Vф, см3 | mН, г | |
| 1 титрование | 2 титрование | |||||
По усредненным данным титрования рассчитывают концентрацию ионов Н+ в фильтрате, используя формулу (5.15).
Затем определяют содержание Н+ в почвенном растворе и по уравнению:
mx = CH+VФЭХ 10-3 5.16
где Vф - общий объем фильтрата, см3;
Эх – эквивалент определяемого иона (Э(Н+) =1)
Почва, как известно, состоит из органической и минеральной части. Содержащиеся в почве в поглощенном состоянии ионы водорода могут обмениваться в эквивалентных количествах на любые другие ионы. Общее уравнение ионного обмена Б.П.Никольского (ур. 5.10).
При обмене ионов Н+ в почве происходит процесс
ПН++ К+ + Cl— → ПК++ Н+ + Cl—.
Вытесненный ион Н+ и определяется титрованием. Сделайте выводы.
Количественная характеристика ионного обмена в почве впервые изучена К.К.Гедройцем.
ЗАДАНИЕ 7. Определение содержания ионов в пробе питьевой или технической воды в пересчете на анион ОН-
Для определения общего количества анионов в исследуемом растворе, в основном, используются аниониты, которые предварительно переводят в ОН- форму. Для этого через предварительно набухшей под водой анионит ЭДЭ-10П, находящийся в ионообменной колонке, пропускают 10 см31 н раствора NaОН.
Затем анионит отмывают от не поглощенных ионов ОН- небольшими порциями дистиллированной воды до отрицательной реакции по фенолфталеину. Для проверки на полноту промывания каплю фильтрата помещают на предметное стекло и добавляют к ней одну каплю фенолфталеина. Отсутствие окраски при этом свидетельствует о полноте промывания анионита от ионов ОН-.
Во всех случаях пропускания через ионообменную колонку жидкостей над анионитом следует оставлять столбик жидкости 1-1,5 см, иначе в колонке могут образоваться воздушные пузырьки, которые уменьшат ее емкость и затруднят прохождение жидкости через ионит.
Испытуемую жидкость (питьевую или техническую воду) в объеме 25 см3 пропускают через подготовленный анионит и промывают его 2-3 раза небольшими порциями дистиллированной воды. Фильтрат и промывные воды собирают в мерную колбу объемом 50 см3.
Раствор доводят до метки дистиллированной водой, отбирают 25 см3, добавляют 1-2 капли индикатора (фенолфталеин) и титруют из бюретки 0,01 н раствором кислоты (НCl) до исчезновения малиновой окраски. Титрование повторяют, а данные заносят в табл. 5.10
По среднему значению Vк-ты, пошедшего на титрование, рассчитывают концентрацию ионов ОН- в пробе из выражения:
СН+ *Vк-ты
Сон- = ————— 5.17
Vпр
Затем рассчитывают содержание ионов ОН- ионов в 25 см3 взятой на анализ воды:
mОН-= СОН _ VФ ЭОН _ 10 -3 г / 25 см3 воды. 5.18
Таблица 5.10. Результаты титрования при анионном обмене
| Объем отобранного фильтрата Vпр, см3 | СН+ , моль/дм3 | Объем кислоты, пошедшей на титрование Vк-ты, см3 | Спробы на ОН-ион, моль/дм3 | Vф, см3 | mОН-, г | ||
| 1 титрование | 2 титрование | среднее | |||||
Далее выражают mОН_ на 1 дм3 (1 л) питьевой или технической воды и делают вывод об общем содержании анионов в пробе в пересчете на ОН—ион.
На границе раздела раствор сильного электролита и полярное твердое тело (анионит) возникает двойной электрический слой. Ионы внешней обкладки этого слоя, сравнительно слабо связанные с твердой фазой силами электростатического взаимодействия, могут обмениваться с одноименными ионами из раствора в эквивалентных количествах.
Процессы ионного обмена на твердой поверхности характеризуются уравнениям Б.П. Никольского (см. ур –ние 5.10).
При обмене анионов в пробе с анионитом в ОН- форме происходит процесс, который схематично можно записать:
Cl- │Cl-
 Анионит X OH— +SO42- ® Анионит SO42 + X OH—
Анионит X OH— +SO42- ® Анионит SO42 + X OH—
CO32- и др │ CO32
и др.
Концентрация ОН- анионов определяется титрованием HCl и будет характеризовать суммарное количество анионов в пробе воды в перерасчете на ион ОН-.
ТЕМА 6.
КОЛЛОИДНЫЕ СИСТЕМЫ
ВВЕДЕНИЕ
Коллоидная химия изучает физико-химические свойства гетерогенных высокодисперсных систем и высокомолекулярных соединений в твердом состоянии и в растворах. Коллоидная химия — важный самостоятельный раздел физической химии. Коллоидная химия уделяет особое внимание роли поверхностных явлений на границе раздела фаз.
В настоящее время коллоидная химия занимается уже не только химическим строением и химическими реакциями, протекающими в коллоидных системах, но и физической структурой, физическими (и даже механическими) свойствами и физико-химическими процессами, характерными для высокодисперсных и высокомолекулярных систем. Вот почему правильнее было бы назвать этот раздел науки более общим термином — физическая химия дисперсных систем.
Из курса физической химии известно, что если одно вещество в более или менее раздробленном (дисперсном) состоянии равномерно распределено в массе другого вещества, то систему называют дисперсной. Раздробленное вещество в этом случае называют дисперсной фазой, а среду, в которой оно распределено, — дисперсионной средой. Так, система, представляющая собой взмученную в воде глину, состоит из взвешенных мелких частиц глины — дисперсной фазы и воды — дисперсионной среды.
Для характеристики и классификации различных дисперсных Систем в практике широко пользуются понятием степень дисперсности D, которая определяется как величина, обратная величине размера (диаметра) дисперсной частицы a:D=l/a м-1. Отсюда следует, что степень дисперсности есть величина, показывающая, какое число частиц можно уложить вплотную в 1 м.
Иногда применяется и другая характеристика степени дисперсности — так называемая удельная поверхность, которая представляет собой отношение поверхности S данного тела к занимаемому объему V, т. е. Sуд.=S/V, где Sуд. — удельная поверхность. С повышением степени дисперсности величина удельной поверхности быстро растет.
дисперсные системы по величине частиц дисперсной фазы и по степени дисперсности можно разделить условно на три группы: грубодисперсные, коллоидно-дисперсные и молекулярно (ионно)-дисперсные (табл. 6.1).
Дисперсные системы третьей группы, известные под общим названием истинных или молекулярных растворов, всесторонне исследуются в физической химии. Эти системы являются наиболее изученными, так как сравнительно просты по составу и структуре (дискретными единицами в них являются либо простые молекулы, либо ионы), а поведение определяется простыми и четкими
закономерностями. Молекулярно- и ионно-дисперсные системы могут образоваться самопроизвольно; они являются системами равновесными и термодинамически устойчивыми, подчиняющимися правилу фаз.
Таблица 6.1

Вторая группа дисперсных систем, получивших название коллоидно-дисперсных, является основным объектом изучения коллоидной химии. Системы этой группы получили название коллоидов или коллоидных систем. Структурной и кинетической единицей в них являются не ион и не молекула в общем смысле, а либо комплекс (агрегат), состоящий из обычных молекул, атомов или ионов, называемых мицеллой, либо макромолекула, т. е. молекула-полимер «гигантских» размеров ~100÷1 нм, обладающая молекулярной или частичной массой в десятки и сотни единиц.
С увеличением относительной молекулярной массы в дисперсных системах второй группы можно ожидать новых качественных изменений, т. е. появления новых,более сложных свойств, которые
Таблица 6.2
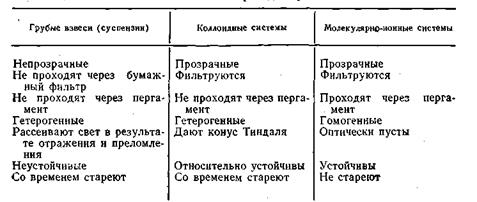
не укладываются в закономерности более простых систем третьей группы. По мере изменения размеров частиц от наиболее крупных (грубодисперсных) к мелким и обратно соответственно изменяются кинетические, оптические, каталитические и другие свойства дисперсных систем. В табл. 6.2 приведены изменения некоторых свойств различных дисперсных систем.
Из этой таблицы следует, что коллоидно-дисперсные системы в отличие от истинных растворов сами по себе агрегативно неустойчивы. Размеры их дисперсных частиц могут изменяться как самопроизвольно, так и под влиянием внешних факторов. Одной из причин неустойчивости коллоидных растворов является их гетерогенность. Обладая громадной суммарной поверхностью, следовательно, большой свободной энергией, коллоидные системы согласно второму началу термодинамики стремятся к равновесному состоянию, характеризующемуся разделением системы на две фазы, имеющие минимальные межфазовые поверхности и минимальную свободную поверхностную энергию.
Агрегативная устойчивость коллоидно-дисперсных систем повышается, если на поверхности коллоидных частиц за счет свободной поверхностной энергии адсорбируются молекулы (ионы) третьего компонента системы – стабилизатора, Так, если в пробирку с водой ввести небольшое количество растительного масла, при встряхивании образуется эмульсия, которая быстро расслаивается снова на два слоя – масло и вода. Неустойчивость эмульсии объясняется самопроизвольным уменьшением суммарной поверхности за счет слипания мелких капелек масла в более крупные. Однако если ввести в эту смесь небольшое количество 2%-ного раствора мыла и хорошо встряхнуть, образуется стойкая эмульсия белого цвета. Мыло в данном случае играет роль стабилизатора.
В отличие от коллоидно-дисперсных систем высокомолекулярные системы значительно более устойчивы: они дают при смешении с растворителями молекулярные растворы, подобные обычным растворам низкомолекулярных веществ, но с очень длинными цепными молекулами. Такие растворы являются гомогенными системами, они образуются самопроизвольно, потому что сам процесс растворения идет с уменьшением свободной энергии и не требует наличия стабилизатора. Растворы высокомолекулярных соединений являются термодинамически равновесными и потому обратимыми системами.
Гетерогенные коллоидно–дисперсные и гомогенные высокомолекулярные системы обладают целым рядом общих свойств, что и делает их объектом изучения коллоидной химии.
Во многом близки к коллоидно–дисперсным системам и изучаются теми же методами суспензии, эмульсии и пены (D ≈ 105 ÷ 107 м-1). Хотя эти системы и обладают рядом особых специфических свойств, однако их следует причислить именно к коллоидным системам.
Коллоиды очень широко распространены в природе и играют важную практическую роль, чем и определяется не только научное, но и народнохозяйственное значение коллоидной химии. Драгоценные камни, а также другие минералы в недрах земли, пищевые продукты, одежда, обувь, дым, облака, мутная вода в природных водоемах, почва, глина – все это не что иное, как коллоидные системы. Такие биологические жидкости, как кровь, плазма, лимфа, спинно – мозговая жидкость, белки, крахмал, слизи и камеди, являются коллоидами.
Существенную роль играют коллоиды в промышленности, главным образом в таких ее отраслях, как добыча и переработка нефти, металлургическая промышленность, горнорудное дело, производство различных строительных материалов и пластмасс, синтетических волокон, синтетического каучука и резины, текстильная, лакокрасочная и пищевая промышленность, мыловаренное производство и т.д. Такие важные для промышленности технологические процессы, как обогащение полезных ископаемых путем флотации, механическая и термическая обработка металлов, технология фотографических и кинематографических процессов, имеют прямое отношение к коллоидно–дисперсным системам. В фармацевтической и парфюмерной промышленности многие лекарственные и бытовые препараты производятся в виде паст, кремов, мазей, тонких суспензий и эмульсий.
Исключительно важное значение имеет коллоидная химия в геологии. Представления о коллоидном состоянии вещества способствуют более углубленному пониманию процессов образования минералов, различных руд, горных пород и т. п.
В области почвоведения многие проблемы, например процессы ионного обмена, строение и свойства почвенного поглощающего комплекса, биохимия гумуса и др., также тесно связаны с коллоидной химией. Закономерности, устанавливаемые ею, дают возможность агроному не только глубже понимать процессы, протекающие в почве, но и в известной мере сознательно их изменять в желаемом направлении.
Велика роль коллоидной химии в вопросах химической защиты растений от различных вредителей и сорняков. В целях более высокой эффективности различные ядохимикаты применяются в виде суспензий, эмульсий, дымов и туманов (аэрозолей). Вот почему в системе агрономического образования коллоидной химии уделяется большое внимание. Такие важные для подготовки агронома научные дисциплины, как почвоведение, агрохимия, физиология растений и животных, метеорология, биохимия, микробиология и др., широко пользуются основными положениями и методами коллоидной химии.
Краткая история развития коллоидной химии. Как самостоятельная научная дисциплина коллоидная химия возникла в начале XX в., однако практические сведения о коллоидах можно найти уже в работах Аристотеля и алхимиков. Многие коллоидные системы и их свойства были хорошо известны человеку в глубокой древности и широко им использовались. Однако до середины XIX в., несмотря на успешное развитие естествознания, изучение и понимание коллоидов продвинулось очень мало. Объясняется это не только сложностью коллоидных систем, но и тем, что в XVIII и начале XIX вв. в естествознании господствовали идеалистические и вульгарно-механистические взгляды на сложные явления природы вроде учения о «жизненной силе» и т. п.
Русские ученые внесли неоценимый вклад в создание основ коллоидной химии. Так, в трудах М. В. Ломоносова (1751) четко различались явления кристаллизации и свертывания (коагуляция) растворов, описаны способы получения и свойства коллоидных растворов в воде и стекле (его знаменитые цветные стекла по существу являются твердыми растворами). Позднее Т. Е. Ловиц (1789) впервые открыл одно из важнейших явлений, на которых основана коллоидная химия,— адсорбцию из растворов на твердом адсорбенте (угле). Это свойство угля Ловиц успешно использовал в практических целях для осветления сахарного сиропа и растительных масел, а также для очистки селитры, которая применялась в производстве пороха.
В 1808 г. профессор Московского университета Ф. Ф. Рейсс впервые установил факт движения частичек дисперсной фазы и дисперсионной среды под влиянием внешнего электрического поля. Эти работы легли в основу изучения электрокинетических свойств коллоидно-дисперсных систем.
Большое значение имели работы итальянского химика Сельми, который еще в 1845 г., исследуя свойства различных растворов, заметил, что биологические жидкости — сыворотка, молоко, кровь, лимфа и другие — резко отличаются по своим свойствам от обычных истинных растворов; они были им названы псевдорастворами. Сельми доказал, что характерным отличием псевдорастворов (или ложных растворов) от истинных растворов является то, что образование их не сопровождается самопроизвольным раздроблением вещества на молекулы. Не менее важное значение имели работы Фарадея, который впервые (1857) открыл явление, получившее впоследствии название «эффекта Фарадея», а также разгадал секрет древних алхимиков — способ получения коллоидных растворов золота.
Однако началом классического периода в развитии коллоидной химии следует считать работы английского химика Грэма (1861), которого по праву считают «отцом» коллоидной химии. Он ввел термин и определил понятие «коллоиды, причем в отличие от обычных истинных растворов коллоидные растворы были названы Грэмом золями.
Профессор Киевского университета И. Г. Борщов (1833—1878) независимо от Грэма дал определение сущности коллоидного раствора (золя) и коллоидной частицы.
Позднейшие исследования подтвердили правоту высказывания И. Г. Борщова о том, что правильнее говорить не о коллоидах как об особой группе веществ, а о коллоидном состоянии вещества.. Эту идею об универсальности коллоидного состояния вещества окончательно развил и экспериментально обосновал другой русский ученый П. П. Веймарн, которому удалось получить в коллоидном состоянии огромное количество веществ, считавшихся до него типичными кристаллоидами. Так, раствор мыла в воде обладает свойствами коллоида, а мыло растворенное в спирте, проявляет свойства истинных растворов. Аналогично этому типичный кристаллоид — поваренная соль, растворенная в воде, дает истинный раствор, а в бензоле — коллоидный раствор и т. п. В настоящее время любое вещество можно получить в коллоидном состоянии. Поэтому нельзя говорить о коллоидных веществах, а следует говорить о коллоидном состоянии тех или иных веществ.
Начало современного этапа развития коллоидной химии тесно связано с целым рядом замечательных открытий в области физики и смежных с ней наук в первые два десятилетия нашего века. За этот период произошла переоценка многих классических представлений. В учении о коллоидах в этот период на первый план выступает изучение поверхностносорбционных явлений. Эти явления были подробно исследованы русскими учеными А. А. Титовым (1910) и Н. А. Шиловым (1916), а также зарубежными — Ленгмюром (1917) и др. Успешное применение советским ученым А. В. Думанским центрифуги для изучения коллоидных систем послужило мощным толчком к разработке метода ультрацентрифугирования, который, по существу, является одним из важнейших современных методов исследования коллоидных растворов.
В решении проблемы устойчивости коллоидных систем и их коагуляции наряду с выдающимися работами таких крупных зарубежных ученых, как Дюкло, Фрейндлих и Кройт, весомый вклад внесли и наши советские ученые Н. П. Песков, А. И. Рабинович, П. А. Ребиндер и многие другие.
Большую известность у нас и за рубежом приобрели работы С. М. Липатова и В. А. Каргина в области исследования высокомолекулярных соединений. В частности, В. А. Каргин и его сотрудники подробно исследовали механизм процесса образования коллоидных частиц, экспериментально доказав наличие двух стадий в этом процессе.
В области исследования поверхностно-сорбционных слоев коллоидных систем большое значение приобрели работы А. Н. Фрумкина, Б. В. Дерягина и других советских ученых.
В нашей стране впервые были выполнены обширные и всесторонние исследования почвенных коллоидов. Выдающиеся работы К. К. Гедройца явились основополагающими в учении о почвенном поглощающем комплексе. Дальнейшее развитие наука о почвенных коллоидах получила в работах В. Р. Вильямса, А. Ф. Тюлина, И. Н. Антипова-Каратаева, А. Н. Соколовского, Н. П. Ремезова, С. Н. Алешина, Н. И. Горбунова, А. В. Петербургского и других советских ученых. Из зарубежных исследователей необходимо отметить работы Г. Вигнера и С. Маттсона.
Дата добавления: 2016-02-20; просмотров: 2156;
