Общая характеристика элементов
Элементы фтор, хлор, бром, иод, астат составляют главную подгруппу VII группы – семейство галогенов (в переводе с греческого соль рождающие). Объясняется их способностью образовывать бинарные соединения типа NaCl за счёт проявления ими окислительных свойств.
На внешнем уровне у них 7 электронов ns2np5, электронная конфигурация обусловливает характерную степень окисления всех элементов в их соединениях (-1). В то же время для хлора, брома и иода известны соединения, где их степени окисления имеют положительные значения: +1, +3, +5, +7. 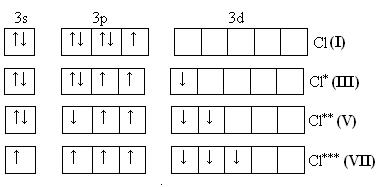
До завершения оболочки не достаёт 1 электрона. Поэтому галогены – сильные окислители. Это типичные неметаллы (за исключением At, и отчасти иода). Обладают большим сродством к электрону (сродство к электрону – энергия, которая выделяется при присоединении к атому одного электрона).
Легко присоединяют электрон Э + е- = Э- , достраивая электронную оболочку до устойчивой оболочки атомов ближайших благородных газов. Радиус иона больше радиуса атома, так как при присоединении электронов радиус увеличивается. Окислительная способность (т.е. способность присоединять электроны у галогенов уменьшается от F к At). Поэтому фтор вытесняет все следующие за ним галогены, у йода и астата появляются металлические признаки.
При обычных условиях галогены существуют в виде простых веществ, состоящих из двухатомных молекул типа Наl2  - F2 , Cl2 , Br2 , I2.
- F2 , Cl2 , Br2 , I2.
Сила связи Э – Э уменьшается вниз по группе за исключением связи F – F, которая неожиданно слабее (причина этого, по-видимому, состоит в более близком расположении неподелённых электронных пар из-за малых размеров атома фтора, отталкивание неподелённых электронных пар ослабляет связь). В Cl2 , Br2 , I2 – дативная связь дополнительная, за счёт спаренных p-электронов одного атома и вакантных d-орбиталей другого.
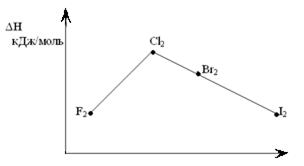
Аномальное изменение энергии связи связано с различными размерами атомов. ЕF2 < ECl2 за счёт малых размеров атома F. На близком расстоянии атомы отталкиваются друг от друга. С одной стороны в молекуле Cl2 действуют силы отталкивания между неподелёнными электронными парами, находящихся на близком расстоянии. Самой прочной молекулой является молекула Cl2. Это связано с тем, что в дополнение к образованию связи по спин-валентному механизму, происходит добавочное взаимодействие свободных электронных пар одного атома хлора со свободной d орбиталью другого - по донорно-акцепторному механизму. Такие дополнительные связи называются дативными и приводят к упрочнению молекулы. 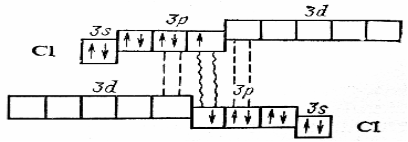
Уменьшение энергии связи от Cl2 к I2 объясняется увеличением расстояний между атомами. Увеличение tплавл. связано с тем, что с увеличением размера атома возрастает поляризуемость молекул и усиливается способность к межмолекулярному взаимодействию, а чем более прочная связь между молекулами, тем более высокая tплавл..
Физические свойства галогенов существенно различаются: так, при нормальных условиях F2 – зеленовато – жёлтый, трудно сжижаемый газ с резким запахом. Фтор крайне токсичен, при попадании а организм человека вызывает отёк лёгких, разрушение зубов, ногтей, ломкость кровеносных сосудов, повышает хрупкость костей.
Cl2 – также газ желто – зеленого цвета, но сжижается легко; Br2 – красно- коричневая густая жидкость со зловонным запахом, ядовит (единственный жидкий при обычных условиях неметалл). I2 – фиолетовые кристаллы. Для человека смертельная доза 2-3 г йода, но в форме иодид - ионов безвреден.
Общая характеристика VII группы
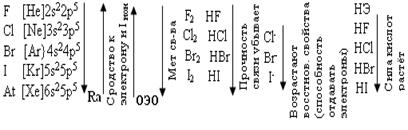
Галоводороды - летучие водородные соединения галогенов, хорошо растворимы в воде, ведут себя в водных растворах как кислоты. Сила кислот (способность к диссоциации на ионы) растёт сверху вниз, т. к. уменьшается прочность связи Н – Э в молекулах от F к At.
Дата добавления: 2016-01-30; просмотров: 1829;
