Бор. Получение. Химические свойства
Бор по своим свойствам наиболее схож с элементом IV-A группы кремнием («диагональное сходство»).
Бор – кристаллическое вещество, черного цвета, тугоплавкое при t = 2300 С.
Наиболее распространены две модификации бора: аморфный и кристаллический. Аморфная модификация наиболее реакционноспособна.
Получение бора
1. Термическое разложение гидридов бора:
B2H6  2B + 3H2
2B + 3H2
2. Магнийтермией из оксида бора:
B2O3 + 3Mg  3MgO + 2B
3MgO + 2B
B2O3 + Zn  ZnO + B
ZnO + B
3. Из хлорида бора:
2BCl3 + 3Zn  3ZnCl2 + 2B
3ZnCl2 + 2B
Непосредственно активно бор реагирует только со фтором, однако при нагревании протекает взаимодействие с кислородом, азотом, углеродом.
B + 2F2 → BF4
4B + 3O2 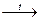 2B2O3
2B2O3
2B + N2 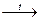 2BN
2BN
4B + 3C 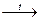 B4C3
B4C3
Бор реагирует с горячими концентрированными кислотами H2SО4 и HNO3
B + H2SO4конц. → H3BO3 + SO2↑ + H2O
B + HNO3конц. → H3BO3 + NO2↑ + H2O
Со щелочами реагирует только в присутствии сильных окислителей:
B + NaOH + H2O2 → NaBO2 + H2O
Однако аморфный бор может реагировать со щелочами при кипячении:
Bаморфн. + NaOH 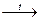 NaBO2 + H2↑
NaBO2 + H2↑
SiO2 + B → Si + B2O3
Галогениды бора
BF3 BCl3 BBr3 BI3
газ газ жидкость твердый
Ecвязи кДж 644 443 376 284
 устойчивость падает
устойчивость падает
ВСl3 образуется посредством взаимодействия трех электронов атома бора в возбужденном состоянии. Образуется три связи по спин - валентному (обменному) механизму.
|
|
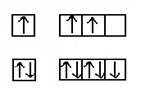
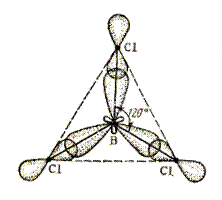
Так как в галогениде BГal3 имеется свободная орбиталь за счет атома бора, то в этом случае молекула BГal3 может быть акцептором электронной пары и участвовать в образовании связи по донорно-акцепторному механизму.
|
|


Ион имеет тетраэдрическую структуру
|

Галогениды бора имеют кислотный характер и гидролизуются:
BCl3 + H2O → H3BO3 + HCl
BF4 + HF → H[BF4] (сильная кислота)
Кислотные галогениды реагируют с основными галогенидами:
ВF3 + NaF = Na[BF4]
С водородом бор непосредственно не реагирует. Гидриды бора получают не прямым взаимодействием с водородом, а косвенным путем.
Например, действием соляной кислоты на борид магния.
Мg3В2 + 6HCl ® В2Н6 +3МgCl2
Получается смесь бороводородов (боранов). Бораны известны газообразные, жидкие и твердые.
В2Н6 – диборан – газ
В4Н10 – тетраборан – жидкость
В10Н14– твердый боран.
Они имеют неприятный запах и очень ядовиты. Большинство из них самовоспламеняются и разлагаются водой.
2В4Н10 + 11 О2 = 4В2О3 + 10 Н2О
В2Н6 + 6 Н2О = 2Н3ВО3 + 6Н2
В молекулах бороводородов атомы бора связаны водородными «мостиками».
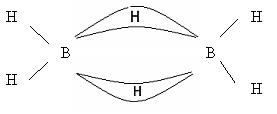
Бораны – особый вид соединений, в них образуется электроннодефицитная связь. В их молекулах электронов меньше, чем необходимо для образования двухэлектронных связей. Это так называемая «банановая связь», образуется в результате перекрывания двух sp3-гибридных орбиталей атомов бора и одной s-орбитали атома водорода. Каждый мостиковый атом водорода образует с двумя атомами бора общую двухэлектронную трехцентровую связь В – Н – В.
Соединения с дефицитом электронов являются акцепторами электронов.
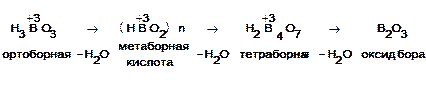
при температуре 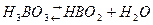
4НВО2 = Н2В4О7 + Н2О
Н2В4О7 = 2В2О3 + Н2О
H2B4O7 ↔ 2H+ + B4O72-
(кислых солей не образует)
В отличие от обычных кислот ортоборная кислота не отщепляет Н+, а вызывает смещение равновесия диссоциации воды, присоединяя за счет донорно-акцепторного взаимодействия OH-, выступает в роли одноосновной.
B(OH)3 + H2O → B(OH)4- + H+ Кд = 5,8 ·10-10
Координационное число бора по кислороду равно 3, поэтому кислородные соединения бора образуют полимерные соединения (полибораты).
Все кислоты превращаются в ортоборную:
HBO2 + H2O → H3BO3
H2B4O7 + 5H2O → 4H3BO3
Если ортоборная наиболее устойчивая кислота, то соли ее не существуют в обычных условиях по сравнению с солями мета- и тетраборной кислот. Так при действии на раствор борной кислоты гидроксидом натрия получается не ортоборат, а тетраборат натрия (при недостатке NaOH) или метаборат (в избытке NaOH):
2NaOHнед + 4H3BO3 = Na2B4O7 + 7 H2O
NaOHизб + H3BO3 = NaBO2 + 2H2O
При избытке щелочи образующийся тетраборат натрия превращается в метаборат натрия:
Na2B4O7 + 2NaOHизб = 4NaBO2 + H2O
Кислотный гидролиз тетрабората натрия приводит к образованию ортоборной кислоты:
Na2B4O7 + 2HCl + 5 H2O = 2NaCl + 4 H3BO3
Алюминий
По содержанию в земной коре занимает первое место среди металлов и третье среди всех элементов, после кислорода и кремния.
Металлические свойства его выражены сильнее, чем у бора. Химические связи алюминия с другими металлами в основном ковалентного характера. Тип кристаллической структуры - ГПУ.
В отличие от бора атом алюминия имеет свободные d-подуровни на внешнем уровне. У Al3+ небольшой радиус и довольно высокий заряд, за счет чего он является комплексообразователем с координационным числом 4 или 6. Соединения Al более устойчивы, чем бора.
Получение алюминия
В промышленности Al получают электролизом расплава Al2O3 в криолите (Na3AlF6)
Al2O3 → Al+3 + AlO3-3
K (-) Al+3 + 3e = Al0
A (+) 2AlO3-3 – 6e = Al2O3 + 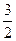 O2
O2
Ga, In, Tl – рассеянные элементы, встречаются в оксидных и сульфидных рудах. В этом случае соответствующие соединения концентрируют и действуют восстановителями.
Э2O3 + 3H2 → 2Э + 3H2O
Э2O3 + CO → 2Э + CO2
Дата добавления: 2016-01-30; просмотров: 8128;
