Законы идеального газа. Аннотация: традиционное изложение темы, дополненное демонстрацией на компьютерной модели.
Аннотация: традиционное изложение темы, дополненное демонстрацией на компьютерной модели.
Из трех агрегатных состояний вещества наиболее простым является газообразное состояние. В газах силы, действующие между молекулами, малы и при определенных условиях ими можно пренебречь.
Газ называется идеальным, если:
- можно пренебречь размерами молекул, т.е. можно считать молекулы материальными точками;
- можно пренебречь силами взаимодействия между молекулами (потенциальная энергия взаимодействия молекул много меньше их кинетической энергии);
- удары молекул друг с другом и со стенками сосуда можно считать абсолютно упругими.
Реальные газы близки по свойствам к идеальному при:
- условиях, близких к нормальным условиям (t = 00C, p = 1.03·105 Па);
- при высоких температурах.
Законы, которым подчиняется поведение идеальных газов, были открыты опытным путем достаточно давно. Так, закон Бойля - Мариотта установлен еще в 17 веке. Дадим формулировки этих законов.
Закон Бойля - Мариотта. Пусть газ находится в условиях, когда его температура поддерживается постоянной (такие условия называются изотермическими).Тогда для данной массы газа произведение давления на объем есть величина постоянная:
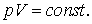
Эту формулу называют уравнением изотермы. Графически зависимость p от V для различных температур изображена на рисунке.
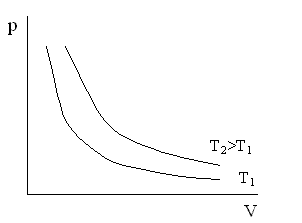
Свойство тела изменять давление при изменении объема называется сжимаемостью. Если изменение объема происходит при T=const, то сжимаемость характеризуетсяизотермическим коэффициентом сжимаемости 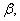 который определяется как относительное изменение объема, вызывающее изменение давления на единицу.
который определяется как относительное изменение объема, вызывающее изменение давления на единицу.
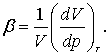
Для идеального газа легко вычислить его значение. Из уравнения изотермы получаем:
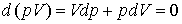
и тогда

Знак минус указывает на то, что при увеличении объема давление уменьшается. Т.о., изотермический коэффициент сжимаемости идеального газа равен обратной величине его давления. С ростом давления он уменьшается, т.к. чем больше давление, тем меньше у газа возможностей для дальнейшего сжатия.
Закон Гей - Люссака. Пусть газ находится в условиях, когда постоянным поддерживается его давление (такие условия называются изобарическими). Их можно осуществить, если поместить газ в цилиндр, закрытый подвижным поршнем. Тогда изменение температуры газа приведет к перемещению поршня и изменению объема. Давление же газа останется постоянным. При этом для данной массы газа его объем будет пропорционален температуре:
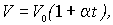
где V0 - объем при температуре t = 00C, 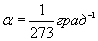 - коэффициент объемного расширения газов. Его можно представить в виде, аналогичном коэффициенту сжимаемости:
- коэффициент объемного расширения газов. Его можно представить в виде, аналогичном коэффициенту сжимаемости:
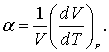
Графически зависимость V от T для различных давлений изображена на рисунке.
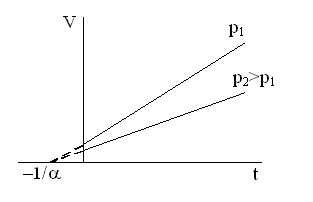
Перейдя от температуры в шкале Цельсия к абсолютной температуре 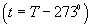 , закон Гей - Люссака можно записать в виде:
, закон Гей - Люссака можно записать в виде:
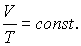
Закон Шарля. Если газ находится в условиях, когда постоянным остается его объем (изохорические условия), то для данной массы газа давление будет пропорционально температуре:
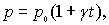
где р0 - давление при температуре t = 00C, 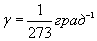 - коэффициент давления. Он показывает относительное увеличение давления газа при нагревании его на 10:
- коэффициент давления. Он показывает относительное увеличение давления газа при нагревании его на 10:
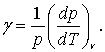
Закон Шарля также можно записать в виде:

Закон Авогадро: один моль любого идеального газа при одинаковых температуре и давлении занимает одинаковый объем. При нормальных условиях (t = 00C, p = 1.03·105 Па) этот объем равен 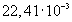 м-3/моль.
м-3/моль.
Число частиц, содержащихся в 1 моле различных веществ, наз. постоянная Авогадро:
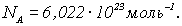
Легко вычислить и число n0 частиц в 1 м3 при нормальных условиях:

Это число называется числом Лошмидта.
Закон Дальтона: давление смеси идеальных газов равно сумме парциальных давлений входящих в нее газов, т.е.
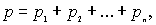
где 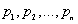 - парциальные давления - давления, которые бы оказывали компоненты смеси, если бы каждый из них занимал объем, равный объему смеси при той же температуре.
- парциальные давления - давления, которые бы оказывали компоненты смеси, если бы каждый из них занимал объем, равный объему смеси при той же температуре.
Уравнение Клапейрона - Менделеева. Из законов идеального газа можно получить уравнение состояния, связывающее Т, р и V идеального газа в состоянии равновесия. Это уравнение впервые было получено французским физиком и инженером Б. Клапейроном и российским учеными Д.И. Менделеевым, поэтому носит их имя.
Пусть некоторая масса газа занимает объем V1, имеет давление p1 и находится при температуре Т1. Эта же масса газа в другом состоянии характеризуется параметрами V2, p2, Т2 (см. рисунок). Переход из состояния 1 в состояние 2 осуществляется в виде двух процессов: изотермического (1 - 1') и изохорического (1' - 2).
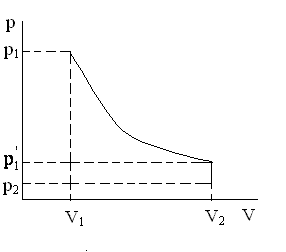
Для данных процессов можно записать законы Бойля - Мариотта и Гей - Люссака:
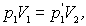

Исключив из уравнений p1', получим
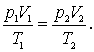
Так как состояния 1 и 2 были выбраны произвольно, то последнее уравнение можно записать в виде:
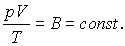
Это уравнение называется уравнением Клапейрона, в котором В - постоянная, различная для различных масс газов.
Менделеев объединил уравнение Клапейрона с законом Авогадро. Согласно закону Авогадро, 1 моль любого идеального газа при одинаковых p и T занимает один и тот же объем Vm, поэтому постоянная В будет одинаковой для всех газов. Эта общая для всех газов постоянная обозначается R и называется универсальной газовой постоянной. Тогда
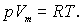
Это уравнение и является уравнением состояния идеального газа, которое также носит название уравнение Клапейрона - Менделеева.
Числовое значение универсальной газовой постоянной можно определить, подставив в уравнение Клапейрона - Менделеева значения p, T и Vm при нормальных условиях:
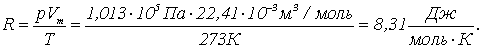
Уравнение Клапейрона - Менделеева можно записать для любой массы газа. Для этого вспомним, что объем газа массы m связан с объемом одного моля формулой V=(m/M)Vm, где М - молярная масса газа. Тогда уравнение Клапейрона - Менделеева для газа массой m будет иметь вид:
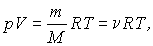
где 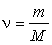 - число молей.
- число молей.
Часто уравнение состояния идеального газа записывают через постоянную Больцмана:
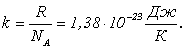
Исходя из этого, уравнение состояния можно представить как
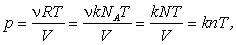
где 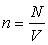 - концентрация молекул. Из последнего уравнения видно, что давление идеального газа прямо пропорционально его температуре и концентрации молекул.
- концентрация молекул. Из последнего уравнения видно, что давление идеального газа прямо пропорционально его температуре и концентрации молекул.
Дата добавления: 2016-01-30; просмотров: 989;
